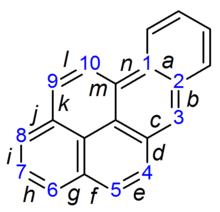
NervesystemetRediger
Prenatal eksponering af BaP hos rotter er kendt for at påvirke indlæring og hukommelse i gnavermodeller. Drægtige rotter, der spiser BaP, har vist sig at påvirke hjernefunktionen negativt i deres afkoms sene liv. På et tidspunkt, hvor synapser først dannes og justeres i styrke af aktivitet, nedsatte BaP NMDA-receptorafhængig nervecelleaktivitet målt som mRNA-ekspression af NMDA NR2B-receptorunderenheden.
ImmunsystemRediger
BaP har en effekt på antallet af hvide blodlegemer og hæmmer nogle af dem i at differentiere sig til makrofager, kroppens første forsvarslinje til at bekæmpe infektioner. I 2016 blev den molekylære mekanisme afsløret som en beskadigelse af makrofagmembranens lipid raft-integritet ved at sænke membranens kolesterol på 25 %. Det betyder, at færre immunreceptorer CD32 (et medlem af Fc-familien af immunreceptorer) kunne binde sig til IgG og forvandle den hvide blodcelle til en makrofag. Derfor bliver makrofagmembranerne modtagelige for bakterieinfektioner.
ReproduktionssystemRediger
I forsøg med hanrotter har subkronisk eksponering for inhaleret BaP vist sig generelt at nedsætte testiklernes og bitestiklernes funktion med lavere produktion af kønssteroider/testosteron og sædproduktion.
Kræftfremkaldende virkningRediger
BaP’s metabolitter er mutagene og stærkt kræftfremkaldende, og det er opført som et kræftfremkaldende stof i gruppe 1 af IARC. Chemical agents and related occupations, Volume 10, A review of Human Carcinogens, IARC Monographs, Lyon France 2009
I juni 2016 blev BaP tilføjet som benzochrysen til REACH-kandidatlisten over særligt problematiske stoffer med henblik på godkendelse.
Numre undersøgelser siden 1970’erne har dokumenteret sammenhænge mellem BaP og kræft. Det har været vanskeligere at knytte kræft til specifikke BaP-kilder, især hos mennesker, og det har været vanskeligere at kvantificere risikoen ved forskellige eksponeringsmetoder (indånding eller indtagelse). En forbindelse mellem A-vitaminmangel og emfysem hos rygere blev i 2005 beskrevet som værende forårsaget af BaP, som fremkalder A-vitaminmangel hos rotter.
En undersøgelse fra 1996 gav molekylære beviser for, at komponenter i tobaksrøg er forbundet med lungekræft. BaP viste sig at forårsage genetiske skader i lungeceller, som var identiske med de skader, der blev observeret i DNA’et i de fleste ondartede lungetumorer.
Regulært forbrug af kogt kød er epidemiologisk set blevet forbundet med et øget niveau af tarmkræft (selv om dette i sig selv ikke beviser kræftfremkaldende virkning).En NCI-undersøgelse fra 2005 viste, at en øget risiko for kolorektal adenomer var forbundet med BaP-indtagelse, og i højere grad med BaP-indtagelse fra alle fødevarer. Fødevarerne i sig selv er dog ikke nødvendigvis kræftfremkaldende, selv om de indeholder spor af kræftfremkaldende stoffer, fordi mave-tarmkanalen beskytter sig selv mod kræft ved løbende at afgive sit yderste lag. Desuden har afgiftende enzymer som f.eks. cytokromer P450 en øget aktivitet i tarmen for at beskytte mod fødevarebårne toksiner. I de fleste tilfælde metaboliseres små mængder BaP således, inden de passerer over i blodet. Lungerne er ikke beskyttet på nogen af disse måder.
Detoxifikationsenzymerne cytokrom P450 1A1 (CYP1A1) og cytokrom P450 1B1 (CYP1B1) er både beskyttende og nødvendige for benzopyrentoksicitet. Forsøg med musestammer, der er konstrueret til at fjerne (knockout) CYP1A1 og CYP1B1, viser, at CYP1A1 primært beskytter pattedyr mod lave doser af BaP, og at fjernelse af denne beskyttelse akkumulerer store koncentrationer af BaP. Medmindre CYP1B1 også slås ud, skyldes toksicitet bioaktivering af BaP til benzopyren-7,8-dihydrodiol-9,10-epoxid, som er den ultimative toksiske forbindelse.
Interaktion med DNAEdit

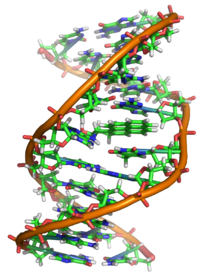
Det er korrekt sagt, at BaP er et procarcinogen, hvilket betyder, at dets mekanisme for carcinogenese afhænger af dets enzymatiske metabolisme til BaP-diolepoxid. Det interkalerer i DNA, og det elektrofil epoxid angribes af nukleofile guaninbaser, hvorved der dannes et voluminøst guaninaddukt.

Røntgenkrystallografiske og kernemagnetiske resonansstrukturundersøgelser har vist, hvordan denne binding forvrænger DNA’et ved at forvirre den dobbelthelikale DNA-struktur. Dette forstyrrer den normale proces med kopiering af DNA og forårsager mutationer, hvilket forklarer forekomsten af kræft efter eksponering. Denne virkningsmekanisme ligner den for aflatoksin, som binder sig til N7-positionen af guanin.
Der er tegn på, at benzopyrendiol epoxid specifikt er rettet mod det beskyttende p53-gen. Dette gen er en transkriptionsfaktor, der regulerer cellecyklus og dermed fungerer som tumorsuppressor. Ved at inducere G (guanin) til T (thymidin) transversioner i transversion hotspots i p53 er der en sandsynlighed for, at benzopyrendiolepoxid inaktiverer tumorundertrykkende evne i visse celler, hvilket fører til kræft.
Benzopyren-7,8-dihydrodiol-9,10-epoxid er det kræftfremkaldende produkt af tre enzymatiske reaktioner:
- Benzopyren oxideres først af cytokrom P450 1A1 til dannelse af en række produkter, herunder (+)benzopyren-7,8-epoxid.
- Dette produkt metaboliseres af epoxidhydrolase, der åbner epoxidringen for at give (-)benzopyren-7,8-dihydrodiol.
- Det endelige carcinogen dannes efter endnu en reaktion med cytokrom P450 1A1 for at give (+)benzopyren-7,8-dihydrodiol-9,10-epoxid. Det er dette diolepoxid, der binder kovalent til DNA.
BaP inducerer cytokrom P4501A1 (CYP1A1) ved at binde sig til AHR (arylhydrogencarbonreceptor) i cytosolen. Ved bindingen translokaliseres den transformerede receptor til kernen, hvor den dimerer med ARNT (arylhydrogencarbonreceptor nuclear translocator) og derefter binder xenobiotiske responselementer (XRE’er) i DNA, der er placeret opstrøms for visse gener. Denne proces øger transkriptionen af visse gener, navnlig CYP1A1, efterfulgt af en øget CYP1A1-proteinproduktion. Denne proces svarer til induktion af CYP1A1 ved visse polychlorerede biphenyler og dioxiner. Tilsyneladende forhindrer CYP1A1-aktivitet i tarmslimhinden, at større mængder af indtaget benzopyren kommer ind i portalblodet og det systemiske kredsløb. Intestinal, men ikke hepatisk, ekspression af CYP1A1 afhænger af TOLL-like receptor 2 (TLR2), som er en eukaryotisk receptor for bakterielle overfladestrukturer såsom lipoteichoesyre.
Dertil kommer, at BaP har vist sig at aktivere et transposon, LINE1, i mennesker.