La estenosis aórtica (EA) valvular es la enfermedad valvular más frecuente en los países desarrollados. El diagnóstico de la EA se confirma clásicamente mediante ecocardiografía, la herramienta estándar para detectar y evaluar la gravedad de la enfermedad (1). Sin embargo, la evaluación de la gravedad de la EA sigue siendo un reto. La EA grave suele definirse como un gradiente medio >40 mmHg, un área de la válvula aórtica (AVA) <1 cm2 y una velocidad máxima del chorro aórtico >4,0 m/s (2). Sin embargo, con frecuencia se observan discrepancias entre el gradiente medio y el área valvular en un mismo paciente (3). Estas discrepancias son fáciles de entender en pacientes con bajo gasto cardíaco secundario a una fracción de eyección del VI reducida, pero también pueden darse en pacientes con una función del VI aparentemente conservada (4). En la práctica diaria, pueden dar lugar a una subestimación de la estenosis y de la gravedad de los síntomas y, por tanto, a un retraso inadecuado de la sustitución de la válvula aórtica (RVA), lo que a su vez puede repercutir negativamente en la evolución del paciente (5-7). En este número de Diagnóstico y Terapia Cardiovascular, OZKAN ha revisado con elegancia el concepto de EA de bajo gradiente en pacientes con función del VI conservada (8).
Nueva clasificación de la estenosis aórtica
Recientemente, varios autores han informado de que bajo la misma denominación de EA grave (AVA <1 cm2), pueden identificarse varias entidades que difieren en cuanto a las tasas de flujo transvalvular y a los gradientes de presión desarrollados (9-11). El primero en subrayar la importancia de integrar la relación válvula-gradiente con el patrón de flujo fue el grupo de Pibarot et al. (5), mientras que Miners et al. (3) fueron los primeros en mostrar claramente las inconsistencias para graduar la gravedad de la EA y en proponer con Dumesnil et al. (6) la nueva clasificación de la EA. En los pacientes con un AVA <1 cm2, pueden identificarse cuatro categorías de EA de gradiente de flujo: flujo normal/gradiente bajo (NF/LG), flujo normal/gradiente alto (NF/HG), flujo bajo/gradiente alto (LF/HG) y flujo bajo/gradiente bajo (LF/LG). El LF se define como un volumen de elevación del VI indexado <35 mL/m2 y el LG como un gradiente medio de presión transaórtica <40 mmHg (12).
Flujo normal-bajo gradiente
Este patrón se observa en el 31-38% de los pacientes y parece identificar a un grupo de pacientes con un grado menos grave de EA -incongruencia inherente a las guías- o que ha estado expuesto a la enfermedad durante un periodo de tiempo más corto. Esta entidad se caracteriza por una función miocárdica longitudinal del VI preservada, lo que se traduce en un nivel de BNP y una puntuación de riesgo de Monin más bajos (12,13). El pronóstico de estos pacientes parece estar relativamente preservado en comparación con las otras categorías.
Flujo normal-alto gradiente
Este patrón representa la entidad más prevalente (39-72%) y es totalmente consistente con los criterios propuestos por las guías (4,5,12). En comparación con el grupo de NF/LG, aunque la función longitudinal del VI está preservada, el BNP es mayor y la tasa de supervivencia libre de eventos cardíacos de la NF/HG es reducida. Además, los pacientes con NF/HG parecen tener una EA más grave, lo que sugiere una exposición más prolongada a esta enfermedad progresiva. Cuando son sintomáticos, estos pacientes son remitidos clásicamente para RVA, mientras que cuando son asintomáticos, el manejo de estos pacientes subraya la necesidad de optimizar la estratificación del riesgo.
Bajo flujo-alto gradiente
Este patrón representa el 8% de los pacientes con EA grave (4,12). Se caracteriza por un volumen de elevación del VI indexado <35 mL/m2 a pesar de una fracción de eyección del VI conservada, un nivel de BNP y una puntuación de riesgo de Monin elevados y una reducción significativa de la función longitudinal del VI (14). Cabe destacar que la fracción de eyección del VI es una estimación cruda de la función sistólica del VI. La fracción de eyección del VI está influida tanto por la función miocárdica intrínseca como por la geometría de la cavidad del VI. Por lo tanto, para un grado similar de acortamiento miocárdico intrínseco, la fracción de eyección del VI tenderá a aumentar en relación con el grado de remodelación concéntrica del VI. Por lo tanto, la fracción de eyección del VI puede subestimar notablemente el grado de deterioro miocárdico en presencia de remodelación concéntrica del VI, como suele ocurrir en los pacientes con EA. Por lo tanto, lo que es normal para un VI con geometría normal puede ser anormal para un VI con remodelación concéntrica. Además, la reducción del gasto del VI (relacionada con la disfunción miocárdica intrínseca y el remodelado significativo del VI) puede, a su vez, dar lugar a gradientes transvalvulares inferiores a los esperados. El pronóstico de estos pacientes es casi idéntico al de los pacientes con NF/HG. Cuando son sintomáticos, estos pacientes tienden a tener una mejor supervivencia si son tratados quirúrgicamente.
Bajo flujo-bajo gradiente
La prevalencia del patrón LF/LG parece ser menor de lo que se informó inicialmente. Esta entidad supone un 7% en pacientes asintomáticos y hasta un 15-35% en pacientes sintomáticos (4-6,12,14). Este patrón, a saber, la EA paradójica de bajo flujo, representa una entidad clínica difícil que se ha puesto de relieve recientemente. Se asocia a un remodelado concéntrico del VI más pronunciado, a una cavidad del VI más pequeña, a un aumento de la poscarga global del VI, a una disfunción miocárdica intrínseca, a una fibrosis miocárdica y a un pronóstico sombrío (12,15). En pacientes asintomáticos, hemos demostrado que la probabilidad de seguir vivo sin RVA a los 3 años era 5 veces menor que en el patrón NF/LG y 4,3 veces mayor que en el grupo NF/HG (12). Esta entidad clínica se diagnostica a menudo de forma errónea, lo que puede llevar a una subestimación de la gravedad de la EA y, por tanto, a una infrautilización o a un retraso inadecuado de la cirugía. Es importante reconocer esta entidad para no negar la cirugía a un paciente sintomático con AVA pequeña y LG.
Discordancia entre el gradiente y el área valvular
Las posibles causas de discordancia entre el AVA y el gradiente en pacientes con fracción de eyección del VI conservada incluyen (I) errores de medición; (II) tamaño corporal pequeño; (III) EA paradójica de bajo flujo; y (IV) clasificación inconsistente relacionada con discrepancias intrínsecas en los criterios de las guías (4,6,7,10,11). En primer lugar, los pacientes con un tamaño corporal y unas dimensiones del VI pequeñas pueden presentar un gradiente de presión transvalvular más bajo debido a un volumen sistólico menor, aunque normal. En segundo lugar, el volumen de carrera y, por lo tanto, el AVA pueden estar subestimados debido a la subestimación del tracto de salida del VI y/o a la colocación errónea del volumen de muestra del Doppler de onda pulsada. Se pueden utilizar varios métodos para corroborar las mediciones Doppler-ecocardiográficas del volumen sistólico y del AVA. Por ejemplo, en ausencia de regurgitación mitral significativa, el volumen sistólico puede estimarse fácilmente mediante el método de Simpson (método volumétrico para medir la fracción de eyección y los volúmenes del VI). Si el volumen de carrera medido por estos métodos independientes es consistente con el volumen de carrera medido en el tracto de salida del VI, uno puede estar tranquilo sobre la exactitud de la medición del volumen de carrera. En tercer lugar, la LF/LG paradójica representa una nueva entidad en la que el estado de LF resulta tanto del remodelado concéntrico del VI como de la reducción de la función longitudinal subendocárdica. Esto pone de manifiesto la ausencia de una estimación errónea de la gravedad de la EA. En cuarto lugar, en algunos casos, la discrepancia en la relación gradiente-área valvular puede estar relacionada con incoherencias en las directrices actuales. Una armonización de la definición de EA grave podría reclasificar a algunos de estos pacientes con EA «grave» en EA «moderada». Cuando se combinan los datos clínicos prospectivos actuales con los datos hemodinámicos anteriores y los datos invasivos, parece que un gradiente de 40 mmHg se ajusta más a un área valvular de 0,8 cm2 mientras que un área valvular de 1 cm2 se relaciona con un gradiente medio de 26 mmHg (3,6,16). Además, cuando hay una discordancia entre el área valvular (en el rango severo) y el gradiente (en el rango moderado) en pacientes con fracción de eyección del VI preservada, puede ser necesaria una evaluación ecocardiográfica Doppler más completa y potencialmente otras pruebas diagnósticas (BNP, puntuación de calcio por tomografía computarizada multicorte, ecocardiografía de esfuerzo con ejercicio/dobutamina) para confirmar la gravedad de la enfermedad y guiar el manejo terapéutico.
Implicaciones clínicas y manejo
En la práctica diaria, la evaluación de la gravedad de la EA debe integrar el patrón de gradiente de flujo a la medición clásica del AVA. Como regla general, un gradiente transvalvular bajo (<40 mmHg) o una velocidad (<4 m/s) no excluye la presencia de una EA grave en pacientes con un AVA pequeño y una fracción de eyección del VI conservada. Además, una fracción de eyección del VI conservada (>50%) no excluye la presencia de disfunción sistólica miocárdica y bajo flujo transvalvular en la EA. Los pacientes con EA NF/LG clásicamente no tienen disfunción subendocárdica o ésta es mínima y tienen un resultado relativamente preservado. En esta categoría NF/LG, la indicación de RVA debe limitarse a los pacientes en los que los síntomas pueden atribuirse claramente a la EA. En la categoría NF/HG, el RVA (quirúrgico o percutáneo) es el único tratamiento que mejora significativamente tanto la supervivencia como los síntomas. Cuando son asintomáticos, la estratificación del riesgo individual puede ayudar a identificar a los pacientes que pueden beneficiarse de una cirugía temprana. En las demás categorías, el estado de FL representa un testimonio de disfunción miocárdica intrínseca y un proceso de enfermedad más avanzado. Los pacientes sintomáticos con LF/HG también deberían beneficiarse de una intervención quirúrgica temprana. Cuando están asintomáticos, también debe fomentarse la estratificación individual del riesgo. La ecocardiografía de ejercicio puede ser de interés al desenmascarar a los pacientes con distensibilidad valvular limitada y/o reserva contráctil del VI agotada (17,18). La LF/LG paradójica conlleva un mal resultado incluso en pacientes asintomáticos. En esta categoría, aunque el beneficio de la cirugía no está demostrado, la RVA puede ser probablemente beneficiosa en pacientes sintomáticos seleccionados (7,19,20) (Tabla 1). En la práctica clínica, determinar esta entidad es un reto. Antes de considerar la intervención quirúrgica, los síntomas deben corresponderse con la gravedad de la EA. En los pacientes de bajo riesgo, se puede recomendar la RVA. En los pacientes de alto riesgo, se necesitan estudios de resultados adicionales para determinar la modalidad y el momento de tratamiento más adecuados.
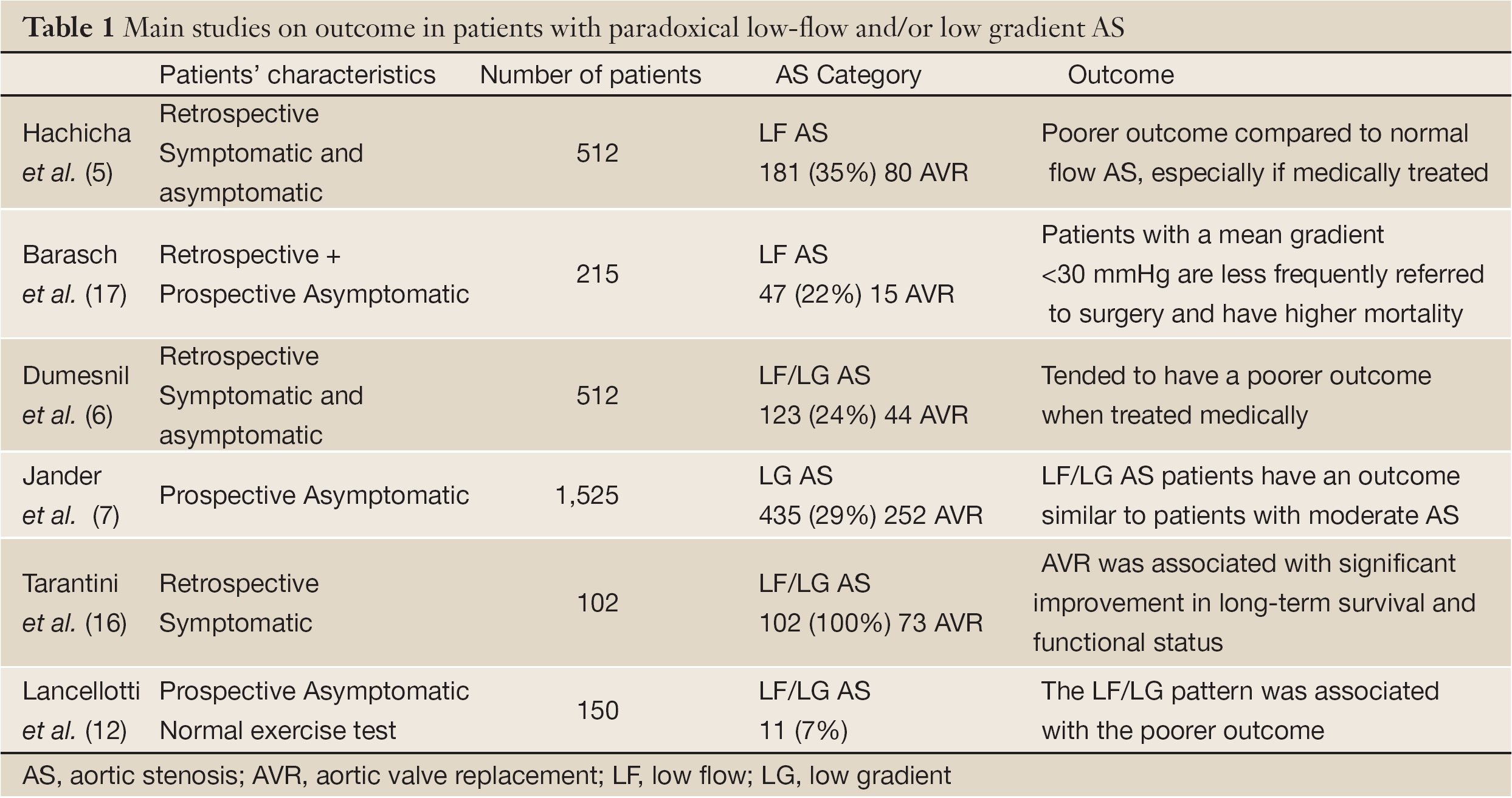
Tabla completa
Agradecimientos
Declaración: Los autores declaran no tener ningún conflicto de intereses.
- Lancellotti P, Donal E, Magne J, et al. Risk stratification in asymptomatic moderate to severe aortic stenosis: the importance of the valvular, arterial and ventricular interplay. Heart 2010;96:1364-71.
- Bonow RO, Carabello BA, Kanu C, et al. ACC/AHA 2006 guidelines for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (writing committee to revise the 1998 Guidelines for the Management of Patients With Valvular Heart Disease): developed in collaboration with the Society of Cardiovascular Anesthesiologists: endorsed by the Society for Cardiovascular Angiography and Interventions and the Society of Thoracic Surgeons. Circulation 2006;114:e84-231.
- Minners J, Allgeier M, Gohlke-Baerwolf C, et al. Clasificación inconsistente de la estenosis de la válvula aórtica según las directrices actuales: estudios hemodinámicos en pacientes con función ventricular izquierda aparentemente normal. Heart 2010;96:1463-8.
- Adda J, Mielot C, Giorgi R, et al. Low-Flow, Low-Gradient Severe Aortic Stenosis Despite Normal Ejection Fraction Is Associated With Severe Left Ventricular Dysfunction as Assessed by Speckle-Tracking Echocardiography: A Multicenter Study. Circ Cardiovasc Imaging 2012;5:27-35.
- Hachicha Z, Dumesnil JG, Bogaty P, et al. La estenosis aórtica severa paradójica de bajo flujo y bajo gradiente a pesar de una fracción de eyección preservada se asocia con una mayor poscarga y una menor supervivencia. Circulation 2007;115:2856-64.
- Dumesnil JG, Pibarot P, Carabello B. Estenosis aórtica grave paradójica de bajo flujo y/o bajo gradiente a pesar de una fracción de eyección ventricular izquierda conservada: implicaciones para el diagnóstico y el tratamiento. Eur Heart J 2010;31:281-9.
- Jander N, Minners J, Holme I, et al. Outcome of patients with low-gradient «severe» aortic stenosis and preserved ejection fraction. Circulation 2011;123:887-95.
- Ozkan A. Estenosis aórtica «severa» de bajo gradiente con fracción de eyección ventricular izquierda preservada. Cardiovasc Diagn Ther 2012;2:19-27.
- Dumesnil JG, Pibarot P, Akins C. New approaches to quantifying aortic stenosis severity. Curr Cardiol Rep 2008;10:91-7.
- Pibarot P, Dumesnil JG. Evaluación de la gravedad de la estenosis aórtica: cuando el gradiente no se ajusta al área valvular. Heart 2010;96:1431-3.
- Lancellotti P, Magne J. Valvuloarterial impedance in aortic stenosis: look at the load, but do not forget the flow. Eur J Echocardiogr 2011;12:354-7.
- Lancellotti P, Magne J, Donal E, et al. Clinical outcome in asymptomatic severe aortic stenosis insights from the new proposed aortic stenosis grading classification. J Am Coll Cardiol 2012;59:235-43.
- Monin JL, Lancellotti P, Monchi M, et al. Risk score for predicting outcome in patients with asymptomatic aortic stenosis. Circulation 2009;120:69-75.
- Lancellotti P, Donal E, Magne J, et al. Impact of global left ventricular afterload on left ventricular function in asymptomatic severe aortic stenosis: a two-dimensional speckle-tracking study. Eur J Echocardiogr 2010;11:537-43.
- Herrmann S, Störk S, Niemann M, et al. Fibrosis miocárdica por estenosis de la válvula aórtica de bajo gradiente y su influencia en la función y el resultado. J Am Coll Cardiol 2011;58:402-12.
- Zoghbi WA. Estenosis aórtica «severa» de bajo gradiente con función sistólica normal: ¿es hora de refinar las directrices? Circulation 2011;123:838-40.
- Lancellotti P, Lebois F, Simon M, et al. Importancia pronóstica de la ecocardiografía Doppler cuantitativa de ejercicio en la estenosis valvular aórtica asintomática. Circulation 2005;112:I377-82.
- Maréchaux S, Hachicha Z, Bellouin A, et al. Usefulness of exercise-stress echocardiography for risk stratification of true asymptomatic patients with aortic valve stenosis. Eur Heart J 2010;31:1390-7.
- Tarantini G, Covolo E, Razzolini R, et al. Reemplazo valvular para la estenosis aórtica severa con bajo gradiente transvalvular y fracción de eyección ventricular izquierda superior a 0,50. Ann Thorac Surg 2011;91:1808-15.
- Barasch E, Fan D, Chukwu EO, et al. Estenosis aórtica aislada grave con función sistólica ventricular izquierda normal y gradientes transvalvulares bajos: perspectivas fisiopatológicas y pronósticas. J Heart Valve Dis 2008;17:81-8.