Introducción
El SCB es un grupo heterogéneo de trastornos caracterizados por la obstrucción del flujo venoso hepático a varios niveles desde las venas hepáticas pequeñas (VH) hasta la unión de la vena cava inferior (VCI) y la aurícula derecha.1 Se trata de una enfermedad rara, con una prevalencia registrada en China del 0,0065%.2 El SCB puede clasificarse en los tipos primario y secundario según su causa: El tipo primario se refiere a la obstrucción congénita de las venas hepáticas o de la porción hepática de la VCI. El tipo secundario se refiere a la obstrucción de las mismas estructuras anatómicas por un tumor o, más comúnmente, por trombos o trombos en pacientes con enfermedades sistémicas, generalmente trastornos mieloproliferativos.3 El tipo primario de SBC es más común en los países orientales y en África, mientras que el tipo secundario es más común en los países occidentales.
La malformación de Abernethy es una derivación portosistémica anormal congénita rara, descrita por primera vez por John Abernethy en 1793. Constituye una desviación de la sangre portal fuera del hígado mediante una derivación de extremo a extremo o de lado a lado.4 Morgan y Superina clasificaron la derivación portosistémica extrahepática congénita en dos tipos:5 El tipo I, en el que la sangre portal se desvía completamente hacia la VCI con ausencia de la vena porta (VP) y se asocia con insuficiencia hepática y tumores hepáticos; y el tipo II, en el que la VP está intacta y, por tanto, tiene mejor pronóstico. Hasta el año 2016, sólo se habían descrito 101 casos de malformación de Abernethy6, y ninguno se combinó con la BCS. Aquí presentamos un caso de SCB combinado y malformación de Abernethy tipo II diagnosticado mediante ultrasonografía dúplex y angiografía por tomografía computarizada (TC).
Informe de caso
Este estudio fue aprobado por el comité ético del Primer Hospital Afiliado de la Universidad de Zhengzhou. Una mujer de 60 años ingresó en el Departamento de Intervención con una historia de 10 años de venas prominentes de la pared abdominal, distensión abdominal e hinchazón leve de ambas piernas. La exploración física reveló muchas venas subcutáneas prominentes dilatadas con flujo ascendente en la pared abdominal, hígado y bazo palpables y edema leve de las piernas sin varices, pigmentación ni úlceras. La encefalopatía hepática no era evidente. Los valores de amoníaco en sangre y los índices de la función hepática y renal estaban en el rango normal, con la excepción del recuento de plaquetas (33 x 109/L) consistente con un leve hiperesplenismo.
El TAC preoperatorio con contraste reveló una marcada atrofia del lóbulo derecho del hígado y un agrandamiento compensatorio del lóbulo izquierdo, sin masa hepática, y esplenomegalia. Los hallazgos vasculares fueron una obstrucción membranosa de la VCI con dilatación de los afluentes lumbares superiores y de las venas hemiáceas/azigosas (Figura 1A); una obstrucción de todo el recorrido de la VH derecha; una obstrucción membranosa de la VH media y de la VH izquierda en el orificio de la VH (Figura 1B); y una vena frénica y una vena pericárdica dilatadas, que drenaban sangre de la VH media y de la VH izquierda a la vena cava superior. Las imágenes de fase venosa portal revelaron una anastomosis de lado a lado de 2 mm de diámetro entre la VP y la VCI (Figura 1C). Las venas esplénica y mesentérica superior estaban orientadas normalmente y se unían para formar la VP principal. Estos resultados coincidían con los de la ecografía Doppler abdominal (figura 2). Se realizó el diagnóstico de malformación de Abernethy de tipo II y BCS.
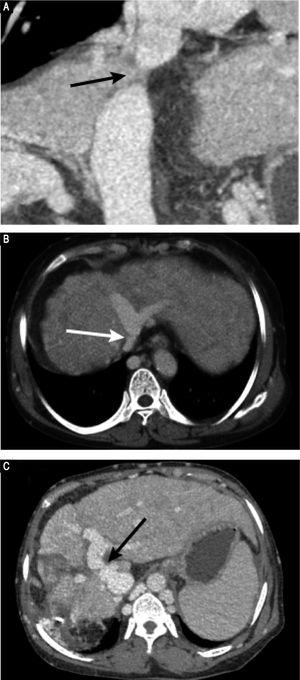
Imágenes preoperatorias de TC. A. La angiografía por TC revela una obstrucción membranosa de la VCI intrahepática (flecha). B. La TC axial en fase porta venosa revela que no se puede visualizar la VH derecha; el coorificio de la VH media y la VH izquierda tienen una obstrucción membranosa; y las venas ácigos y hemiácigos están marcadamente dilatadas (flecha). C. La TC axial en fase venosa porta revela una anastomosis de lado a lado (flecha) entre la vena porta y la VCI, un hallazgo compatible con una malformación de Abernethy de tipo II.
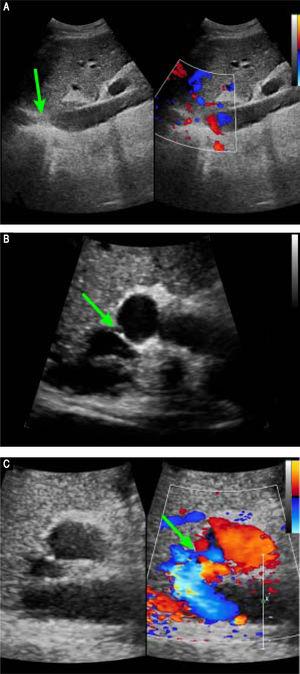
Imágenes ecográficas Doppler preoperatorias. A. Las imágenes de ecografía bidimensional abdominal y de ecografía Doppler tridimensional revelan una obstrucción membranosa de la VCI intrahepática sin flujo sanguíneo (flecha). B. La ecografía bidimensional abdominal y las imágenes de ecografía Doppler revelan que el coorificio de la VH media y la VH izquierda tienen una obstrucción membranosa y no hay flujo sanguíneo, C. La ecografía bidimensional abdominal y las imágenes de ecografía Doppler revelan una conexión anormal (flecha) entre la vena porta y la VCI.
Basado en estos hallazgos, realizamos una angioplastia percutánea con balón (ABP) para la VCI obstruida. Para la malformación de Abernethy, elegimos un tratamiento conservador porque la paciente estaba asintomática y el diámetro de la derivación era pequeño. Para el procedimiento de ABP, primero realizamos una vena cavagráfica inferior a través de la vena femoral derecha para identificar la anatomía y la localización de la sección ocluida de la VCI (Figura 3A). A continuación, se introdujo por vía transfemoral una aguja de acero roma de fabricación propia en la parte distal de la obstrucción para romper la membrana obstructiva de la VCI. A continuación, se introdujo un alambre de intercambio súper rígido y se colocó en la vena cava superior a través de la VCI obstruida. Se realizó una PTBA de la obstrucción de la membrana de la VCI con un catéter de balón de 25 mm de diámetro (Cook Medical, Bloomington, IN, EE.UU.) (Figura 3B). Después de la PTBA, la presión de la VCI había disminuido de 19 a 10 cm H2O, y la cavidad de la vena inferior reveló un flujo sanguíneo adecuado de la VCI y ninguna estenosis (Figura 3C).
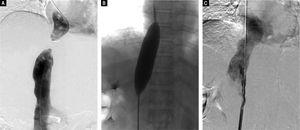
Imágenes de angiografía de sustracción digital. A. El cavograma de la vena inferior por vía yugular y por vía femoral revela una obstrucción completa de la VCI intrahepática, que confirmó los resultados de la ecografía Doppler y la angiografía por TC. B. Dilatación de la VCI obstruida con un balón de 25 mm de diámetro tras la ruptura exitosa de la membrana, C. El cavograma de la vena inferior inmediatamente después de la angioplastia con balón revela la permeabilidad de la VCI sin estenosis residual.
Se administró heparina de bajo peso molecular (4.100 U/12 h, por vía subcutánea) inmediatamente después del procedimiento y se continuó durante 5 días. La warfarina (5 mg/día, por vía oral) se administró a partir del segundo día y durante un año después de la intervención con una relación internacional normalizada de 2-3. Las varices subcutáneas de la pared abdominal habían disminuido notablemente al segundo día de la intervención. La encefalopatía hepática no se ha producido en ningún momento desde que se realizó el procedimiento y, a los 6 meses de seguimiento, la ecografía Doppler reveló que la VCI era patente.
Discusión
En nuestra paciente, tanto la VH como la VCI tenían obstrucción membranosa. La obstrucción del VH estaba compensada por las venas frénicas y pericárdicas dilatadas, por lo que el paciente no presentaba signos ni síntomas de hipertensión portal, como ascitis y hemorragia por varices esofágicas y gástricas. Dado que la hipertensión de la VCI era la principal manifestación clínica del paciente, sólo se trató la VCI obstruida, y no se utilizó ni la recanalización de la VH ni la derivación portosistémica intrahepática transyugular.
Dado que la VCI obstruida de nuestro paciente era de tipo membranoso, la PTBA era el tratamiento más adecuado. Lo realizamos y fue exitoso. La PTBA es el tratamiento más común del SCB en los países asiáticos y africanos y ha demostrado ser eficaz en la mayoría de los pacientes, con el alivio de la obstrucción venosa sintomática y el restablecimiento del flujo venoso normal y la prevención de la enfermedad hepática progresiva.7 Cuando hay estenosis residual o reoclusión de los vasos poco después de la PTBA, la colocación de un stent puede ser un tratamiento exitoso.8
En general, el tratamiento de las malformaciones congénitas del sistema portal depende del tipo de derivación, los síntomas que se presentan, las anomalías congénitas coexistentes, la injuria hepática, las complicaciones y la comorbilidad. El determinante más importante parece ser el tipo de lesión.5 En el caso de los niños con una derivación de tipo I, debe considerarse el cierre quirúrgico, pero si no es posible, está indicado un seguimiento estrecho. Con la experiencia clínica y los avances tecnológicos, cada vez más pacientes son candidatos a la cirugía. Sin embargo, no se ha descrito ninguna estrategia quirúrgica para los pacientes adultos con una derivación de tipo II. Cuando estos pacientes presentan síntomas graves, como encefalopatía hepática o hemorragia colateral, la derivación debe cerrarse pronto, lo que puede ayudar a evitar el desarrollo de congestión venosa mesentérica.4,9,10
Los tratamientos reportados de las malformaciones de Abernathy incluyen operaciones, como el cierre de la derivación, la resección del nódulo hepático, el trasplante de hígado, y el tratamiento intervencionista, como la obliteración percutánea con balón, la embolización transcatéter percutánea con espirales o tapones metálicos, la colocación de stents y la colocación de injertos de stent.11,12 En los últimos años, ha habido una tendencia hacia el uso del tratamiento intervencionista. Por las razones expuestas, decidimos no tratar la malformación de Abernathy de nuestra paciente, sino vigilar estrechamente los hallazgos clínicos, bioquímicos y de imagen de la paciente.
En resumen, hemos presentado el primer caso que conocemos de malformación combinada de BCS y Abernathy tipo II en China. La oclusión membranosa de la VCI se trató con PTBA; la malformación de Abernathy no se trató debido a su pequeño diámetro y al estado asintomático de la paciente.
Abreviaturas
- –
SBC: Síndrome de Budd-Chiari.
- –
TC: tomografía computarizada.
- –
VH: vena hepática.
- –
IVC: vena cava inferior.
- –
PTBA: angioplastia percutánea con balón.
- –
VP: vena porta
Conflicto de intereses
Los autores declaran que no existe ningún conflicto de intereses en relación con la publicación de este informe de caso.
Agradecimientos
Agradecemos al Dr. Yan Zhang del Departamento de Ecografía, y al Primer Hospital Afiliado de la Universidad de Zhengzhou por su ayuda en el seguimiento de los pacientes y la preparación de las imágenes ecográficas.