Valvulaarinen aorttastenoosi (AS) on yleisin läppävika kehittyneissä maissa. AS:n diagnoosi varmistetaan klassisesti kaikukardiografialla, joka on vakioväline taudin havaitsemiseen ja vaikeusasteen arviointiin (1). AS:n vaikeusasteen arviointi on kuitenkin edelleen haastavaa. Vaikea AS määritellään yleensä keskimääräiseksi gradientiksi >40 mmHg, aorttaläpän pinta-alaksi (AVA) <1 cm2 ja aorttasuihkun huippunopeudeksi >4,0 m/s (2). Keskimääräisen gradientin ja läppäpinta-alan välillä havaitaan kuitenkin usein eroja yksittäisen potilaan kohdalla (3). Nämä eroavaisuudet on helppo ymmärtää potilailla, joilla on alhainen sydämen teho LV:n pienentyneen ejektiofraktion vuoksi, mutta niitä voi esiintyä myös potilailla, joilla LV:n toiminta on näennäisesti säilynyt (4). Päivittäisessä käytännössä ne voivat mahdollisesti johtaa ahtauman ja oireiden vakavuuden aliarviointiin ja siten aorttaläpän vaihdon epätarkoituksenmukaiseen viivästymiseen, millä puolestaan voi olla kielteinen vaikutus potilaan lopputulokseen (5-7). Tässä Cardiovascular Diagnosis and Therapy -lehden numerossa OZKAN on tyylikkäästi tarkastellut matalan gradientin AS:n käsitettä potilailla, joiden LV-toiminta on säilynyt (8).
Uusi aorttastenoosin luokitteluluokitus
Viime aikoina useat kirjoittajat ovat raportoineet, että saman vaikean AS:n nimityksen (AVA <1 cm2) alla voidaan tunnistaa useita entiteettejä, jotka eroavat toisistaan transvalvulaaristen virtausnopeuksien ja kehittyvien painegradienttien suhteen (9-11). Ensimmäisenä Pibarotin ja muiden ryhmä (5) korosti läppä-gradienttisuhteen yhdistämisen merkitystä virtausmalliin, kun taas Miners ja muut (3) osoittivat ensimmäisenä selvästi AS:n vaikeusasteen luokittelun epäjohdonmukaisuudet ja ehdottivat yhdessä Dumesnilin ja muiden kanssa (6) uutta AS:n luokitusta. Potilailla, joilla on AVA <1 cm2, voidaan tunnistaa neljä virtausgradientin AS-luokkaa: normaali virtaus/matala gradientti (NF/LG), normaali virtaus/korkea gradientti (NF/HG), matala virtaus/korkea gradientti (LF/HG) ja matala virtaus/matala gradientti (LF/LG). LF määritellään indeksoiduksi LV-iskutilavuudeksi <35 ml/m2 ja LG keskimääräiseksi trans-aortan painegradientiksi <40 mmHg (12).
Normaali virtaus – matala gradientti
Tämä kuvio havaitaan 31-38 %:lla potilaista, ja se näyttäisi yksilöivän potilasryhmän, jolla on lievempi AS-oireyhtymä – ohjeisiin sisältyvä epäjohdonmukaisuus – tai joka on altistunut AS:lle lyhyemmän aikaa. Tälle kokonaisuudelle on ominaista, että LV:n pitkittäinen sydänlihaksen toiminta on säilynyt, mikä johtaa alhaisempaan BNP-tasoon ja Moninin riskipisteytykseen (12,13). Näiden potilaiden ennuste näyttää olevan suhteellisen säilynyt verrattuna muihin luokkiin.
Normaali virtaus – korkea gradientti
Tämä kuvio edustaa yleisintä kokonaisuutta (39-72 %), ja se vastaa täysin suuntaviivoissa ehdotettuja kriteerejä (4,5,12). Verrattuna NF/LG-ryhmään, vaikka LV:n pituussuuntainen toiminta säilyy, BNP on korkeampi ja NF/HG:n sydäntapahtumavapaa eloonjäämisaste on alhaisempi. Lisäksi NF/HG-potilailla näyttäisi olevan vaikeampi AS, mikä viittaa siihen, että potilaat altistuvat tälle etenevälle taudille pidempään. Kun nämä potilaat oireilevat, heidät ohjataan klassisesti AVR:ään, kun taas kun he ovat oireettomia, näiden potilaiden hoidossa korostuu tarve optimoituun riskistratifikaatioon.
Matalan virtauksen ja korkean gradientin
Tämä kuvio on 8 prosentilla potilaista, joilla on vaikea AS (4,12). Sille on ominaista indeksoitu LV:n iskutilavuus <35 ml/m2 huolimatta säilyneestä LV:n ejektiofraktiosta, korkeasta BNP-tasosta ja Moninin riskipisteytyksestä sekä LV:n pitkittäistoiminnan merkittävästä heikkenemisestä (14). On huomattava, että LV:n ejektiofraktio on karkea arvio LV:n systolisesta toiminnasta. LV:n ejektiofraktioon vaikuttavat sekä sydänlihaksen sisäinen toiminta että LV-ontelon geometria. Näin ollen sydänlihaksen sisäisen lyhenemisen ollessa samassa määrin LV:n ejektiofraktio pyrkii kasvamaan suhteessa LV:n konsentrisen uudelleenmuodostuksen laajuuteen. LV:n ejektiofraktio voi näin ollen aliarvioida selvästi sydänlihaksen vajaatoiminnan laajuutta, kun kyseessä on LV:n konsentrinen uudelleenmuodostus, kuten AS-potilailla yleensä on. Näin ollen se, mikä on normaalia LV:lle, jolla on normaali geometria, voi olla epänormaalia LV:lle, jolla on konsentrinen remodelling. Lisäksi LV-tuoton väheneminen (joka liittyy sydänlihaksen sisäiseen toimintahäiriöön ja merkittävään LV:n uudelleenmuodostukseen) voi puolestaan johtaa odotettua pienempiin transvalvulaarisiin gradientteihin. Näiden potilaiden lopputulos on lähes sama kuin NF/HG-potilailla. Kun nämä potilaat oireilevat, heidän eloonjäämisensä on yleensä parempi, jos heidät hoidetaan kirurgisesti.
Low flow-low gradient
LF/LG-kuvion esiintyvyys näyttää olevan pienempi kuin mitä alun perin raportoitiin. Tämän kokonaisuuden osuus on 7 % oireettomilla potilailla ja jopa 15-35 % oireisilla potilailla (4-6,12,14). Tämä kuvio, nimittäin paradoksaalinen matalan virtauksen AS, edustaa haastavaa kliinistä kokonaisuutta, jota on viime aikoina korostettu. Se liittyy voimakkaampaan LV:n konsentriseen uudelleenmuodostukseen, pienempään LV-onteloon, lisääntyneeseen LV:n globaaliin jälkikuormitukseen, sydänlihaksen sisäiseen toimintahäiriöön, sydänlihaksen fibroosiin ja huonoon ennusteeseen (12,15). Oireettomilla potilailla olemme osoittaneet, että todennäköisyys pysyä hengissä ilman AVR:ää kolmen vuoden kuluttua oli 5-kertainen NF/LG-malliin verrattuna ja 4,3-kertainen NF/HG-ryhmään verrattuna (12). Tämä kliininen kokonaisuus diagnosoidaan usein väärin, mikä voi johtaa AS:n vaikeusasteen aliarviointiin ja siten leikkauksen alikäyttöön tai epätarkoituksenmukaiseen viivästymiseen. On tärkeää tunnistaa tämä kokonaisuus, jotta leikkausta ei kielletä oireiselta potilaalta, jolla on pieni AVA ja LG.
Gradientin ja läppäpinta-alan välinen epäjohdonmukaisuus
Potilailla, joilla on säilynyt LV:n ejektiofraktio, AVA:n ja gradientin välisen epäjohdonmukaisuuden mahdollisia syitä ovat mm. seuraavat: (I) mittausvirheet, (II) pieni elimistön koko, (III) paradoksaalinen matalavirtauksinen AS ja (IV) ohjeiden kriteereihin sisältyviin luontaisiin eroavuuksiin liittyvä epäjohdonmukainen luokittelu (4,6,7,10,11). Ensinnäkin potilailla, joilla on pieni ruumiinkoko ja LV:n mitat, voi olla pienempi transvalvulaarinen painegradientti pienemmän, vaikkakin normaalin iskutilavuuden vuoksi. Toiseksi aivohalvaustilavuus ja näin ollen AVA voi olla aliarvioitu, koska LV:n ulosvirtauskanava on aliarvioitu ja/tai pulssiaaltodopplerin näytemäärä on sijoitettu väärin. Doppler-ekokardiografisten aivohalvaustilavuuden ja AVA:n mittausten vahvistamiseksi voidaan käyttää useita menetelmiä. Jos esimerkiksi merkittävää mitraaliregurgitaatiota ei ole, aivohalvaustilavuus voidaan helposti arvioida Simpsonin menetelmällä (volumetrinen menetelmä, jolla mitataan LV:n ejektiofraktio ja tilavuudet). Jos näillä riippumattomilla menetelmillä mitattu aivohalvaustilavuus vastaa LV:n ulosvirtauskanavasta mitattua aivohalvaustilavuutta, voidaan olla varmoja aivohalvaustilavuuden mittauksen tarkkuudesta. Kolmanneksi paradoksaalinen LF/LG edustaa uutta kokonaisuutta, jossa LF-tila on seurausta sekä LV:n konsentrisesta uudelleenmuodostuksesta että subendokardiaalisen pitkittäistoiminnan heikkenemisestä. Tämä hahmottaa sen, ettei AS:n vaikeusastetta voida arvioida virheellisesti. Neljänneksi, joissakin tapauksissa gradientti-venttiilipinta-alan suhteen epäsuhta voi liittyä nykyisten ohjeiden epäjohdonmukaisuuksiin. Vaikean AS:n määritelmän yhdenmukaistaminen voi luokitella osan näistä potilaista, joilla on ”vaikea” AS, uudelleen ”kohtalaiseksi” AS:ksi. Kun yhdistetään nykyiset prospektiiviset kliiniset tiedot aikaisempiin hemodynaamisiin kaiku- ja invasiivisiin tietoihin, näyttää siltä, että 40 mmHg:n gradientti sopii paremmin yhteen 0,8 cm2 :n läppäpinta-alan kanssa, kun taas 1 cm2 :n läppäpinta-ala vastaa 26 mmHg:n keskimääräistä gradienttia (3,6,16). Kun läppäpinta-ala (vaikealla alueella) ja gradientti (kohtalaisella alueella) poikkeavat toisistaan potilailla, joilla on säilynyt LV:n ejektiofraktio, saatetaan lisäksi tarvita kattavampaa Doppler-keuhkokardiografista arviointia ja mahdollisesti muita diagnostisia testejä (BNP, kalsiumpisteytys monilevyisessä tietokonetomografiassa, rasitus-/dobutamiinirasituskeuhkokardiografia), jotta voidaan varmistua taudin vaikeusasteesta ja ohjata terapeuttista hoitoa.
Kliiniset vaikutukset ja hoito
Päivittäisessä käytännössä AS:n vaikeusasteen arvioinnissa virtauksen gradienttikuvio olisi sisällytettävä klassiseen AVA:n mittaukseen. Yleissääntönä voidaan todeta, että alhainen transvalvulaarinen gradientti (<40 mmHg) tai nopeus (<4 m/s) ei sulje pois vakavan AS:n esiintymistä potilailla, joilla on pieni AVA ja säilynyt LV:n ejektiofraktio. Lisäksi säilynyt LV:n ejektiofraktio (>50 %) ei sulje pois sydänlihaksen systolisen toimintahäiriön ja alhaisen transvalvulaarisen virtauksen esiintymistä AS:ssä. Potilailla, joilla on NF/LG AS, ei yleensä ole subendokardiaalista toimintahäiriötä tai se on minimaalinen, ja heidän lopputuloksensa on suhteellisen säilynyt. Tässä NF/LG-luokassa AVR:n indikaatio olisi rajoitettava potilaisiin, joiden oireet voidaan selvästi liittää AS:ään. Luokassa NF/HG AVR (kirurginen tai perkutaaninen) on ainoa hoito, joka parantaa merkittävästi sekä elossaoloaikaa että oireita. Kun potilaat ovat oireettomia, yksilöllinen riskistratifiointi voi auttaa tunnistamaan potilaat, jotka voivat hyötyä varhaisesta leikkauksesta. Muissa luokissa LF-tila on todiste sydänlihaksen sisäisestä toimintahäiriöstä ja pidemmälle edenneestä tautiprosessista. Oireisten potilaiden, joilla on LF/HG, pitäisi myös hyötyä nopeasta AVR:stä. Kun potilaat ovat oireettomia, olisi myös kannustettava yksilölliseen riskinmääritykseen. Rasituskaikukardiografia voi olla hyödyllinen, sillä se voi paljastaa potilaat, joilla on rajoittunut läpän compliance ja/tai loppunut LV:n supistumisreservi (17,18). Paradoksaalinen LF/LG merkitsee huonoa lopputulosta myös oireettomilla potilailla. Vaikka leikkauksesta saatavaa hyötyä ei ole todistettu, AVR voi todennäköisesti olla hyödyksi valikoiduille oireisille potilaille (7,19,20) (taulukko 1). Kliinisessä käytännössä tämän kokonaisuuden toteaminen on haastavaa. Ennen kuin leikkausta harkitaan, oireet on sovitettava yhteen AS:n vaikeusasteen kanssa. Matalan riskin potilailla voidaan suositella AVR:ää. Suuren riskin potilailla tarvitaan lisätulostutkimuksia, jotta voidaan määrittää sopivin hoitomuoto ja hoidon ajoitus.
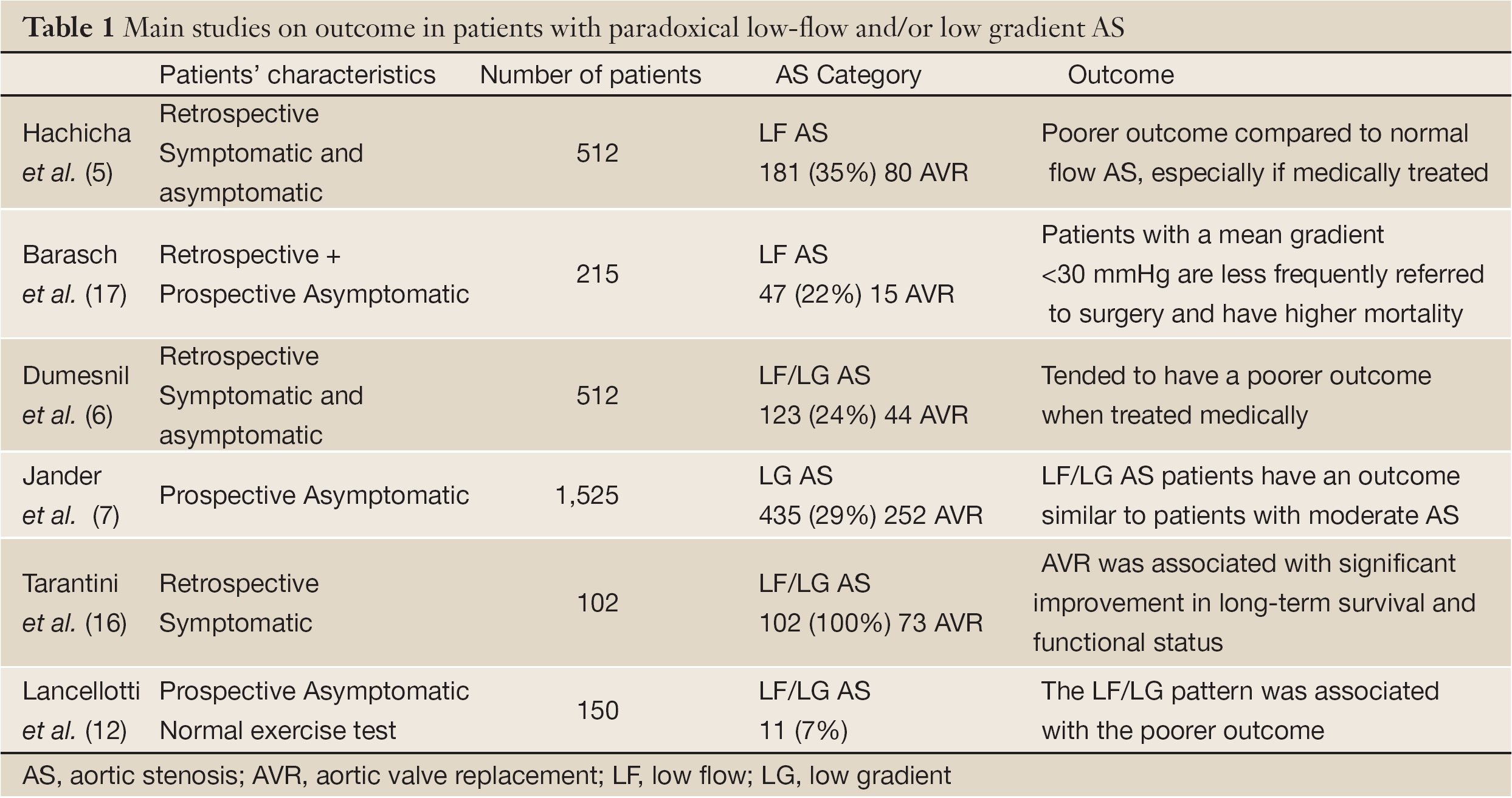
Täydellinen taulukko
Kiitokset
Tiedonantovelvollisuus: Kirjoittajilla ei ole eturistiriitoja.
- Lancellotti P, Donal E, Magne J, et al. Riskistratifiointi oireettomassa keskivaikeassa ja vaikeassa aorttastenoosissa: Valvulaarisen, arteriaalisen ja ventrikulaarisen vuorovaikutuksen merkitys. Heart 2010;96:1364-71.
- Bonow RO, Carabello BA, Kanu C, et al. ACC/AHA 2006 guidelines for the management of patients with valveular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (writing committee to revise the 1998 Guidelines for the Management of Patients With Valvular Heart Disease): kehitetty yhteistyössä sydän- ja verisuonitautilääkärien anestesiologiyhdistyksen (Society of Cardiovascular Anesthesiologists) kanssa: hyväksytty sydän- ja verisuonitautien angiografia- ja toimenpideliitossa (Society for Cardiovascular Angiography and Interventions) ja rintakirurgiyhdistyksessä. Circulation 2006;114:e84-231.
- Minners J, Allgeier M, Gohlke-Baerwolf C, et al. Inconsistent grading of aortic valve stenosis by current guidelines: haemodynamic studies in patients with apparently normal left ventricular function. Heart 2010;96:1463-8.
- Adda J, Mielot C, Giorgi R, et al. Low-Flow, Low-Gradient Severe Aortic Stenosis Despite Normal Ejection Fraction Is Associated With Severe Left Ventricular Dysfunction as Assessed by Speckle-Tracking Echocardiography: A Multicenter Study. Circ Cardiovasc Imaging 2012;5:27-35.
- Hachicha Z, Dumesnil JG, Bogaty P, et al. Paradoxical low-flow, low-gradient severe aortic stenosis despite preserved ejection fraction is associated with higher afterload and reduced survival. Circulation 2007;115:2856-64.
- Dumesnil JG, Pibarot P, Carabello B. Paradoxical low flow and/or low gradient severe aortic stenosis despite preserved left ventricular ejection fraction: implications for diagnosis and treatment. Eur Heart J 2010;31:281-9.
- Jander N, Minners J, Holme I, et al. Outcome of patients with low-gradient ”severe” aortic stenosis and preserved ejection fraction. Circulation 2011;123:887-95.
- Ozkan A. Low gradient ”severe” aortic stenosis with preserved left ventricular ejection fraction. Cardiovasc Diagn Ther 2012;2:19-27.
- Dumesnil JG, Pibarot P, Akins C. New approaches to quantifying aortic stenosis severity. Curr Cardiol Rep 2008;10:91-7.
- Pibarot P, Dumesnil JG. Aorttastenoosin vaikeusasteen arviointi: kun gradientti ei sovi venttiilin pinta-alaan. Heart 2010;96:1431-3.
- Lancellotti P, Magne J. Valvuloarteriaalinen impedanssi aorttastenoosissa: katso kuormitusta, mutta älä unohda virtausta. Eur J Echocardiogr 2011;12:354-7.
- Lancellotti P, Magne J, Donal E, et al. Clinical outcome in asymptomatic severe aortic stenosis insights from the new proposed aortic stenosis grading classification. J Am Coll Cardiol 2012;59:235-43.
- Monin JL, Lancellotti P, Monchi M, et al. Riskipisteytys lopputuloksen ennustamiseksi potilailla, joilla on oireeton aorttastenoosi. Circulation 2009;120:69-75.
- Lancellotti P, Donal E, Magne J, et al. Impact of global left ventricular afterload on left ventricular function in asymptomatic severe aortic stenosis: a two-dimensional speckle-tracking study. Eur J Echocardiogr 2010;11:537-43.
- Herrmann S, Störk S, Niemann M, et al. Low-gradient aorttaläpän ahtauma myocardial fibrosis and its influence on function and outcome. J Am Coll Cardiol 2011;58:402-12.
- Zoghbi WA. Matala-asteinen ”vaikea” aorttaläpän ahtauma, jolla on normaali systolinen toiminta: aika tarkentaa ohjeita? Circulation 2011;123:838-40.
- Lancellotti P, Lebois F, Simon M, et al. Prognostic importance of quantitative exercise Doppler echocardiography in asymptomatic valvular aortic stenosis. Circulation 2005;112:I377-82.
- Maréchaux S, Hachicha Z, Bellouin A, et al. Usefulness of exercise-stress echocardiography for risk stratification of true asymptomatic patients with aortic valve stenosis. Eur Heart J 2010;31:1390-7.
- Tarantini G, Covolo E, Razzolini R, et al. Valve replacement for severe aortic stenosis with low transvalvular gradient and left ventricular ejection fraction exceeding 0.50. Ann Thorac Surg 2011;91:1808-15.
- Barasch E, Fan D, Chukwu EO, et al. Severe isolated aortic stenosis with normal left ventricular systolic function and low transvalvular gradients: pathophysiologic and prognostic insights. J Heart Valve Dis 2008;17:81-8.
.