INTRODUCTION
Diagnostiikka- ja leikkaustekniikoiden sekä postoperatiivisen hoidon kehittymisestä huolimatta akuuttiin A-tyypin aortan dissekaatioon liittyy edelleen korkea sairastuvuus ja kuolleisuus lyhyellä ja pitkällä aikavälillä. Tämänhetkisen sairaalakuolleisuuden on arvioitu olevan 15-35 %, ja viiden vuoden eloonjäämisprosentti on 65-75 %.1-7
Suuren postoperatiivisen aivohalvauksen esiintyvyys näillä potilailla (10-20 %)3,5,7,8 on yhdistetty riittämättömään aivosuojaan verenkierron pysähdyksen aikana, embolisiin tapahtumiin tai huonoon perfuusioon, joka aiheutuu siitä, että veren virtaus kulkee mieluummin väärästä luumenista, kun perfuusio tapahtuu reisivaltimon avulla.9,10,10. Viime vuosina uusien aivojen suojaustekniikoiden, kuten selektiivisen antegradan aivoperfuusion ja kainalovaltimon kanyloinnin, käyttöönotto on vähentänyt huomattavasti tämän komplikaation esiintyvyyttä.10-17.
Tämän retrospektiivisen tutkimuksen tarkoituksena on kuvata kokemuksiamme akuutista tyypin A aortan dissekaatioleikkauksesta – suhteessa sairaalakuolleisuuteen, uusintatoimenpiteiden esiintyvyyteen ja pitkäaikaiseen eloonjäämiseen – ja analysoida aivosuojauksen vaikutusta tuloksiimme.
MENETELMÄT
Maaliskuun 1990 ja lokakuun 2007 välisenä aikana sairaalassamme leikattiin akuutin tyypin A aortan dissekaatioleikkauksen vuoksi 98 peräkkäistä potilasta (79 miestä ja 19 naista). Tänä aikana diagnosoiduista ja leikkaukseen lähetetyistä potilaista (103) viisi jätettiin pois; kaksi potilasta yli 85-vuotiaana ja muut, koska heillä oli peruuttamattomia aivo- tai viskeraalisia vaurioita.
Mediaani-ikä oli 59 vuotta. Yleisin oire potilaan tullessa oli akuutti rintakipu. Diagnoosi varmistettiin alkuvaiheen aortografialla (18 %), transthorakaalisella kaikukardiografialla (76 %), transesofageaalisella kaikukardiografialla (66 %) ja thorako-abdominaalisella tietokonetomografialla (CT) (65 %). Lukuun ottamatta 11 potilasta, joille tehtiin vain yksi diagnostinen testi, kaikki potilaat diagnosoitiin käyttämällä kahta tai kolmea näistä kuvantamismenetelmistä yhdistelmänä (tällä hetkellä käytetty diagnostinen järjestelmä on thorakoabdominaalinen tietokonetomografia, johon on yhdistetty tai johon ei ole yhdistetty tranthorakaalista kaikukardiografiaa ja intraoperatiivista transesofageaalista kaikukardiografiaa).
Yhteensä 91 (93 %) potilaalle tehtiin hätäleikkaus (24 tunnin kuluessa) ja lopuille tehtiin kiireellinen leikkaus (72 tunnin kuluessa diagnoosin tekemisestä).
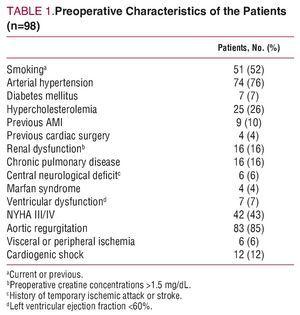
Kuvantamistutkimukset osoittivat aortan regurgitaation 83 potilaalla (55 %:lla oli vaikea regurgitaatio). Leikkausta edeltävät kliiniset ja demografiset ominaisuudet on esitetty taulukossa 1.
Kirurginen tekniikka
Kirurgisen toimenpiteen peruskonsepteihin kuuluu nousevan aortan tai aortan kaaren korvaaminen, primaarisen repeämän resektio ja distaalisen anastomoosin valmistelu verenkierron pysäytyksen aikana. Tämän 18 vuoden aikana tämän patologian kirurginen strategia on kehittynyt asteittain. Aluksi vain nouseva aortta resekoitiin ja aortta puristettiin ilman verenkiertopysähdystä. Vuonna 1994 otettiin käyttöön distaalinen anastomoosi verenkierron pysäyttämisen yhteydessä, mikä on nykyisin tekniikka, jota käytetään kaikilla potilailla, ja samalla sovelletaan erilaisia aivojen suojausmenetelmiä. Aivojen suojausmenetelmäksi verenkiertopysähdyksen aikana otettiin hiljattain käyttöön selektiivinen antegradoituva aivoperfuusio kainalovaltimon kautta (kuva 1).
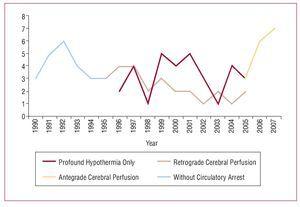
Kuva 1. Aivojen suojausmenetelmä verenkiertopysähdyksen aikana. Leikkausstrategian kehittyminen.
Toimenpide suoritettiin mediaani sternotomialla, reisivaltimon kanyloinnilla (82 %), kainalovaltimon kanyloinnilla (16 %) tai aortan kaaren kanyloinnilla (2 %), laskimopalautus oikean eteisen (85 %) tai reisilaskimon (15 %) kautta ja kardiopulmonaalinen ohitus. Ruumiinlämpöä seurattiin ruokatorven ja virtsarakon kautta, ja syvä hypotermia saavutettiin, kun virtsarakon lämpötila oli 18oC.
Aortan kiristyksen jälkeen nouseva aortta avattiin pitkittäissuunnassa ja suprakoronaarinen läpileikkaus suoritettiin mahdollisen intimarepeämän paikantamiseksi ja aorttaläpän morfologian ja toiminnan tutkimiseksi. Sitten nouseva aortta avattiin syvän hypotermian ja verenkiertopysähdyksen aikana ja koko aortan kaari tutkittiin. 27 prosentille potilaista lisättiin retrogradinen aivoperfuusio ylemmän laskimokäytävän kautta (200-300 ml/min). Niillä 16 potilaalla, joilla suoritettiin antegradatiivinen aivosuojaus, käytettiin oikeaa kainalovaltimoa (10-15 ml/kg/min), ja selektiivinen perfuusio suoritettiin vasemman kaulavaltimon kautta kaikilla potilailla.
Primäärinen repeämä tunnistettiin 83 potilaalla; se sijaitsi 14 %:lla potilaista aortan juuresta, 67 %:lla 67 %:lla nousevasta aortasta ja 19 %:lla 19 %:lla potilailla aortan kaaresta. Primaarisen repeämän vaurioittama aortan osa resekoitiin ja korvattiin Hemashield-dakronisiirteellä (Boston Scientific, Massachusetts, Yhdysvallat), joka anastomoitiin jatkuvalla 4/0-monofilamenttiompeleella, jota tuettiin heterologisella sydänpussin kaistaleella, ja proksimaalinen ja distaalinen natiiviaortta vahvistettiin gelatiini-resorsinssi-formaldehydillä (GRF, biologinen liima; Cardial Laboratories, Saint-Etienne, Ranska). Varhaisen kokemuksemme aikana aortan segmentin korvaaminen suoritettiin 21 potilaalle käyttäen inkluusiotekniikkaa (proteesiputken peittäminen resektoidulla natiivilla aortalla). Nykyisin käytetään graftinterpositiotekniikkaa (korvaaminen putkiproteesilla ja natiivin aortan täydellinen resektio).
Potilaista 61:llä (63 %) korvattiin vain nouseva aortta, 24:llä (24 %) se laajennettiin puolikaareen ja 13:lla (13 %) koko aortan kaareen. Puolikaarella tarkoitamme tapauksia, joissa kaari resekoitiin osittain ja tehtiin vain distaalinen anastomoosi ilman, että supra-aortan runkoa olisi tarvinnut istuttaa uudelleen. Norsunrunkoa käytettiin 6 potilaalla (kun aortan kaari korvataan kokonaan, proteesiputken vapaa segmentti jää distaaliseen anastomoosiin roikkumaan laskevaan rinta-aorttaan, mikä helpottaa mahdollisia toimenpiteitä tällä alueella). Aorttaläppä säästettiin resuspendoimalla kommissuurat uudelleen 4/0-monofilamenttisilla ompeleilla, joita tuettiin teflonlaastarilla 46 potilaalla (47 %), korvattiin 34 potilaalla (35 %) ja istutettiin uudelleen 1 potilaalla (1 %). Kun aorttaläppä jouduttiin vaihtamaan, 73 prosentilla potilaista se tehtiin käyttämällä läpänsiirrettä ja sepelvaltimoiden uudelleen istuttamista Bentall-tekniikalla. Aorttaläpän preoperatiivinen tila on kuvattu taulukossa 2. Leikkauksen jälkeen uusintaläpän tapauksessa läpän toimivuus todettiin intraoperatiivisen transesofageaalisen kaikukardiografian avulla 84 prosentilla potilaista, lievä regurgitaatio 13 prosentilla ja kohtalainen regurgitaatio (II/IV) lopuilla potilailla.

Kardiopulmonaalisen ohitusleikkauksen keskimääräinen kesto oli 183 (58) minuuttia, iskemia-aika 113 (39) minuuttia ja verenkiertopysähdysaika 3 (23) minuuttia.
Alkuperäisen käyttökokemuksen käsittävistä potilaista kaikkiaan 24 %:lla ei suoritettu verenkiertopysähdystä. Jäljelle jääneillä potilailla aivojen suojausmenetelmänä käytettiin syvää hypotermiaa vain 32 (33 %) potilaalla, retrogradista aivoperfuusiota lisättiin 26 (27 %) potilaalla ja antegradista perfuusiota lopuilla 16 (16 %) potilaalla.
Seuranta
Kaikille eloonjääneille potilaille tehtiin vuosittaiset kliiniset ja kaikukardiografiset tarkastukset sekä sarjatoimiset tietokonekerroskuvaus (TT), jossa arvioitiin distaalista aorttaa. Kliiniset tiedot saatiin haastattelemalla potilaita, perheenjäseniä ja perusterveydenhuollon lääkäreitä henkilökohtaisesti ja puhelimitse. Seurantaprosentti oli 95 % (79 potilasta).
Tilastollinen analyysi
Kaikissa analyyseissä käytettiin SPSS-tilasto-ohjelmaa (versio 14.0 for Windows). Perioperatiivisille muuttujille tehtiin univariaattinen analyysi tilastollisesti merkittävien riskitekijöiden määrittämiseksi (P
TULOKSET
Sairaalakuolleisuus
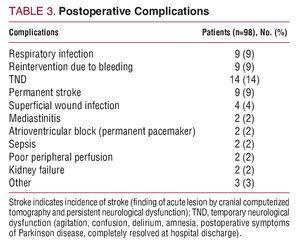
Sairaalakuolleisuus oli 15 % (15/98): 6 potilasta menehtyi intraoperatiivisen verenvuodon vuoksi, 3 potilasta alhaisen sydämen minuuttituoton vuoksi, 2 potilasta hermostovaurion vuoksi, 2 potilasta sepsiksen vuoksi ja 2 potilasta monielinelinten toiminnanvajauksen vuoksi leikkauksen jälkeen. Taulukossa 3 on esitetty postoperatiiviset komplikaatiot.
Yksittäisanalyysi osoitti, että korkea ikä, vasemman kammion toimintahäiriö, kardiogeeninen sokki, kardiopulmonaalinen ohitusleikkausaika >200 min, aortan kiinnitysaika >130 min ja postoperatiivinen aivohalvaus olivat sairaalakuolleisuuden vaaratekijöitä (taulukko 4). Näille muuttujille tehtiin monimuuttuja-analyysi, joka osoitti, että korkea ikä (≥70 vuotta) (RR=2,85; P=.04) ja preoperatiivinen kardiogeeninen sokki (RR=2,6; P=.025) todettiin sairaalakuolleisuuden riippumattomiksi ennustetekijöiksi.

Preoperatiivinen neurologinen toimintahäiriö ja ensimmäiset kokemusvuodet (1990-1994) olivat ainoat muuttujat, jotka olivat yhteydessä postoperatiivisiin neurologisiin komplikaatioihin (taulukko 4) yksimuuttuja-analyysissä, mutta nämä eivät saavuttaneet tilastollista merkitsevyyttä monimuuttuja-analyysissä.
Kuolleisuus ja erityiset postoperatiiviset neurologiset komplikaatiot (pysyvä aivohalvaus ja tilapäinen neurologinen toimintahäiriö ) mitattiin niistä potilaista, joille tehtiin verenkiertopysähdys, ja niistä potilaista, joille ei tehty verenkiertopysähdystä, ja ne stratifioitiin käytetyn aivojen suojausmenetelmän (syvä hypotermia yksinään tai yhdistettynä retrogradiseen tai antegradaariseen perfuusioon) mukaan (taulukko 5). Tilastollisesti merkitseviä eroja ei havaittu minkään välillä.

Seuranta
Seurantaprosentti oli 95 % (79 potilasta), mediaani 61 (vaihteluväli 1-204) kuukautta. Sairaalasta kotiutumisen jälkeen kaikille potilaille tehtiin kaikukardiografinen tutkimus 2 kuukauden kuluttua ja sen jälkeen vuosittain. Yhteensä 67 prosentille (56/83) potilaista tehtiin vähintään yksi tietokonetomografiatutkimus. Niistä 27 eloonjääneestä potilaasta, joille ei tehty tietokonetomografiaa, 17 kieltäytyi tutkimuksesta tai ei osallistunut siihen, 4 hävisi tutkimuksesta ja 6 kuoli seurannan aikana, joista 1 johtui tunnetusta aortan syystä (vatsa-aortan aneurysman repeämä).
Tietokonetomografia osoitti distaalisessa aortassa pysyvän avoimen väärän luumenin 71 %:lla potilaista, joista 17 %:lla esiintyi rinta- ja vatsa-aortan etenevää laajentumaa.
Uusintatoimenpiteet
Kokonaisuudessaan 13 (16 %) potilaalle tehtiin uusintatoimenpide seurannan aikana. Syyt olivat seuraavat: vakava aortan regurgitaatio ja aortan juuren laajentuma viidellä potilaalla, vakava aortan regurgitaatio ja aortan juuren redissektio kolmella potilaalla, vakava aortan regurgitaatio yksinään yhdellä potilaalla, vakava aortan ja mitraaliläpän regurgitaatio yhdellä potilaalla, mitraali- ja aorttaläpän endokardiitti yhdellä potilaalla, aortan ja aorttaläpän välinen pseudoaneurysma yhdellä potilaalla ja aortan juuren ja oikean eteisen välille muodostunut fisteli yhdellä. Yhdellekään potilaalle ei tehty uutta toimenpidettä laskevan aortan sairauden vuoksi. Käytetyt kirurgiset toimenpiteet esitetään taulukossa 6. Nonreintervention curve
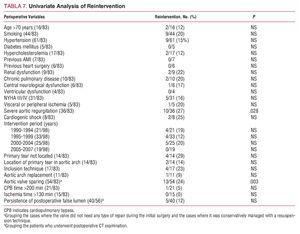
Long-Term Survival
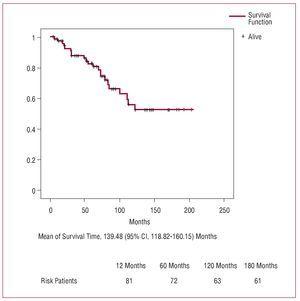
Kuva 3. Eloonjäämiskäyrä seurannan aikana (Kaplan-Meier).

Ykseismuuttuja-analyysi osoitti kuolleisuuden ennustetekijöiksi seurannan aikana vanhan iän (≥70 vuotta), sisäänottotekniikan, postoperatiivisen TND:n ja ei-antegraationaalisten aivosuojamenetelmien käytön (taulukko 9). Monimuuttuja-analyysissä ainoa tilastollisesti merkitsevä riippumaton kuolleisuuden ennustaja seurannan aikana oli se, että ei käytetty antegradaa aivojen suojausta (RR=3,1; P=,02).

KESKUSTELU
Akuutti A-tyypin aortan dissektio on kriittinen tilanne, joka vaatii useimmissa tapauksissa välitöntä kliinistä reagointia ja kirurgista hätätoimenpidettä.
Siegal ym.18 arvioivat, että hoitamattomilla potilailla kuolleisuusriski lisääntyy 1 %:lla tunneittain ensimmäisten 48 tunnin aikana ja saavuttaa 70 %:n asteen tason viikon kuluttua. International Registry of Acute Aortic Syndrome (IRAD)1 -rekisterin tietojen mukaan konservatiivisesti hoidettujen potilaiden kuolleisuus on 58 %, kun taas kirurgisen hoidon kokonaiskuolleisuus on 24 %.
Vaikka diagnostisissa ja kirurgisissa tekniikoissa sekä postoperatiivisessa hoidossa on viime vuosina tapahtunut suurta edistystä, sairaalakuolleisuudessa on huomattavaa vaihtelua, ja se vaihtelee 15-30 %:n välillä.2,3,19-21 Kokemuksessamme sairaalakuolleisuus oli 15 %, mikä vastaa nykyisten sarjojen parhaita tuloksia.4,22
Sairaalakuolleisuuden ennustetekijät vastaavat useimpien julkaistujen sarjojen ennustetekijöitä.2-4,21 IRAD:n tietojen1 mukaan kuolleisuuden riippumattomat muuttujat ovat korkea ikä, hypotensio/shokki, aiempi sydänsairaus ja preoperatiivinen munuais-, suoliliepeen tai sydänlihaksen iskemia. Nämä tulokset osoittavat, että sairaalakuolleisuus liittyy yleensä potilaiden leikkausta edeltäviin kliinisiin ominaisuuksiin, joita on vaikea muuttaa. Rampoldi ja muut1 ovat osoittaneet, että epävakaiden potilaiden leikkauskuolleisuus on vähintään kaksinkertainen vakaisiin potilaisiin verrattuna (31,4 % vs. 16,7 %). Nämä havainnot osoittavat preoperatiivisen hemodynaamisen vakauden merkityksen ja korostavat hätäleikkauksen tarvetta ennen hemodynaamisen tilan heikkenemistä.
Sarjassamme ainoat riippumattomat sairaalakuolleisuutta ennustavat tekijät olivat korkea ikä (≥70 vuotta) ja preoperatiivinen kardiogeeninen sokki.
Kirurgisen resektion laajuutta ei tunnistettu sairaalakuolleisuuden riippumattomaksi riskitekijäksi; laajemmat resektiot, joihin liittyi myös aortankaaren korvaaminen, eivät vaikuttaneet varhais- tai myöhäisvaiheen tuloksiin. Toiset kirjoittajat ovat toisaalta ehdottaneet yksinomaan nousevan aortan resektiota ja väittäneet, että laajempiin resektioihin liittyvä riski on suurempi kuin mahdollinen hyöty ja että leikkauksen päätavoite on potilaan selviytyminen.5
Neurologisen vamman syy aortan dissekaatioleikkauksen aikana on monitekijäinen, ja se voi johtaa pitkittyneeseen verenkiertopysähdykseen, emboliatapahtumiin ja huonoon aivoperfuusioon, joka johtuu siitä, että virtaus tapahtuu mieluummin väärän luumenin kautta.
Postoperatiiviset neurologiset komplikaatiot ovat yleinen sairastuvuuden ja kuolleisuuden syy aortan dissekaatioleikkauksen yhteydessä, ja niiden esiintyvyys on arviolta 10 %:a-20 %:a.3,5,7,8
Ergin ym.9 ja Hagl ym.10 huomauttavat, että postoperatiivinen aivohalvaus aiheuttaa pääasiassa embolisia tapahtumia mahdollisessa yhteydessä reisivaltimosta tapahtuvaan retrogradiseen perfuusioon, mutta ei suoraan käytettyyn aivosuojamenetelmään, kun taas TND liittyisi riittämättömään aivosuojaukseen. Antegradinen aivoperfuusio on yhdistetty TND:n merkittävään vähenemiseen viimeaikaisissa sarjoissa10,11,23,24 , vaikka sen merkitys aivohalvauksen vähentämisessä ei ole yhtä selvä.
Antegradinen aivoperfuusio on muuttanut verenkiertopysähdyksen käsitettä näillä potilailla, koska tarkalleen ottaen täydellistä verenkiertopysähdystä ei suoriteta, kun otetaan huomioon, että jatkuvaa aivoperfuusiota ylläpidetään 500 mL/min:n ja 1 000 mL/min välillä. Lisäksi useat kirjoittajat ovat ehdottaneet, että kohtalainen hypotermia (25oC) riittäisi suojaamaan aivoja ja välttämään syvän hypotermian haitalliset vaikutukset.17,25,26 Ryhmämme käytti kuitenkin syvää hypotermiaa, koska nämä korjaukset ovat monimutkaisia, niiden odotetaan kestävän pitkään ja koska tämä jäähdytysmenetelmä on osoittautunut erittäin tehokkaaksi suojaamaan aivoja ja muita elimiä.17,27,28
Aksillaarivaltimon kanylointi femoraalisen sijaan vähentää huonon viskeraalisen ja aivoperfuusion riskiä, trombien remobilisoitumista vatsa- ja rinta-aortasta kohti aivoja ja lisäksi ohjaa virtauksen uudelleen todelliseen luumeniin, vähentää liiallisen paineen muodostumisen mahdollisuutta aortan puristamisen yhteydessä ja helpottaa antegradan distaalisen perfuusion palauttamista.12-16. Kaikki nämä edut näyttävät osoittavan, että antegradoituva aivoperfuusio kainalovaltimon kautta, paitsi jos valtimo on vaikean ateroskleroosin vaurioittama, on ensisijainen menetelmä aivojen suojaamiseksi.10,11,17 .
Sarjassamme antegradinen aivoperfuusio kainalovaltimoa käyttäen vähensi TND:n esiintyvyyden 6 prosenttiin ja sairaalakuolleisuuden 6 prosenttiin 16:lla viimeisimmällä potilaalla, joille tehtiin leikkaus, mikä viittaa, mutta ei osoita, että se suojaa neurologisilta komplikaatioilta ja niihin liittyvältä sairastuvuudelta ja kuolleisuudelta. Mahdollisesti tämä tilastollisen merkitsevyyden puute johtuu siitä, että kainalovaltimon kautta tapahtuvaa antegrada-perfuusiota käyttävien toimenpiteiden määrä oli pieni. Kun otetaan huomioon tämän toimenpiteen harvinaisuus (
Kymmenen vuoden kuluttua 73,3 %:lle potilaista ei ollut tehty uutta toimenpidettä, ja tämä tulos on samankaltainen kuin julkaistut tulokset.3,4,6,29,30. Aorttaläppä säästettiin aina, kun se oli mahdollista, ja vain silloin, kun kyseessä oli läpän rappeuma, annuloaortan ektasia tai aiempi sydänläppävika, päätettiin suorittaa läpän vaihto yksinään tai yhdessä aortan juuren vaihdon kanssa (Bentall-tekniikka), toimenpide, joka ei muuttanut sairaalakuolleisuutta.
Sarjassamme 77 %:lla uusintatoimenpiteen suorittaneista potilaista (13/78) tämä oli tarpeen vaikean aorttaläpän regurgitaation vuoksi, joka oli esiintynyt jo aiemmin ja jota oli hoidettu konservatiivisesti läpän uusintatutkimuksella alkuperäisen toimenpiteen aikana. Preoperatiivinen akuutti aortan regurgitaatio ja aorttaläpän säästäminen olivat juuri ne tekijät, jotka määrittivät aortan myöhäisen uusintatoimenpiteen, ja tämä oikeuttaisi aorttaläpän aggressiivisen hoidon alkuperäisen toimenpiteen aikana.6,29 Hagl ja muut31 suosittelivat juuren ja aorttaläpän systemaattista korvaamista (Bentall-tekniikka). Toisaalta Estrera ja muut32 raportoivat hyväksyttävästä kestävyydestä aorttaläpän säästämisen jälkeen; he huomauttivat, että mahdollisen uusintatoimenpiteen ei pitäisi sanella alkuperäistä toimenpidettä, ja suosittelivat aorttaläpän säästämistä kroonisen antikoagulanttihoidon välttämiseksi ja sen mahdollisen roolin välttämiseksi väärän luumenin tromboosin puuttuessa33.
Me katsomme, että vaikean aorttaläpän regurgitaation alkuesiintymä määrittää sellaisen dissekaation suuremman vaikeusasteen, jonka alkuperä tai laajuus ulottuu aortan juureen, ja näin ollen aggressiivisen hoidon, jossa aortan juuri ja läppä resekoidaan ja siihen istutetaan läppäsiirrännäinen (Bentall-tekniikka), pitäisi olla valintamenetelmä.4,6,29,31 Näissä tapauksissa läpän resuspensio säästämällä aortan juuresta jättää jälkeensä luonnostaan sairastuneen segmentin, joka aiheuttaa suuremman riskin uusintaläpän repeytymiselle ja myöhemmille komplikaatioille. Aortan juuren korvaustekniikasta, johon liittyy aorttaläpän uudelleen istuttaminen (Davidin tekniikka), julkaistut tulokset ovat lupaavia, ja vaikka pitkän aikavälin arviointia tarvitaankin, siitä voi tulla mielenkiintoinen vaihtoehto33,34 .
Sairaalasta kotiutumisen jälkeen eloonjääneistä 56 potilaasta, joille tehtiin seurannan aikana tietokonetomografia, vain kuudella (11 %) potilaalla (6 potilaasta) oli havaittavissa etenevä laajentuma aortan muilla alueilla, mikä merkitsi leikkausindikaatiota: kahdella potilaalla oli vatsa-aortan aneurysma, kahdella torako-abdominaalinen aneurysma ja kahdella laskevan rinta-aortan aneurysma. Näistä potilaista 2 kieltäytyi uusintatoimenpiteestä, ja muilla oli jokin liitännäissairaus (korkea ikä, vakava neurologinen vajaatoiminta jne.), joka teki toimenpiteen mahdottomaksi.
Tällainen distaalisen aortan uusintatoimenpiteiden alhainen osuus johtuu todennäköisesti toimenpiteen aikana havaittujen primaaristen intimarepeämien suuresta prosenttimäärästä ja päätöksestämme resektioida se kaikissa tapauksissa. Itse asiassa niistä 15 potilaasta, joilla intimarepeämää ei löydetty, 60 prosenttia (9 potilasta) kuului ryhmään, jolle ei tehty verenkiertopysähdystä (joka estää aortan kaaren tutkimisen ja sulkee pois intimarepeämät kyseisellä tasolla) ja jossa uusintatoimenpiteen riski oli suurentunut lähelle tilastollisen merkitsevyyden rajaa (P=.06). Näin ollen useat kirjoittajat kuvaavat, että intimarepeämän poistamatta jättäminen alkuperäisen leikkauksen aikana on tärkein tekijä, joka vaikuttaa rinta- tai vatsa-aortan laajentamisen myöhäiseen uusintatoimenpiteeseen6,30 .
Vaikka ryhmällämme ei ole kokemusta tästä, jotkut kirjoittajat huomauttavat, että tietyissä tapauksissa stentin istuttaminen laskevaan rinta-aorttaan alkuperäisen tai toisen toimenpiteen yhteydessä voisi parantaa tuloksia vähentämällä uusintatoimenpiteiden esiintyvyyttä ja taudin etenemisestä distaaliseen aorttaan johtuvien komplikaatioiden puhkeamista35,36.
Sairaalasta kotiutumisen jälkeinen aktuaarinen eloonjäämiskäyrä osoittaa joitakin prosenttilukuja, jotka ovat vertailukelpoisia muiden kirjoittajien kuvaamien prosenttilukujen kanssa.2,3,5,6 Vanhuus on useimmissa sarjoissa yksi seurannan aikaiseen kuolleisuuteen vaikuttavista riippumattomista riskitekijöistä, mikä johtuu osittain tämän potilasryhmän matalasta elinaikakertymästä.2 Pitkän aikavälin eloonjäämiskäyttäytymisen riippumattomien ennustetekijöiden määrittelyssä on yleisesti ottaen suurta vaihtelua. Chiappini ja muut2 kuvasivat 487 potilasta käsittävän sarjan, jossa tehtiin leikkaus tyypin A aortan dissekaation vuoksi, ja totesivat, että ainoa riskitekijä oli leikkausta edeltävä diabetes. Erwin ja muut3 havaitsivat 315 potilaan ryhmässä pitkälle edenneen iän ja postoperatiivisen dialyysin kuolleisuutta ennustaviksi tekijöiksi seurannan aikana.
Sarjassamme havaitsimme, että antegradaattisen aivosuojauksen käyttämättä jättäminen oli myöhäiskuolleisuuden ennustaja, mikä osoittaa, että vaikka antegradaattisella perfuusiolla ei ollut merkittävää vaikutusta alkuperäisiin postoperatiivisiin tuloksiin, sillä on kuitenkin suuri merkitys myöhäisen eloonjäämisen kannalta.
Erginin ja muiden tutkijoiden tutkimukset9 yhdistivät postoperatiivisen trombosyyttihäiriön (TND:n) ja pitkäkestoisen aivotoiminnan heikkenemisen. Pompilio ym.37 arvioivat perioperatiivisten neurologisten tapahtumien vaikutusta myöhäiskuolleisuuteen, eli potilailla, jotka selvisivät sairaalajaksolta neurologisen vamman vuoksi, oli huonompi pitkäaikainen eloonjäämisaste. Tämä seikka saattaa selittyä keuhkoputkentulehduksen, uusien neurologisten tapahtumien ja muiden komplikaatioiden suurella riskillä, joka liittyy näiden potilaiden alentuneeseen toimintakykyyn.4
Rajoitukset
Tälle artikkelille ominaisia ovat kaikki ne rajoitukset, jotka liittyvät retrospektiivisiin ei-satunnaistettuihin tutkimuksiin. Taudin vähäinen esiintyvyys tarkoittaa, että vain harvoille potilaille tehtiin interventio, mikä rajoittaa tulosten tilastollista voimaa.
Koska tämä katsaus kattaa pitkän ajanjakson, ensimmäiset potilaat, joita hoidettiin ilman aivoverenkierron pysäyttämistä, ja myöhemmät potilaat, joita hoidettiin antegradisella aivoperfuusio-menetelmällä, eivät olleet ajan tasalla muiden mainittujen aivojen suojausmenetelmien kanssa. Viimeksi mainittua menetelmää (antegrada aivoperfuusio) sovellettiin pieneen otoskokoon (16 potilasta), mikä rajoittaa tulosten tilastollista merkitsevyyttä.
YHTEENVETO
Akuutin aortan dissekaation leikkauksella saadaan hyväksyttäviä lyhyt- ja pitkäaikaistuloksia, ja useimmilla potilailla hätätoimenpide pitäisi olla aiheellinen.
Vaikeaan aortan regurgitaatioon liittyy suuri varhaisen uusintatoimenpiteen riski, ja tämä oikeuttaisi aorttaläpän aggressiivisen hoidon alkuperäisen leikkauksen aikana.
Antegradoituva aivoperfuusio on muuttanut verenkiertopysähdyksen käsitettä ja parantanut pitkäaikaisennustetta näillä potilailla. Katsomme, että vaikka tarvitaan kokemuksia laajemmista sarjoista, antegradan aivoperfuusion käyttö akuutissa aortan dissektioleikkauksessa voisi parantaa näiden potilaiden ennustetta.
LUETTELOT
CT: tietokonetomografia
TND: tilapäinen neurologinen toimintahäiriö