INTRODUCTION
Malgré les progrès des techniques diagnostiques et chirurgicales et des soins postopératoires, la dissection aortique aiguë de type A continue d’être associée à une morbidité et une mortalité élevées à court et à long terme. La mortalité hospitalière actuelle a été estimée entre 15 % et 35 %, avec un taux de survie à 5 ans de 65 % à 75 %.1-7
La forte incidence d’accident vasculaire cérébral postopératoire chez ces patients (10 % à 20 %)3,5,7,8 a été associée à une protection cérébrale inadéquate pendant l’arrêt circulatoire, à des événements emboliques ou à une malperfusion due à un flux préférentiel à travers la fausse lumière pendant la perfusion utilisant l’artère fémorale.9,10 Ces dernières années, l’introduction de nouvelles techniques de protection cérébrale, telles que la perfusion cérébrale antégrade sélective et la canulation de l’artère axillaire, a considérablement réduit l’incidence de cette complication10-17.
Le but de cette étude rétrospective est de décrire notre expérience en matière de chirurgie de dissection aortique aiguë de type A – en relation avec la mortalité hospitalière, l’incidence de réintervention et la survie à long terme – et d’analyser l’influence de la protection cérébrale sur nos résultats.
Méthodes
Entre mars 1990 et octobre 2007, 98 patients consécutifs (79 hommes et 19 femmes) ont subi une chirurgie dans notre hôpital pour une dissection aortique aiguë de type A. Parmi les patients diagnostiqués et orientés vers la chirurgie (103) durant cette période, 5 ont été exclus ; 2 patients en raison de leur âge supérieur à 85 ans et les autres en raison de la présentation de lésions cérébrales ou viscérales irréversibles.
L’âge médian était de 59 ans. Le symptôme le plus fréquent à la présentation était une douleur thoracique aiguë. Le diagnostic a été confirmé par une aortographie au cours de la période initiale (18%), une échocardiographie transthoracique (76%), une échocardiographie transoesophagienne (66%) et une tomographie informatisée (CT) thoraco-abdominale (65%). À l’exception de 11 patients, pour lesquels un seul test de diagnostic a été effectué, tous les patients ont été diagnostiqués en utilisant 2 ou 3 de ces techniques d’imagerie en combinaison (actuellement, le système de diagnostic employé est la tomographie thoraco-abdominale avec ou sans échocardiographie transthoracique et l’échocardiographie transœsophagienne peropératoire).
Un total de 91 (93%) patients ont été opérés en urgence (dans les 24 h) et les autres ont été opérés en urgence (dans les 72 h suivant le diagnostic).
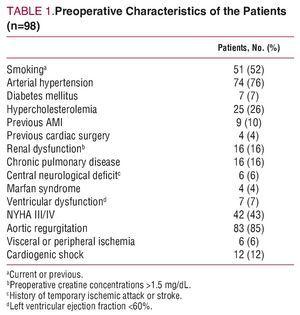
Les examens d’imagerie ont démontré une régurgitation aortique chez 83 patients (55% avec une régurgitation sévère). Les caractéristiques cliniques et démographiques préopératoires sont présentées dans le tableau 1.
Technique chirurgicale
Les concepts de base de la procédure chirurgicale impliquent le remplacement de l’aorte ascendante ou de la crosse aortique, la résection de la déchirure primaire et la préparation de l’anastomose distale pendant l’arrêt circulatoire. Au cours de cette période de 18 ans, la stratégie chirurgicale employée pour cette pathologie a progressivement évolué. Initialement, seule l’aorte ascendante était réséquée avec un clampage aortique sans arrêt circulatoire. En 1994, on a introduit l’anastomose distale avec arrêt circulatoire, qui est la technique actuellement utilisée chez tous les patients, tout en appliquant différentes méthodes de protection cérébrale. La perfusion cérébrale antégrade sélective via l’artère axillaire a été récemment introduite comme méthode de protection cérébrale pendant l’arrêt circulatoire (figure 1).
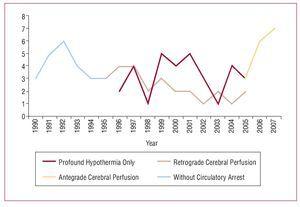
Figure 1. Évolution de la stratégie chirurgicale.
Elle a été réalisée par sternotomie médiane, canulation de l’artère fémorale (82%), canulation de l’artère axillaire (16%) ou canulation de l’arc aortique (2%), avec retour veineux par l’oreillette droite (85%) ou la veine fémorale (15%) et pontage cardio-pulmonaire. La température corporelle a été surveillée par l’œsophage et la vessie, et l’hypothermie profonde a été atteinte lorsque la température de la vessie a atteint 18oC.
Après clampage aortique, l’aorte ascendante a été ouverte longitudinalement et une transection supracoronaire a été réalisée pour localiser la déchirure intimale, le cas échéant, et pour examiner la morphologie et le fonctionnement de la valve aortique. Ensuite, en hypothermie profonde et en arrêt circulatoire, l’aorte ascendante a été débridée et la totalité de la crosse aortique examinée. Chez 27 % des patients, une perfusion cérébrale rétrograde a été ajoutée via la veine cave supérieure (200-300 ml/min). Chez les 16 patients où une protection cérébrale antérograde a été réalisée, l’artère axillaire droite a été utilisée (10-15 mL/kg/min), et une perfusion sélective a été réalisée via l’artère carotide gauche chez tous les patients.
La déchirure primaire a été identifiée chez 83 patients ; elle était située dans la racine aortique chez 14%, l’aorte ascendante chez 67%, et la crosse aortique chez 19% des patients. Le segment aortique affecté par la déchirure primaire a été réséqué et remplacé par un greffon en dacron Hemashield (Boston Scientific, Massachusetts, États-Unis) anastomisé avec une suture continue monofilament 4/0 soutenue par une bande péricardique hétérologue et renforçant l’aorte native proximale et distale avec de la gélatine-résorcine-formaldéhyde (GRF, colle biologique ; Laboratoires Cardial, Saint-Étienne, France). Au cours de notre première expérience, le remplacement du segment aortique a été réalisé en utilisant la technique d’inclusion (recouvrement du tube prothétique par l’aorte native réséquée) chez 21 patients. Actuellement, la technique d’interposition du greffon est utilisée (remplacement par une prothèse tubulaire avec résection complète de l’aorte native).
Le remplacement de l’aorte ascendante uniquement a été réalisé chez 61 (63%) patients, étendu à l’hémiarque chez 24 (24%), et à l’arc aortique total chez 13 (13%). Par hémiarque, nous faisons référence aux cas de résection partielle de la crosse, avec une anastomose distale uniquement, sans nécessité de réimplantation du tronc supra-aortique. Une trompe d’éléphant a été utilisée chez 6 patients (lors du remplacement total de la crosse aortique, un segment libre du tube prothétique reste dans l’anastomose distale suspendu dans l’aorte thoracique descendante, ce qui facilite les interventions potentielles dans cette zone). La valve aortique a été épargnée en resuspendant les commissures avec des sutures monofilament 4/0 soutenues par un patch en téflon chez 46 patients (47%), remplacée chez 34 (35%) et réimplantée chez 1 (1%). Lorsque la valve aortique devait être remplacée, dans 73% des cas, cela a été fait en utilisant un greffon valvulaire avec réimplantation des artères coronaires selon la technique de Bentall. L’état préopératoire de la valve aortique est décrit dans le tableau 2. Après la chirurgie, en cas de remise en suspension, la compétence valvulaire a été objectivée par échocardiographie transœsophagienne peropératoire chez 84 % des patients, une régurgitation légère chez 13 % d’entre eux et une régurgitation modérée (II/IV) chez les autres patients.

La durée moyenne du pontage cardio-pulmonaire était de 183 (58) min, la durée de l’ischémie, de 113 (39) min, et la durée de l’arrêt circulatoire, de 3 (23) min.
Un total de 24% des patients, comprenant l’expérience initiale, n’ont pas subi d’arrêt circulatoire. Chez les autres patients, la méthode de protection cérébrale utilisée était une hypothermie profonde chez seulement 32 (33%) patients, une perfusion cérébrale rétrograde a été ajoutée chez 26 (27%) patients, et une perfusion antégrade chez les 16 (16%) autres.
Suivi
Tous les patients survivants ont subi des contrôles cliniques et échocardiographiques annuels, ainsi que des examens CT en série pour évaluer l’aorte distale. Les données cliniques ont été obtenues par des entretiens personnels et téléphoniques avec les patients, les membres de la famille et les médecins de soins primaires. Un taux de suivi de 95% a été atteint (79 patients).
Analyse statistique
Le programme statistique SPSS (version 14.0 pour Windows) a été utilisé dans toutes les analyses. Une analyse univariée a été réalisée sur les variables périopératoires afin de déterminer les facteurs de risque statistiquement significatifs (P
RESULTATS
Mortalité hospitalière
La mortalité hospitalière était de 15% (15/98) : 6 patients sont décédés en raison d’une hémorragie peropératoire ; 3, d’un faible débit cardiaque ; 2, d’une atteinte neurologique ; 2, d’un sepsis ; et 2 en raison d’une défaillance multi-organique postopératoire. Le tableau 3 montre les complications postopératoires.
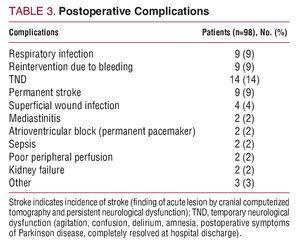
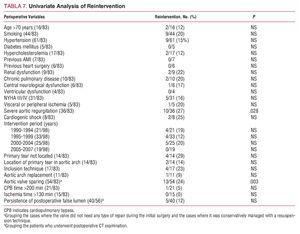
L’analyse univariée a montré que l’âge avancé, la dysfonction ventriculaire gauche, le choc cardiogénique, le temps de pontage cardio-pulmonaire >200 min, le temps de clampage aortique >130 min et l’accident vasculaire cérébral postopératoire étaient des facteurs de risque de mortalité hospitalière (tableau 4). Ces variables ont fait l’objet d’une analyse multivariée qui a montré que l’âge avancé (≥70 ans) (RR=2,85 ; P=0,04) et le choc cardiogénique préopératoire (RR=2,6 ; P=0,025) ont été identifiés comme des prédicteurs indépendants de la mortalité hospitalière.

La dysfonction neurologique préopératoire et les premières années d’expérience (1990-1994) étaient les seules variables associées aux complications neurologiques postopératoires (tableau 4) dans l’analyse univariée, mais elles n’ont pas atteint la signification statistique dans l’analyse multivariée.
La mortalité et les complications neurologiques postopératoires spécifiques (accident vasculaire cérébral permanent et dysfonctionnement neurologique temporaire ) ont été mesurées parmi les patients qui ont subi un arrêt circulatoire et ceux qui n’en ont pas subi et ont été stratifiés selon la méthode de protection cérébrale utilisée (hypothermie profonde seule ou en combinaison avec une perfusion rétrograde ou antégrade) (tableau 5). Aucune différence statistiquement significative n’a été constatée entre les uns et les autres.

Suivi
Un taux de suivi de 95 % (79 patients) a été atteint, avec une médiane de 61 (intervalle, 1-204) mois. Après la sortie de l’hôpital, tous les patients ont subi un examen échocardiographique à 2 mois et ensuite annuellement. Au total, 67 % (56/83) des patients ont subi au moins un examen tomodensitométrique. Parmi les 27 patients survivants qui n’ont pas subi de CT, 17 ont refusé l’examen ou ne se sont pas présentés, 4 ont été perdus de vue et 6 sont décédés pendant le suivi, dont 1 d’une cause aortique connue (rupture d’anévrisme de l’aorte abdominale).
La tomographie assistée par ordinateur a montré la persistance d’une fausse lumière perméable dans l’aorte distale chez 71% des patients, dont 17% ont présenté une dilatation progressive de l’aorte thoracique et de l’aorte abdominale.
Réintervention
Au total, 13 (16%) patients ont subi une réintervention au cours du suivi. Les causes étaient les suivantes : régurgitation aortique sévère et dilatation de la racine aortique chez 5 patients, régurgitation aortique sévère et redissection de la racine aortique chez 3, régurgitation aortique sévère seule chez 1, régurgitation aortique et mitrale sévère chez 1, endocardite des valves mitrale et aortique chez 1, pseudo-anévrisme aorto-trachéal chez 1, et fistule entre la racine aortique et l’oreillette droite chez 1. Aucun patient n’a subi de réintervention pour une maladie de l’aorte descendante. Les procédures chirurgicales appliquées sont présentées dans le tableau 6. La mortalité hospitalière était de 23% (3/13), 2 patients sont décédés en raison d’une hémorragie peropératoire et 1 en raison d’un faible débit cardiaque.
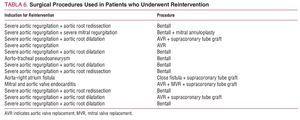
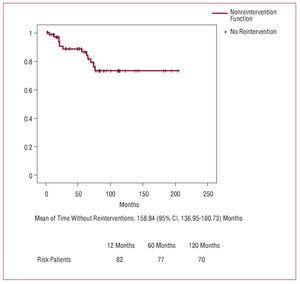
Figure 2. Courbe de non-réintervention
Survie à long terme
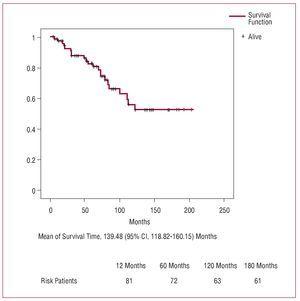
Figure 3. Courbe de survie pendant le suivi (Kaplan-Meier).

L’analyse univariée a montré l’âge avancé (≥70 ans), la technique d’inclusion, le TND postopératoire et l’application de méthodes de protection cérébrale non antégrade (tableau 9) comme prédicteurs de la mortalité pendant le suivi. Dans l’analyse multivariée, le seul facteur prédictif indépendant statistiquement significatif de mortalité au cours du suivi était la non-utilisation d’une protection cérébrale antégrade (RR=3,1 ; P=0,02).

DISCUSSION
La dissection aortique aiguë de type A est une situation critique qui nécessite une réponse clinique immédiate et une intervention chirurgicale d’urgence dans la plupart des cas.
Siegal et al18 ont estimé que, chez les patients non traités, le risque de mortalité augmente de 1% toutes les heures pendant les 48 premières heures et atteint 70% après une semaine. Selon les données de l’International Registry of Acute Aortic Syndrome (IRAD),1 la mortalité chez les patients traités de manière conservatrice est de 58% contre une mortalité chirurgicale totale de 24%.
Bien que ces dernières années de grands progrès aient été réalisés dans les techniques diagnostiques et chirurgicales et dans les soins postopératoires, il existe une variabilité considérable dans la mortalité hospitalière, allant de 15 à 30%.2,3,19-21 Dans notre expérience, la mortalité hospitalière était de 15%, similaire aux meilleurs résultats des séries actuelles.4,22
Les prédicteurs de la mortalité hospitalière coïncident avec ceux de la plupart des séries publiées.2-4,21 Selon les données de l’IRAD,1 les variables indépendantes de la mortalité sont l’âge avancé, l’hypotension/le choc, les antécédents cardiaques et l’ischémie rénale, mésentérique ou myocardique préopératoire. Ces résultats montrent que la mortalité hospitalière est généralement associée aux caractéristiques cliniques préopératoires des patients et qu’il est difficile de les modifier. Rampoldi et al1 ont montré que les patients instables ont un taux de mortalité chirurgicale qui est au moins le double de celui des patients stables (31,4% vs 16,7%). Ces résultats révèlent l’importance de la stabilité hémodynamique préopératoire et soulignent la nécessité d’une chirurgie d’urgence avant le début de la détérioration hémodynamique.
Dans notre série, les seuls facteurs prédictifs indépendants de mortalité hospitalière étaient l’âge avancé (≥70 ans) et le choc cardiogénique préopératoire.
L’étendue de la résection chirurgicale n’a pas été identifiée comme un facteur de risque indépendant de mortalité hospitalière ; les résections plus étendues avec remplacement de la crosse aortique n’ont pas affecté les résultats précoces ou tardifs. D’autres auteurs, en revanche, ont proposé la résection exclusive de l’aorte ascendante, arguant que le risque lié aux résections plus étendues l’emporte sur le bénéfice potentiel et que l’objectif principal de la chirurgie est la survie du patient5.
La cause des lésions neurologiques au cours de la chirurgie de la dissection aortique est multifactorielle et peut entraîner un arrêt circulatoire prolongé, des événements emboliques et une mauvaise perfusion cérébrale en raison du flux préférentiel à travers la fausse lumière.
Les complications neurologiques postopératoires sont une cause fréquente de morbidité et de mortalité dans la chirurgie de la dissection aortique, avec une incidence estimée à 10 %-20 %.3,5,7,8
Ergin et al9 et Hagl et al10 soulignent que l’accident vasculaire cérébral postopératoire est principalement dû à des événements emboliques dans une association possible avec la perfusion rétrograde de l’artère fémorale, mais pas directement avec la méthode de protection cérébrale utilisée, alors que le TND serait associé à une protection cérébrale inadéquate. La perfusion cérébrale antégrade a été associée à une réduction significative du TND dans des séries récentes,10,11,23,24 bien que son rôle soit moins clair en ce qui concerne la réduction de l’AVC.
La perfusion cérébrale antégrade a modifié le concept d’arrêt circulatoire chez ces patients car, à proprement parler, l’arrêt circulatoire total n’est pas effectué, étant donné que la perfusion cérébrale continue est maintenue entre 500 ml/min et 1000 ml/min. De plus, plusieurs auteurs ont proposé qu’une hypothermie modérée (25oC) serait suffisante pour protéger le cerveau et éviter les effets néfastes d’une hypothermie profonde.17,25,26 Cependant, notre groupe a appliqué une hypothermie profonde car ces réparations sont complexes, prévues pour être de longue durée, et parce que cette méthode de refroidissement s’est avérée très efficace pour protéger le cerveau ainsi que les autres organes17,27,28.
La canulation de l’artère axillaire, au lieu de l’artère fémorale, réduit le risque de mauvaise perfusion viscérale et cérébrale, de remobilisation des thrombus de l’aorte abdominale et thoracique vers le cerveau et, en outre, redirige le flux vers la vraie lumière, diminue le risque d’accumulation de pression excessive lors du clampage de l’aorte et facilite le rétablissement d’une perfusion distale antégrade12-16. Tous ces avantages semblent indiquer que la perfusion cérébrale antégrade par l’artère axillaire, sauf lorsque celle-ci est affectée par une athérosclérose sévère, est la méthode de choix pour la protection cérébrale.10,11,17
Dans notre série, la perfusion cérébrale antégrade par l’artère axillaire a réduit l’incidence du TND à 6% et la mortalité hospitalière à 6% chez les 16 derniers patients opérés, suggérant, mais ne démontrant pas, son rôle dans la protection contre les complications neurologiques et leur morbidité et mortalité concomitantes. Il est possible que ce manque de signification statistique soit dû au faible nombre d’interventions utilisant une perfusion antégrade via l’artère axillaire. Étant donné la rareté de cette intervention (
A 10 ans, 73,3 % des patients n’avaient pas subi de réintervention et ce résultat est similaire à ceux publiés.3,4,6,29,30 La valve aortique a été épargnée dans la mesure du possible et ce n’est qu’en cas de dégénérescence valvulaire, d’ectasie annulo-aortique ou d’antécédents de cardiopathie valvulaire qu’il a été décidé de procéder à un remplacement valvulaire seul ou avec un remplacement de la racine aortique (technique de Bentall), une procédure qui n’a pas modifié la mortalité hospitalière.
Dans notre série, 77% des patients qui ont subi une réintervention (13/78) l’ont exigée en raison d’une régurgitation aortique sévère qui avait déjà été présentée et traitée de manière conservatrice par une resuspension de la valve lors de l’intervention initiale. La régurgitation aortique aiguë préopératoire et l’épargne de la valve aortique étaient précisément les facteurs déterminant la réintervention aortique tardive, ce qui justifierait une gestion agressive de la valve aortique lors de l’intervention initiale.6,29 Hagl et al31 ont recommandé le remplacement systématique de la racine et de la valve aortique (technique de Bentall). D’autre part, Estrera et al32 ont rapporté un niveau acceptable de durabilité après avoir épargné la valve aortique ; ils ont souligné qu’une éventuelle réintervention ne devrait pas dicter la procédure initiale et ont recommandé d’épargner la valve aortique pour éviter un traitement anticoagulant chronique et son rôle possible dans l’absence de thrombose de la fausse lumière33.
Nous considérons que la présentation initiale d’une régurgitation aortique sévère détermine une plus grande sévérité de la dissection, dont l’origine ou l’étendue inclut la racine aortique, et donc une prise en charge agressive avec résection de la racine aortique et de la valve et implantation d’un greffon valvulaire (technique de Bentall) devrait être la procédure de choix.4,6,29,31 Dans ces cas, la resuspension de la valve, en épargnant la racine aortique, laisse derrière elle un segment intrinsèquement malade de l’aorte qui présente un plus grand risque de redissection et de complications ultérieures. Les résultats publiés sur la technique de remplacement de la racine aortique avec réimplantation de la valve aortique (technique de David) sont prometteurs et, bien qu’une évaluation à long terme soit nécessaire, elle pourrait devenir une option intéressante33,34.
Sur les 56 patients ayant survécu à la sortie de l’hôpital et ayant subi un scanner au cours du suivi, ce n’est que chez 6 (11%) que la dilatation progressive dans d’autres régions de l’aorte était évidente avec une indication chirurgicale : 2 patients avec un anévrisme de l’aorte abdominale, 2 avec un anévrisme thoraco-abdominal et 2 avec un anévrisme de l’aorte thoracique descendante. Parmi ces patients, 2 ont refusé la réintervention et les autres présentaient une certaine comorbidité (âge avancé, déficit neurologique sévère, etc.) qui rendait la procédure impossible.
Un si faible taux de réintervention de l’aorte distale est probablement dû au pourcentage élevé de déchirures intimales primaires localisées pendant l’intervention et à notre décision de les réséquer dans tous les cas. En fait, sur les 15 patients chez qui la déchirure intimale n’a pas été trouvée, 60 % (9 patients) faisaient partie du groupe qui n’a pas subi d’arrêt circulatoire (ce qui empêche l’examen de la crosse aortique et exclut les déchirures intimales à ce niveau) et qui présentait un risque accru de réintervention proche des limites de la signification statistique (P=.06). Ainsi, plusieurs auteurs décrivent l’absence de résection de la rupture intimale lors de la chirurgie initiale comme le principal facteur impliqué dans la réintervention tardive pour dilatation de l’aorte thoracique ou abdominale.6,30
Bien que notre groupe n’ait pas d’expérience à cet égard, certains auteurs soulignent que, dans des cas donnés, l’implantation d’une endoprothèse dans l’aorte thoracique descendante au cours de la procédure initiale ou d’une seconde pourrait améliorer les résultats en diminuant l’incidence de la réintervention et l’apparition des complications dues à la progression de la maladie vers l’aorte distale35,36.
La courbe de survie actuarielle après la sortie de l’hôpital indique des pourcentages comparables à ceux décrits par d’autres auteurs.2,3,5,6 L’âge avancé est l’un des facteurs de risque indépendants de mortalité pendant le suivi dans la plupart des séries, en partie à cause de la faible espérance de vie dans ce groupe de patients.2 En général, il y a une grande variabilité dans la détermination des prédicteurs indépendants de la survie à long terme. Chiappini et al2 ont décrit une série de 487 patients ayant subi une intervention pour une dissection aortique de type A et ont constaté que le seul facteur de risque était le diabète préopératoire. Erwin et al3, dans un groupe de 315 patients, ont identifié l’âge avancé et la dialyse postopératoire comme les prédicteurs de la mortalité au cours du suivi.
Dans notre série, nous avons constaté que la non-utilisation de la protection cérébrale antégrade était un prédicteur de la mortalité tardive, ce qui indique que, bien que la perfusion antégrade n’ait pas modifié de manière significative les résultats postopératoires initiaux, elle a une grande importance en ce qui concerne la survie tardive.
Ergin et al9 ont associé le TND postopératoire à une altération de la fonction cérébrale à long terme. Pompilio et al37 ont évalué l’influence des événements neurologiques périopératoires sur la mortalité tardive, c’est-à-dire que les patients qui ont survécu à l’hospitalisation en raison d’une lésion neurologique avaient un taux de survie à long terme plus mauvais. Ce fait peut s’expliquer par le risque élevé de bronchopneumonie, de nouveaux événements neurologiques et d’autres complications liées à la capacité fonctionnelle réduite de ces patients.4
Limites
Cet article partage toutes les limites associées aux études rétrospectives non randomisées. La faible incidence de cette maladie signifie que peu de patients ont subi une intervention, ce qui limite la puissance statistique des résultats.
Comme cette revue couvre une longue période d’expérience, les premiers patients, qui ont été pris en charge sans arrêt circulatoire, et les derniers patients, qui ont été pris en charge avec une perfusion cérébrale antégrade, n’étaient pas contemporains des autres méthodes de protection cérébrale mentionnées. La dernière méthode (perfusion cérébrale antégrade) a été appliquée à un petit échantillon (16 patients), ce qui limite la signification statistique des résultats.
CONCLUSIONS
La chirurgie de dissection aortique aiguë donne des résultats acceptables à court et à long terme et une intervention d’urgence devrait être indiquée chez la plupart des patients.
La régurgitation aortique sévère est associée à un risque élevé de réintervention précoce, ce qui justifierait une prise en charge agressive de la valve aortique lors de la chirurgie initiale.
La perfusion cérébrale antégrade a modifié le concept d’arrêt circulatoire et a amélioré le pronostic à long terme chez ces patients. Nous considérons que, bien que l’expérience de séries plus importantes soit nécessaire, l’application de la perfusion cérébrale antégrade dans la chirurgie de dissection aortique aiguë pourrait améliorer le pronostic chez ces patients.
ABBREVIATIONS
CT : tomographie informatisée
TND : dysfonctionnement neurologique temporaire
.