A billentyűs aorta szűkület (AS) a leggyakoribb billentyűbetegség a fejlett országokban. Az AS diagnózisát klasszikusan echokardiográfiával erősítik meg, amely a betegség kimutatásának és súlyosságának értékelésének standard eszköze (1). Mindazonáltal az AS súlyosságának értékelése még mindig kihívást jelent. A súlyos AS-t általában úgy határozzák meg, hogy az átlagos gradiens >40 mmHg, az aortabillentyű területe (AVA) <1 cm2 és az aorta sugár csúcssebessége >4,0 m/s (2). Egyetlen betegnél azonban gyakran figyelhető meg eltérés az átlagos gradiens és a billentyűterület között (3). Ezek az eltérések könnyen érthetőek azoknál a betegeknél, akiknél a csökkent LV-kilökődési frakció miatt alacsony a szívteljesítmény, de előfordulhatnak látszólag megőrzött LV-funkciójú betegeknél is (4). A mindennapi gyakorlatban potenciálisan a szűkület és a tünetek súlyosságának alulbecsléséhez, és így az aortabillentyűcsere (AVR) nem megfelelő késleltetéséhez vezethetnek, ami viszont negatív hatással lehet a betegek kimenetelére (5-7). A Cardiovascular Diagnosis and Therapy e számában OZKAN elegánsan áttekintette az alacsony gradiensű AS fogalmát megőrzött LV-funkciójú betegeknél (8).
Új aorta-szűkület osztályozási osztályozás
A közelmúltban több szerző is beszámolt arról, hogy a súlyos AS (AVA <1 cm2) azonos elnevezése alatt több entitás is azonosítható, amelyek a transzvalvuláris áramlási sebesség és a kialakuló nyomásgradiensek tekintetében különböznek (9-11). Elsőként Pibarot és munkatársai (5) csoportja hangsúlyozta a billentyű-gradiens kapcsolat áramlási mintázatba való integrálásának fontosságát, míg Miners és munkatársai (3) voltak az elsők, akik egyértelműen kimutatták az AS súlyosságának osztályozására vonatkozó következetlenségeket, és Dumesnil és munkatársaival (6) javaslatot tettek az AS új osztályozására. A <1 cm2 -es AVA-val rendelkező betegeknél négy áramlási gradiens AS-kategória azonosítható: normál áramlás/alacsony gradiens (NF/LG), normál áramlás/magas gradiens (NF/HG), alacsony áramlás/magas gradiens (LF/HG) és alacsony áramlás/alacsony gradiens (LF/LG). Az LF-t úgy definiálják, mint <35 ml/m2 indexált LV lökettérfogatot, az LG-t pedig mint <40 mmHg átlagos transzaorta nyomásgradienst (12).
Normális áramlás-alacsony gradiens
Ez a minta a betegek 31-38%-ánál figyelhető meg, és úgy tűnik, hogy az AS kevésbé súlyos fokával rendelkező betegcsoportot azonosítja – az irányelvekben szereplő következetlenség -, vagy aki rövidebb ideig volt kitéve a betegségnek. Ezt az entitást a megőrzött LV hosszanti myocardialis funkció jellemzi, ami alacsonyabb BNP-szintet és Monin kockázati pontszámot eredményez (12,13). Ezeknek a betegeknek a prognózisa a többi kategóriához képest viszonylag megőrzöttnek tűnik.
Normális áramlás-magas gradiens
Ez a minta képviseli a leggyakoribb entitást (39-72%), és teljes mértékben megfelel az irányelvek által javasolt kritériumoknak (4,5,12). Az NF/LG csoporttal összehasonlítva, bár az LV hosszanti funkciója megmarad, a BNP magasabb, és az NF/HG esetében csökken a szíveseménymentes túlélési arány. Továbbá úgy tűnik, hogy az NF/HG-s betegeknél súlyosabb az AS, ami arra utal, hogy a betegek hosszabb ideig vannak kitéve ennek a progresszív betegségnek. Tünet esetén ezeket a betegeket klasszikusan AVR-re utalják, míg tünetmentesség esetén e betegek kezelése az optimális rizikóstratifikáció szükségességét hangsúlyozza.
Low flow-high gradient
Ez a mintázat a súlyos AS-ben szenvedő betegek 8%-át teszi ki (4,12). Jellemzője az indexált LV stroke térfogat <35 ml/m2 a megőrzött LV ejekciós frakció, a magas BNP-szint és Monin kockázati pontszám, valamint az LV hosszanti funkció jelentős csökkenése ellenére (14). Megjegyzendő, hogy az LV ejekciós frakció az LV szisztolés funkció durva becslése. Az LV ejekciós frakciót mind az intrinsic myocardialis funkció, mind az LV-üreg geometriája befolyásolja. Ezért az intrinsic myocardialis rövidülés hasonló mértéke esetén az LV ejekciós frakció az LV koncentrikus remodelling mértékének függvényében növekszik. Az LV-kilökődési frakció ezért jelentősen alulbecsülheti a szívizom károsodásának mértékét az LV koncentrikus remodelling jelenlétében, ami általában az AS-betegeknél jellemző. Ezért ami normális egy normál geometriájú LV esetében, az abnormális lehet egy koncentrikus remodellinggel rendelkező LV esetében. Ezenkívül az LV teljesítményének csökkenése (a szívizom belső diszfunkciójához és a jelentős LV remodellinghez kapcsolódóan) a vártnál alacsonyabb transzvalvuláris gradienseket eredményezhet. Ezeknek a betegeknek a kimenetele majdnem azonos az NF/HG-s betegekével. Ha ezek a betegek tüneteket okoznak, sebészi kezelés esetén általában jobb a túlélésük.
Low flow-low gradient
Az LF/LG mintázat előfordulási gyakorisága alacsonyabbnak tűnik, mint amiről eredetileg beszámoltak. Ez az entitás a tünetmentes betegeknél 7%-ot, a tünetes betegeknél pedig akár 15-35%-ot is jelenthet (4-6,12,14). Ez a mintázat, nevezetesen a paradox alacsony áramlású AS, kihívást jelentő klinikai entitást jelent, amelyet a közelmúltban hangsúlyoztak. Kifejezettebb LV koncentrikus remodellinggel, kisebb LV-üreggel, megnövekedett globális LV-utóterheléssel, intrinsic myocardialis diszfunkcióval, myocardialis fibrosissal és borús prognózissal jár együtt (12,15). Tünetmentes betegeknél kimutattuk, hogy az AVR nélküli életben maradás valószínűsége 3 év múlva 5-ször kisebb volt, mint az NF/LG mintázat esetében, és 4,3-szor nagyobb, mint az NF/HG csoportban (12). Ezt a klinikai entitást gyakran tévesen diagnosztizálják, ami az AS súlyosságának alulbecsléséhez és ezáltal a műtét alulhasznosításához vagy nem megfelelő késleltetéséhez vezethet. Fontos felismerni ezt az entitást, hogy ne tagadjuk meg a műtétet egy tüneteket mutató, kis AVA-val és LG-vel rendelkező betegtől.
A gradiens és a billentyűterület közötti eltérés
Az AVA és a gradiens közötti eltérés lehetséges okai a megőrzött LV ejekciós frakciójú betegeknél a következők: (I) mérési hibák; (II) kis testméret; (III) paradox alacsony áramlású AS; és (IV) az irányelvek kritériumainak belső eltéréseivel kapcsolatos következetlen osztályozás (4,6,7,10,11). Először is, a kis testmérettel és LV méretekkel rendelkező betegek alacsonyabb transzvalvuláris nyomásgradienst mutathatnak a kisebb, bár normális lökettérfogat miatt. Másodszor, a lüktetési térfogat és ezáltal az AVA alulbecsült lehet a LV kiáramlási traktus alulbecslése és/vagy az impulzushullámos Doppler-mintatérfogat helytelen elhelyezése miatt. A stroke-térfogat és az AVA Doppler-echokardiográfiás méréseinek alátámasztására több módszer is alkalmazható. Jelentős mitrális regurgitáció hiányában például a Simpson-módszerrel (volumetrikus módszer az LV-kivetődési frakció és a térfogat mérésére) könnyen megbecsülhető a lüktető térfogat. Ha az ezekkel a független módszerekkel mért lüktetési térfogat összhangban van az LV kiáramlási traktusban mért lüktetési térfogattal, akkor megnyugodhatunk a lüktetési térfogat mérésének pontosságát illetően. Harmadszor, a paradox LF/LG egy új entitást képvisel, amelyben az LF állapot mind az LV koncentrikus remodelling, mind a csökkent szubendocardialis longitudinális funkció eredménye. Ez körvonalazza az AS súlyosságának hibás becslésének hiányát. Negyedszer, egyes esetekben a gradiens és a szelepterület közötti eltérés a jelenlegi irányelvek következetlenségeivel függhet össze. A súlyos AS definíciójának harmonizálása e “súlyos” AS-ben szenvedő betegek egy részét “mérsékelt” AS-be sorolhatja át. Ha a jelenlegi prospektív klinikai adatokat korábbi hemodinamikai echo és invazív adatokkal kombináljuk, úgy tűnik, hogy egy 40 mmHg gradiens jobban illeszkedik egy 0,8 cm2 -es billentyűterülethez, míg egy 1 cm2 -es billentyűterület 26 mmHg átlagos gradienshez kapcsolódik (3,6,16). Továbbá, ha a billentyűfelület (a súlyos tartományban) és a gradiens (a közepes tartományban) között eltérés mutatkozik a megőrzött LV-kilökődési frakciójú betegeknél, átfogóbb Doppler-echokardiográfiás értékelésre és esetleg más diagnosztikai vizsgálatokra (BNP, kalcium-pontszám multislice komputertomográfiával, terheléses/dobutaminos terheléses echokardiográfia) lehet szükség a betegség súlyosságának megerősítéséhez és a terápiás kezelés irányításához.
Klinikai következmények és kezelés
A mindennapi gyakorlatban az AS súlyosságának értékeléséhez az AVA klasszikus mérése mellett az áramlás-gradiens mintázatot is integrálni kell. Általános szabályként az alacsony transzvalvuláris gradiens (<40 mmHg) vagy sebesség (<4 m/s) nem zárja ki a súlyos AS jelenlétét kis AVA-val és megőrzött LV ejekciós frakcióval rendelkező betegeknél. Ezenkívül a megőrzött LV-kivetődési frakció (>50%) nem zárja ki a szívizom szisztolés diszfunkciójának és az alacsony transzvalvuláris áramlásnak a jelenlétét AS-ben. Az NF/LG AS-ben szenvedő betegeknél klasszikusan nincs vagy minimális a szubendocardialis diszfunkció és viszonylag megőrzött a kimenetel. Ebben az NF/LG kategóriában az AVR indikációját azokra a betegekre kell korlátozni, akiknél a tünetek egyértelműen az AS-nek tulajdoníthatók. Az NF/HG kategóriában az AVR (műtéti vagy perkután) az egyetlen olyan terápia, amely mind a túlélést, mind a tüneteket jelentősen javítja. Tünetmentesség esetén az egyéni rizikóstratifikáció segíthet azonosítani azokat a betegeket, akik számára előnyös lehet a korai műtét. A többi kategóriában az LF állapot az intrinsic myocardialis diszfunkció és a betegség előrehaladottabb folyamatának tanúja. A tünetes LF/HG-s betegeknek is előnyös lenne a gyors AVR. Tünetmentesség esetén az egyéni rizikóstratifikációt is ösztönözni kell. A terheléses echokardiográfia érdekes lehet a korlátozott billentyű compliance és/vagy kimerült LV kontraktilis tartalékkal rendelkező betegek leleplezése révén (17,18). A paradox LF/LG még tünetmentes betegek esetében is rossz kimenetelről árulkodik. Ebben a kategóriában, bár a műtét előnye nem bizonyított, az AVR valószínűleg előnyös lehet a kiválasztott tünetes betegeknél (7,19,20) (1. táblázat). A klinikai gyakorlatban ennek az entitásnak a megállapítása kihívást jelent. A műtét mérlegelése előtt a tüneteket össze kell vetni az AS súlyosságával. Alacsony kockázatú betegeknél az AVR javasolható. Nagy kockázatú betegeknél további kimenetel-vizsgálatokra van szükség a kezelés legmegfelelőbb módjának és időzítésének meghatározásához.
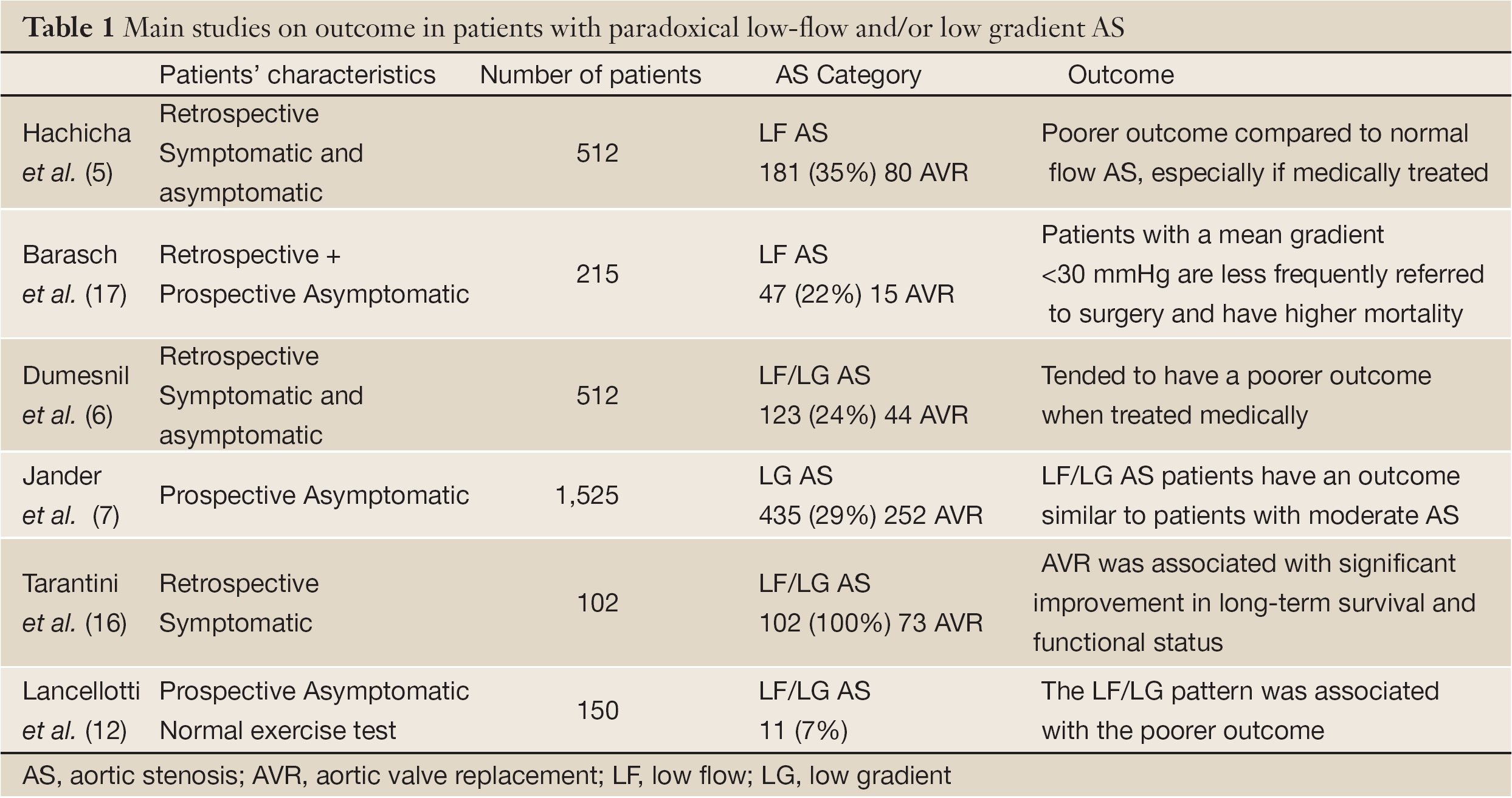
Teljes táblázat
Megköszönések
Közlés: A szerzők nem jelentenek összeférhetetlenséget.
- Lancellotti P, Donal E, Magne J, et al. Risk stratification in asymptomatic moderate to severe aortic stenosis: the importance of the valvular, arterial and ventricular interplay. Heart 2010;96:1364-71.
- Bonow RO, Carabello BA, Kanu C, et al. ACC/AHA 2006 Guidelines for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (writing committee to revise the 1998 Guidelines for the Management of Patients With Valvular Heart Disease): kifejlesztve a Kardiovaszkuláris Aneszteziológusok Társaságával együttműködésben: jóváhagyta a Society for Cardiovascular Angiography and Interventions és a Society of Thoracic Surgeons. Circulation 2006;114:e84-231.
- Minners J, Allgeier M, Gohlke-Baerwolf C, et al. Inconsistent grading of aortic valve stenosis by current guidelines: haemodynamic studies in patients with apparently normal left ventricular function. Heart 2010;96:1463-8.
- Adda J, Mielot C, Giorgi R, et al. Low-Flow, Low-Gradient Severe Aortic Stenosis Despite Normal Ejection Fraction Is Associated With Severe Left Ventricular Dysfunction as Assessed by Speckle-Tracking Echocardiography: A Multicenter Study. Circ Cardiovasc Imaging 2012;5:27-35.
- Hachicha Z, Dumesnil JG, Bogaty P, et al. Paradoxical low-flow, low-gradient severe aortic stenosis despite preserved ejection fraction is associated with higher afterload and reduced survival. Circulation 2007;115:2856-64.
- Dumesnil JG, Pibarot P, Carabello B. Paradoxical low flow and/or low gradient severe aortic stenosis despite preserved left ventricular ejection fraction: implications for diagnosis and treatment. Eur Heart J 2010;31:281-9.
- Jander N, Minners J, Holme I, et al. Outcome of patients with low-gradient “severe” aortic stenosis and preserved ejection fraction. Circulation 2011;123:887-95.
- Ozkan A. Low gradient “severe” aortic stenosis with preserved left ventricular ejection fraction. Cardiovasc Diagn Ther 2012;2:19-27.
- Dumesnil JG, Pibarot P, Akins C. New approaches to quantifying aortic stenosis severity. Curr Cardiol Rep 2008;10:91-7.
- Pibarot P, Dumesnil JG. Az aortaszűkület súlyosságának értékelése: amikor a gradiens nem illeszkedik a billentyűterülethez. Heart 2010;96:1431-3.
- Lancellotti P, Magne J. Valvuloarteriális impedancia aorta-szűkületben: nézzük a terhelést, de ne feledkezzünk meg az áramlásról. Eur J Echocardiogr 2011;12:354-7.
- Lancellotti P, Magne J, Donal E, et al. Clinical outcome in asymptomatic severe aortic stenosis insights from the new proposed aortic stenosis grading classification. J Am Coll Cardiol 2012;59:235-43.
- Monin JL, Lancellotti P, Monchi M, et al. Risk score for predicting outcome in patients with asymptomatic aortic stenosis. Circulation 2009;120:69-75.
- Lancellotti P, Donal E, Magne J, et al. Impact of global left ventricular afterload on left ventricular function in asymptomatic severe aortic stenosis: a two-dimensional speckle-tracking study. Eur J Echocardiogr 2010;11:537-43.
- Herrmann S, Störk S, Niemann M, et al. Low-gradient aortic valve stenosis myocardial fibrosis and its influence on function and outcome. J Am Coll Cardiol 2011;58:402-12.
- Zoghbi WA. Alacsony gradiensű “súlyos” aorta-szűkület normális szisztolés funkcióval: ideje finomítani az irányelveket? Circulation 2011;123:838-40.
- Lancellotti P, Lebois F, Simon M, et al. Prognostic importance of quantitative exercise Doppler echocardiography in asymptomatic valvular aortic stenosis. Circulation 2005;112:I377-82.
- Maréchaux S, Hachicha Z, Bellouin A, et al. Usefulness of exercise-stress echocardiography for risk stratification of true asymptomatic patients with aortic valve stenosis. Eur Heart J 2010;31:1390-7.
- Tarantini G, Covolo E, Razzolini R, et al. Valve replacement for severe aortic stenosis with low transvalvular gradient and left ventricular ejection fraction exceeding 0.50. Ann Thorac Surg 2011;91:1808-15.
- Barasch E, Fan D, Chukwu EO, et al. Severe isolated aortic stenosis with normal left ventricular systolic function and low transvalvular gradients: pathophysiologic and prognostic insights. J Heart Valve Dis 2008;17:81-8.