Inleiding
Volgens de Wereldgezondheidsorganisatie is kanker wereldwijd de tweede doodsoorzaak.1 De aanzienlijke en voortdurende vooruitgang in de behandeling heeft de overleving van kankerpatiënten doen toenemen, maar de nadelige effecten van chemotherapie, met name op het hart, zijn een belangrijke oorzaak van sterfte en morbiditeit. De mortaliteit onder kankerpatiënten die anthracycline-geïnduceerde cardiomyopathie ontwikkelen is hoog (meer dan 60% na twee jaar),2 maar de prognose kan worden verbeterd door vroege opsporing en preventie.
Anthracyclines zoals doxorubicine, daunorubicine, epirubicine, mitoxantrone en idarubicine zijn de meest gebruikte chemotherapiemedicijnen bij kanker. Zij zijn een bekende oorzaak van cardiotoxiciteit (tabel 1), met acute en/of subacute effecten die zich kunnen uiten in elektrocardiografische veranderingen, ventriculaire en supraventriculaire aritmieën, cardiale geleidingsstoornissen (atrioventriculair of takblok), ventriculaire disfunctie, stijging van het hersentype natriuretisch peptide (BNP, een marker van verhoogde voorspanning en hartfalen), myocarditis en pericarditis, en die kunnen optreden tussen het begin van de behandeling en twee weken na het einde van de behandeling. Deze effecten zijn betrekkelijk zeldzaam en de meeste keren een week na het staken van de behandeling terug. Chronische cardiomyopathie wordt als vroeg gedefinieerd als zij binnen een jaar na beëindiging van de chemotherapie begint en als laat na die periode. In beide gevallen wordt systolische of diastolische disfunctie waargenomen (tabel 2) die kan evolueren naar ernstige cardiomyopathie en zelfs tot de dood kan leiden.3 Hoewel sommige studies hebben gesuggereerd dat het risico op het ontwikkelen van ventriculaire disfunctie en de ernst ervan kan worden voorspeld op basis van acute myocardschade,4 is de relatie tussen acute en chronische toxiciteit niet volledig begrepen. De diagnose van hartdysfunctie ten gevolge van kankertherapie is het onderwerp geweest van verschillende studies,3,5 waarvan er een5 wordt beschouwd als de referentiepublicatie over dit onderwerp, en is gebaseerd op HF-symptomen, lichamelijk onderzoek en parameters van de linkerhartkamerfunctie.
Cardiotoxiciteit, farmacokinetiek en therapeutisch gebruik van anthracyclines.
| Werkingsmechanismen | Werkingsmechanismen van cardiotoxiciteit | Anthracycline | Therapeutisch gebruik | Cardiotoxiciteit |
|---|---|---|---|---|
| De vorming van een DNA-complex door conjugatie van platte ringen met nucleotiden remt de DNA- en RNA- en eiwitsynthese. Dit brengt DNA-splitsing door topoisomerase II op gang, hetgeen cytotoxiciteit tot gevolg heeft. Anthracyclinen remmen helicase, waardoor enzymatische splitsing van de dubbele streng van het DNA wordt voorkomen en aldus replicatie en transcriptie worden verstoord. Zij veroorzaken redoxreacties door vorming van cytotoxische vrije radicalen. |
Belangrijkste mechanismen: – topoisomerase II beta-gemedieerde DNA-beschadiging – lipide peroxidatie – oxidatieve stress – apoptose en necrose van hartcellen gestoorde synthese van DNA, RNA en eiwitten en van transcriptiefactoren die betrokken zijn bij de regulatie van genen die specifiek zijn voor het hart. Negatieve balans van sarcomereiwitten in hartcellen door verminderde eiwitexpressie en verhoogde myofilamentdegradatie. Combinatietherapie verergert het myofilamentverlies. Mitochondriale DNA-beschadiging en veranderingen in de mitochondriale bio-energetica. Verstoring van de dynamische regulatie van de hartfunctie, waarbij de adrenerge en adenylyl cyclase-activiteit en de calciumhomeostase worden gewijzigd. |
Doxorubicine | Vergevorderde maagkanker Blaaskanker Borstkanker Ovariële kanker Kleincellige longkanker Thyroïdkanker Ziekte van Hodgkin Acute leukemie Non-Hodgkin lymfoom Neuroblastoom Sarcoom Wilms tumor |
Acute: Hypotensie Arrhythmieën Tachycardie Thromboembolisme Subacuut: Pericarditis Myocarditis Chronisch: Dilaterende cardiomyopathie Contractiele disfunctie Congestief hartfalen |
| Daunorubicine | Acute lymfoblastische leukemie Acute myeloïde leukemie |
Acute: Sinus tachycardie Tachyaritmieën Ventriculaire extrasystolen AV blok Chronisch: Dilaterende cardiomyopathie Contractiele disfunctie Congestief hartfalen |
||
| Epirubicine | Vergevorderde eierstokkanker Maagkanker Borstkanker Longkanker |
Acute: Ventriculaire tachycardie AV-blok Bundeltakblok Bradycardie Thrombo-embolie Chronisch: Dilaterende cardiomyopathie Contractiele disfunctie Congestief hartfalen |
||
| Idarubicine | Acute lymfocytaire leukemie Acute myeloïde leukemie |
Acute: Arrhythmieën Atriumfibrilleren Myocardinfarct Thromboembolisme Chronisch: Dilaterende cardiomyopathie Contractiele disfunctie Congestief hartfalen |
||
| Mitoxantrone | Vergevorderde borstkanker Acute myeloïde leukemie bij volwassenen Non-Hodgkin lymfoom |
Acute: Arrhythmieën Myocarditis Hypertensie Myocardische ischemie Chronisch: Dilaterende cardiomyopathie Contractiele disfunctie Congestief hartfalen |
AV: atrioventriculaire.
Opgenomen uit 24,58,59.
Criteria voor het bevestigen of herzien van een voorlopige diagnose van door chemotherapie geïnduceerde cardiale dysfunctie, volgens de Cardiac Review and Evaluation Committee.
Een van de criteria is voldoende om een diagnose van hartdysfunctie te bevestigen.
Cardiomyopathie gekenmerkt door een afname van de cardiale LVEF die ofwel globaal is ofwel ernstiger in het septum
Symptomen van CHF
Detectie van S3-galop, tachycardie, of beide;
Afname van de LVEF van ten minste 5% tot minder dan 55% met begeleidende tekenen of symptomen van hartinsufficiëntie, of een afname van de LVEF van ten minste 10% tot minder dan 55% zonder begeleidende tekenen of symptomen.
CHF: congestief hartfalen; LVEF: linker ventrikel ejectiefractie.
Opgesteld op basis van 3,60.
Een voorgestelde classificatie verdeelt chemotherapie-geïnduceerde cardiomyopathie in twee typen: type I, veroorzaakt door anthracyclines, die onomkeerbare dosisafhankelijke cardiale schade induceren; en type II, veroorzaakt door trastuzumab, die geen verband houdt met de cumulatieve dosis en die vaak omkeerbaar is na het staken van de behandeling.6 Het tweede type wordt in dit overzichtsartikel niet besproken.
In dit overzicht bespreken de auteurs strategieën bij patiënten die met anthracyclines worden behandeld om de belangrijkste nadelige effecten op het hart te voorkomen of te beperken.
Initiële beoordeling
In verband met de cardiotoxiciteit van anthracyclines moeten alle patiënten die voor chemotherapie worden verwezen een cardiale beoordeling ondergaan om hun cardiovasculaire basiskenmerken vast te stellen, die vervolgens tijdens het behandelingsschema kunnen worden gebruikt voor vergelijkingsdoeleinden. Deze beoordeling moet bestaan uit een klinische anamnese en lichamelijk onderzoek, elektrocardiografie om het hartritme te bepalen en tekenen van ischemie op te sporen, en beeldvorming van het hart, meestal transthoracale echocardiografie met volledig Doppler-onderzoek (tabellen 3 en 4). Wanneer het echocardiogram onvoldoende informatie oplevert, wordt cardiale magnetische resonantie beeldvorming (CMRI) aanbevolen. Voor toekomstige vergelijkingen moeten ook baseline troponineniveaus worden gemeten.5
Aanbevolen protocol cardio-oncologie-echocardiogram.
Standaard transthoracale echocardiografie
– In overeenstemming met ASE/EAE-richtlijnen en IAC-Echo
2D strain imaging-acquisitie
– Apicale 3-, 4-, en 2-kameraanzichten
– Acquire ≥3 hartcycli
– Gelijktijdig verkregen beelden met behoud van dezelfde 2D-framesnelheid en beelddiepte
Framesnelheid tussen 40 en 90 frames/s of ≥40% van HR
– Aortale VTI (aorta-ejectietijd)
ejectietijd)
2D analyse van stammen
– Kwantificeren van segmentale en globale longitudinale stam
– Weergeven van de segmentale stamcurves van apicale aanzichten in een quad-formaat
– Weergeven van de globale stam in een bull’s-oog plot
– Weergeven van de globale stam in een bull’s-oog plot
oogplot
2D strain imaging valkuilen
– Ectopie
– Adem translatie
3D imaging acquisitie
– Apicale 4-kamer volledig volume om LV-volumes te beoordelen en LVEF te berekenen
– Enkelvoudige en meervoudige slagen om ruimtelijke en temporele resolutie te optimaliseren
Rapportage
– Timing van echocardiografie ten opzichte van het IV-infuus (aantal dagen ervoor of erna)
– Vitale functies (BP, HR)
– 3D LVEF/2D biplane Simpson-methode
– GLS (gebruikte echocardiografiemachine, software en versie)
– Bij afwezigheid van GLS, meting van mediale en laterale s′ en MAPSE
– RV: TAPSE
Aangepast uit 5.
2D: tweedimensionaal; 3D: driedimensionaal; ASE/EAE: American Society of Echocardiography/European Association of Echocardiography; BP: bloeddruk; GLS: global longitudinal strain; HR: hartfrequentie; IAC-Echo: Intersocietal Accreditation Commission Echocardiography; IV: intraveneus; LV: linker ventrikel; LVEF: linker ventrikel ejectiefractie; MAPSE: mitral annular plane systolische excursie; RV: rechter ventrikel; TAPSE: tricuspid annular plane systolische excursie; VTI: velocity-time integral.
Echocardiografische beoordeling van de systolische en diastolische functie bij de kankerpatiënt.
LV systolische functie
– Echocardiografie is de methode bij uitstek voor de beoordeling van patiënten vóór, tijdens en na kankertherapie.
– Nauwkeurige berekening van de LVEF moet worden uitgevoerd met de beste methode die in het echocardiografielaboratorium beschikbaar is (idealiter 3DE).
– Bij gebruik van 2DE is de gewijzigde biplane Simpson-techniek de methode van keuze.
– De LVEF moet worden gecombineerd met de berekening van de wall motion score index.
– Bij afwezigheid van GLS door STE wordt kwantificering van de longitudinale functie van de LV met behulp van MAPSE en/of de pieksnelheid van de systolische snelheid (s′) van de mitralis annulus door middel van pulsed-wave TDI aanbevolen.
– Bij LVEF-beoordeling met behulp van 2DE worden kleine veranderingen in LV-contractiliteit vaak niet gedetecteerd.
Diastolische functie
– Hoewel diastolische parameters niet prognostisch zijn gebleken voor door anthracycline geïnduceerde cardiomyopathie, kan een conventionele beoordeling van de LV-diastolische functie, inclusief gradering van de diastolische functie en niet-invasieve schatting van de vullingsdruk van de LV, worden toegevoegd aan de beoordeling van de systolische functie van de LV, overeenkomstig de aanbevelingen van de ASE/EAE voor de evaluatie van de diastolische functie van de LV met echocardiografie.
Opgesteld uit 5.
2DE: tweedimensionale echocardiografie; 3DE: driedimensionale echocardiografie; ASE/EAE: American Society of Echocardiography/European Association of Echocardiography; GLS: global longitudinal strain; LV: linkerventrikel; LVEF: linker ventrikel ejectiefractie; STE: speckle-tracking echocardiografie; TDI: tissue Doppler imaging.
Controle tijdens de therapie
Het is belangrijk om tijdens de chemotherapie te controleren op tekenen en symptomen van cardiotoxiciteit (tabel 5). Het 12-afleidingen elektrocardiogram kan routinematig worden gebruikt om te screenen op aritmieën als gevolg van anthracycline-gerelateerde cardiotoxiciteit, terwijl 24-uurs Holter-monitoring of een event recorder nuttig kan zijn om de etiologie te onderzoeken van syncope die vermoedelijk het gevolg is van aritmie of gevorderd atrioventriculair blok.7 De hartfunctie moet worden gecontroleerd door middel van echocardiografie bij patiënten die met anthracycline worden behandeld. Globale longitudinale rek (GLS) zoals beoordeeld met tweedimensionale speckle tracking is een gevoeligere voorspeller van HF dan linker ventrikel ejectiefractie (LVEF),8 aangezien tijdens anthracycline therapie veranderingen in GLS voorafgaan aan vermindering van LVEF.5 In de klinische praktijk zijn fractionele verkorting en LVEF echter de meest gebruikte parameters geweest,9 hoewel fractionele verkorting in deze context minder betrouwbaar blijkt te zijn. Deze parameters, die afhankelijk zijn van de voor- en nabelasting, zijn minder gevoelig voor de vroege opsporing van preklinische hartziekte. Verschillende studies hebben gesuggereerd dat beoordeling van de diastolische functie met behulp van Doppler-echocardiografie vroegtijdige opsporing van door anthracycline veroorzaakte cardiomyopathie mogelijk kan maken.10,11 Als de LVEF Tabel 6) is en/of de troponines verhoogd zijn, moet een cardiologische raadpleging worden overwogen, waarbij de risico/batenverhouding van chemotherapie tussen de cardioloog en de oncoloog moet worden besproken.5 Een daling van de LVEF tijdens anthracycline-therapie is geassocieerd met een verhoogd risico op cardiale voorvallen, en hoewel een daling van de GLS van 15% waarschijnlijk wijst op cardiotoxiciteit.5 Het onderzoek moet twee tot drie weken na het basisonderzoek worden herhaald om de diagnose te bevestigen. CMRI kan subtiele veranderingen in het myocard en verhogingen van het extracellulaire volume detecteren, die wijzen op oedeem of diffuse fibrose. Hoewel CMRI zeer gevoelig en reproduceerbaar is voor het beoordelen van de hartfunctie en het karakteriseren van myocardweefsel, heeft het de nadelen van beperkte beschikbaarheid en hoge kosten.12 Radionuclide-angiografie is reproduceerbaar en gemakkelijker beschikbaar, maar stelt patiënten bloot aan ioniserende straling, waardoor hun cumulatieve dosis toeneemt, vooral wanneer er seriële onderzoeken nodig zijn, en geeft slechts beperkte informatie over de diastolische functie en klepmorfologie, en zou daarom niet de methode van keuze moeten zijn.12 Endomyocardiale biopsie heeft een grotere sensitiviteit en specificiteit voor de detectie en monitoring van de nadelige effecten van anthracyclines,5 waardoor verlies van myofibrillen, vacuolisatie van cytoplasma, dilatatie van het sarcoplasmatisch reticulum, verhoogd aantal lysosomen en mitochondriale zwelling zichtbaar kunnen worden.12 De invasieve aard van de procedure beperkt echter het gebruik ervan in de klinische praktijk. Biomarkers zijn in verschillende studies gevalideerd; zij zijn niet alleen specifiek voor het opsporen van cardiovasculaire schade, maar ook voor het bepalen van de omvang en de omkeerbaarheid ervan. Terwijl troponine T en I indicatoren zijn voor schade aan de cardiomyocyten, weerspiegelen BNP en het N-terminale gedeelte van pro-BNP (NT-proBNP) een verhoogde myocardiale stress.13,14 Volgens de literatuur is verhoging van troponinen een vroege indicator van cardiotoxiciteit, terwijl BNP minder consistent is.
Voordelen en nadelen van diagnostische onderzoeken bij de beoordeling van door anthracycline veroorzaakte cardiotoxiciteit.
| Diagnostisch onderzoek | Voordelen | Nadelen |
|---|---|---|
| Electrocardiografie | Niet-invasief Lage kosten Metingen QT-interval, waarvan verlenging een bekende marker voor cardiotoxiciteit is |
Metert geen LVEF Intra- en inter-observer variabiliteit in meting van QT interval |
| Doppler echocardiografie | Niet-invasief Lage kosten Beoordeling van functionele en morfologische diastolische (pulmonaal veneuze flow, E/A ratio, isovolumische relaxatietijd) en systolische (wandverdikking tijdens systole, LVEF, fractionele verkorting) parameters, klepstructuur en pericard |
Intra- en inter-waarnemersvariabiliteit Meting van LVEF onderhevig aan variabiliteit en afhankelijk van beeldkwaliteit Twijfelachtige voorspellende waarde voor vroege detectie van subklinische laesies |
| Weefsel-Doppler beeldvorming | Uitstekende temporele resolutie Vroege opsporing van subklinische laesies (in combinatie met markers van ontsteking en oxidatieve stress) Functionele beoordeling van vullingsdrukken (E/e′-verhouding), snelheden, rek en reksnelheid van ventrikelwanden in systole en diastole Opsporing van geïsoleerde diastolische disfunctie |
Meer tijdtijdrovende analyse |
| 2D strain/speckle tracking en GLS | Superieur aan LVEF voor het voorspellen van cardiovasculaire mortaliteit in de algemene bevolking Betere risicostratificatie bij HF-patiënten Mogelijk vroegtijdige LV-dysfunctie te herkennen bij patiënten die een cardiotoxische therapie ondergaan Reproduceerbaar indien uitgevoerd door een ervaren operator |
Zwaar afhankelijk van beeldkwaliteit van 2D-echocardiografie Geen klinisch onderzoek op langeklinische studies op lange termijn naar het vermogen van GLS om aanhoudende dalingen in LVEF of symptomatisch HF te voorspellen |
| Stress-echocardiografie | Bepaling van myocardiale contractiele reserve | Semi-invasief Controversieel en beperkte gegevens over vroege detectie van cardiotoxiciteit |
| Radionuclide-angiografie | Hoge reproduceerbaarheid Lage intra- en inter-waarnemer Gevalideerd voor meting van LVEF |
Ioniserende straling Lage ruimtelijke en temporele resolutie Onjuiste schatting van ventriculaire volumes Onjuiste schatting van LVEF in kleine ventrikels (vrouwen en kinderen) Beoordeelt niet de klepfunctie Weinig informatie over diastolische functie Beperkte voorspellende waarde voor vroege opsporing van subklinische laesies en veranderingen in LVEF |
| Magnetische resonantiebeeldvorming | Reproduceerbaar Geen ioniserende straling Beoordeling van myocardperfusie en -functie en pericard, en detectie van myocardmassa’s Gebruikbaar bij patiënten met slechte echocardiografische beeldkwaliteit Gouden standaard voor berekening van LV volumes en van LVEF T2 sequenties: detecteert segmentale of globale veranderingen in het myocardiale watergehalte als gevolg van ontsteking of microvasculaire of myocytenschade T1 sequenties: geeft informatie over myocardiale laesies en fibrose; met gadoliniumcontrast, detecteert histopathologische veranderingen met inbegrip van intracellulaire vacuolisatie, waardoor voorspelling van latere daling van LVEF Late versterking: detectie van myocardiale fibrose geassocieerd met slechte prognose bij patiënten met CAD, hypertrofische cardiomyopathie en infiltratieve ziekte |
hoge kosten Beperkte beschikbaarheid Geïndiceerd bij patiënten met apparaten die niet compatibel zijn met magnetische resonantie (pacemakers, cardiale resynchronisatieapparaten en implanteerbare cardioverter-defibrillatoren) Risico op contrastnefrotoxiciteit bij patiënten met nierfalen (GFR |
| Computed tomography | High-resolutie beeld Identificeert pericardiale calcificatie of verdikking bij patiënten die radiotherapie of chirurgie ondergaan Visualiseert en beoordeelt calcificatie van de kransslagaders |
Ioniserende straling Gedocumenteerde coronaire calcificatie vóór antikankertherapie is niet voorspellend voor het CV-risico bij patiënten die anthracycline-chemotherapie ondergaan Weinig gebruikt voor detectie en monitoring van subklinische veranderingen in de hartfunctie |
| Scintigrafie | Non-invasief Functionele en structurele beoordeling |
Ioniserende straling Beperkte beschikbaarheid Lage temporele resolutie Beperkte data |
| Biomarkers | Niet-invasief Lage inter-waarnemersvariabiliteit Beoordeling van CV-functie en mogelijke tekenen van hartschade Belofte voor vroege detectie van myocardschade |
Onbepaalde voorspellende waarde |
| Endomyocardiale biopsie | Opsporing van histologisch bewijs van hartschade, inclusief verlies van myofibrillen, vacuolisatie van cytoplasma, dilatatie van het sarcoplasmatisch reticulum, toegenomen aantallen lysosomen en mitochondriale zwelling | Invasief Histologische interpretatie vereist specialistische kennis Geen functionele informatie Resultaten beperkt door hoeveelheid en kwaliteit van biopsiemonster |
| Beoordeling van endotheelschade | Alternatieve parameters van cardiotoxiciteit zoals cytokines, adhesiemoleculen en intima-mediadikte van de halsslagader | Onbepaalde voorspellende waarde |
| Genetische analyse | Minimaal invasief Beoordeelt individuele gevoeligheid voor cardiotoxiciteit |
Onbepaalde voorspellende waarde. |
Opgesteld op basis van 5,12,61.
2D: tweedimensionaal; CAD: coronaire hartziekte; CV: cardiovasculair; ECG: elektrocardiografie; GFR: glomerulaire filtratiesnelheid; GLS: globale longitudinale stam; HF: hartfalen; LV: linkerventrikel; LVEF: linkerventrikel ejectiefractie.
Normale waarden van de totale longitudinale rek per scannerleverancier, geslacht en leeftijd.
| Leeftijd (jaren) | ||||||||
|---|---|---|---|---|---|---|---|---|
| 0-19 | 20-29 | 30-39 | 40-49 | 50-59 | ≥65 | p | ||
| V1 | ||||||||
| Globaal | -22.1±2.4 | -21.2±1.9 | -21.1±2.1 | -21.4±2.0 | -21.0±2.2 | -20.3±1.9 | 0.0218 | |
| Mannelijk | -21.7±3.1 | -20.9±1.9 | -20.6±1.9 | -20.9±1.8 | -21.0±1.9 | -19.7±1.4 | 0.1982 | |
| Vrouw | -22.4±1.6 | -22.4±1.6 | -22.0±1.6 | -21.0±1.9 | -19.7±1.4 | 0.1982 | ||
| .3±1.6 | -22.8±1.8 | -22.6±2.1 | -23.3±1.9 | -20.9±2.1 | 0.0348 | |||
| p (man vs. vrouw) | 0.4292 | 0.0316 | 0.0178 | 0.0029 | 0.1381 | |||
| V2 | ||||||||
| Algemeen | -19.9±2.5 | -19.0±2.1 | -19.5±2.2 | -18.2±2.5 | -17.6±2.5 | -16.7±2.1 | ||
| Mannelijk | -19.4±2.7 | -18.8±2.0 | -19.1±2.3 | -17.9±2.8 | -16.9±2.3 | -15.8±1.4 | 0.0019 | |
| Vrouw | -20.5±2.2 | -20.5±2.2 | -20.8±1.4 | 0.0019 | ||||
| .6±2.3 | -20.2±2.0 | -19.3±0.9 | -20.4±1.5 | -17.3±2.3 | 0.0002 | |||
| p (man vs. vrouw) | 0.1349 | 0.0248 | 0.1083 | 0.4316 | 0.0294 | 0.0928 | ||
| V3 | ||||||||
| Algemeen | -21.4±1.7 | -20.2±2.1 | -20.4±2.3 | -19.4±2.2 | -18.5±2.6 | -17.8±2.8 | ||
| Mannelijk | -21.6±2.0 | -20.2±2.0 | -20.4±2.2 | -19.8±2.3 | -18.7±2.6 | -16.3±3.1 | ||
| Vrouw | -21.1 | -21.1 | -21.1 | -21.1 | -21.2 | |||
| .2±1.5 | -20.2±2.4 | -20.4±2.8 | -18.7±1.8 | -18.3±2.8 | -18.6±2.3 | 0.0141 | ||
| p (man vs. vrouw) | . vrouw) | 0.6076 | 0.9787 | 0.9201 | 0.1415 | 0.7374 | 0.0668 | |
V1: Vivid 7 of Vivid E9 (GE Healthcare); V2: iE33 (Philips Medical Systems); V3: Artida of Apilo (Toshiba Medical Systems).
Opgenomen uit 62.
Als de dosis anthracyclinen hoger is dan 240 mg/m2, moet de cardiale beoordeling worden herhaald voordat verdere cycli worden toegediend (figuur 1).
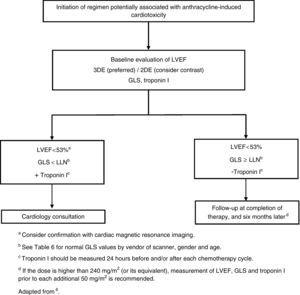
Begin van een behandeling die mogelijk in verband kan worden gebracht met anthracycline-geïnduceerde cardiotoxiciteit. 2DE: tweedimensionale echocardiografie; 3DE: driedimensionale echocardiografie; GLS: globale longitudinale rek; LLN: ondergrens van normaal; LVEF: linker ventrikel ejectiefractie.
Preventie van cardiotoxiciteit
Preventie van anthracycline-geïnduceerde cardiotoxiciteit, met behoud van de therapeutische effectiviteit van de geneesmiddelen, kan worden bereikt met farmacologische en niet-farmacologische middelen.
Niet-farmacologische preventie
Cardiovasculaire risicofactoren moeten worden geïdentificeerd en op de juiste wijze worden behandeld zodra de diagnose kanker is gesteld. Patiënten moeten worden aangemoedigd een gezonde levensstijl aan te nemen, met inbegrip van een dieet met weinig verzadigde vetten en maximaal 2,5 g natrium per dag, toxische stoffen zoals alcohol en tabak te vermijden, en hun body mass index dicht bij 25 kg/m2 te houden. Oefeningen, van lage of hoge intensiteit, tijdens anthracycline-therapie verhogen de cardiovasculaire reserve15 en studies in diermodellen hebben aangetoond dat ze de cardiotoxische effecten van deze middelen kunnen verminderen.16 Hoewel oefeningen veelbelovend zijn gebleken voor het verbeteren van de cardiopulmonale functie bij borstkankeroverlevenden,17,18 zijn er geen klinische studies bij mensen uitgevoerd die de cardioprotectieve rol ervan bevestigen. Een andere maatregel is het verminderen of vermijden van het gebruik van geneesmiddelen die het QT-interval verlengen, met name 5-hydroxytryptamine 3-antagonisten (die vaak worden gebruikt om bijwerkingen van chemotherapie zoals misselijkheid en braken te voorkomen) en antihistaminica.19,20 Het is ook belangrijk de blootstelling aan straling tot een minimum te beperken, elektrolytstoornissen te corrigeren en comorbiditeiten te behandelen (tabel 7).21
Risicofactoren voor anthracycline-geïnduceerde cardiotoxiciteit.
| Cumulatieve doses hoger dan: | Aanbevolen maximum (mg/m2)a: | |
| Doxorubicine | 400-550 | |
| Daunorubicine | 550-800 | |
| Epirubicine | 900-1000 | |
| Idarubicine | 150-225 | |
| Mitoxantrone | 100-140 | |
| Pre-bestaande CV ziekte | Diabetes | |
| Coronaire hartziekte | ||
| Perifere vasculaire ziekte | ||
| Hypertensie | ||
| Genetische predispositie: vrouwelijk geslacht, zwart ras | ||
| Vorige of gelijktijdige mediastinale bestraling | ||
| Intraveneuze bolustoediening | ||
| Combinatie met andere middelen waaronder cyclofosfamide, trastuzumab of paclitaxel | ||
| Lange tijd sinds het einde van de chemotherapie | ||
| Electrolytstoornissen: hypocalciëmie, hypomagnesemie | ||
| Hemochromatose (C282Y-mutatie) | ||
| Hyperthermie | ||
| Leverziekte | ||
CV: cardiovasculair.
Patiënten ouder dan 65 jaar en kinderen kunnen cardiotoxiciteit ontwikkelen bij lagere cumulatieve doses.
Opgesteld op basis van 12,24.
Verlaging van de dosis anthracyclinen is een andere manier om de incidentie van linkerventrikel systolische dysfunctie (LVSD) te verminderen, zoals blijkt uit een onderzoek bij patiënten die 400, 500 of 550 mg/m2 doxorubicine innamen, waarbij de incidentie van congestieve HF respectievelijk 5%, 16% en 26% bedroeg.22 Hoewel anthracyclines cardiotoxisch lijken te zijn, onafhankelijk van de toegediende dosis, hebben verschillende studies aangetoond dat continue infusie van lagere doses gedurende 24 tot 92 uur23 de ernst van de cardiotoxiciteit kan verminderen, en is dit beschreven als een effectieve manier.24 Verlenging van de infusietijd vermindert de cardiotoxiciteit zonder de effectiviteit van de chemotherapie in gevaar te brengen,25 maar infusie die langer duurt dan 96 uur wordt geassocieerd met een hoge incidentie van stomatitis. Het enige geval waarin continue infusie van doxorubicine geen cardioprotectief effect lijkt te hebben in vergelijking met snelle infusie, is bij kinderen met acute lymfoblastische leukemie (ALL).26 Andere klinische onderzoeken waarbij endomyocardiale biopsie werd gebruikt om anthracycline-geïnduceerde cardiale schade te beoordelen in verschillende medicatieschema’s, concludeerden dat continue perfusie tot veel minder significante schade leidt dan snelle intraveneuze toediening.27 Uit deze onderzoeken bleek ook dat patiënten die continue infusie kregen een grotere tolerantie hadden voor hogere cumulatieve doses doxorubicine. Hoewel dierstudies aantoonden dat de anthracyclinespiegels in tumorweefsel gelijk waren ongeacht de wijze waarop de geneesmiddelen werden toegediend (continue of snelle infusie), gold dit niet voor hartweefsel, waarin snelle infusie tot hogere concentraties en dus tot een grotere toxiciteit leidde.28
Farmacologische preventieAntioxidanten
Hoewel antioxidanten vrije radicalen, gevormd door anthracycline therapie, neutraliseren en dus theoretisch cardiotoxiciteit verminderen of voorkomen, toonden klinische trials met N-acetylcysteïne, co-enzym Q, L-carnitine, fenethylamines, amifostine en een combinatie van vitamine E en C en N-acetylcysteïne geen cardioprotectief effect aan.29 Van erytropoëtine en iloprost30 is aangetoond dat ze in vitro bescherming bieden tegen de cardiotoxische effecten van doxorubicine, zonder de antikankereffectiviteit ervan te beïnvloeden, maar hun cardioprotectieve vermogen zal in vivo moeten worden aangetoond.
Liposomale formuleringen
Een manier om de nadelige cardiale effecten van anthracyclines te bestrijden is de formulering van de geneesmiddelen te wijzigen, bijvoorbeeld door ze in te kapselen in liposomen.31 In studies waarin niet-ingekapselde en in liposomen ingekapselde doxorubicine werden vergeleken, werd geen verschil gevonden in de antitumorrespons, de totale overleving of de progressievrije overleving, maar de incidentie van HF en LVSD was lager bij patiënten die werden behandeld met de liposomale formulering, en deze groep had ook een lagere incidentie van andere bijwerkingen, waaronder neutropenie, misselijkheid, braken en diarree.32 Vanwege hun hoge kosten worden deze formuleringen niet op grote schaal gebruikt en de Amerikaanse Food and Drug Administration (FDA) heeft het gebruik ervan alleen goedgekeurd voor eierstokkanker, AIDS-gerelateerd Kaposi sarcoom, en patiënten met multipel myeloom die niet hebben gereageerd op een jaar behandeling met andere geneesmiddelen.33
Dexrazoxaan
De gelijktijdige toediening van dexrazoxaan met antikankerregimes kan een cardioprotectief effect hebben, waarbij verhoging van troponinen wordt voorkomen en de incidentie van HF wordt verminderd.34 Sommige auteurs schrijven het cardioprotectieve effect van deze ijzerchelator toe aan de vermindering van de hoeveelheid intracellulair ijzer, waardoor de door doxorubicine veroorzaakte productie van vrije radicalen kan afnemen.34 Studies naar andere ijzerchelatoren hebben echter geen cardioprotectie aangetoond.35,36 Er is ook gesuggereerd dat het cardioprotectieve effect van dexrazoxaan niet alleen te wijten is aan het feit dat het de vorming van topoisomerase II splitsingscomplexen tegengaat, maar ook aan de inductie van snelle degradatie van topoisomerase II beta, wat suggereert dat dit enzym betrokken is bij de door anthracycline veroorzaakte cardiotoxiciteit.37 Een studie van dexrazoxaan bij meer dan 200 kinderen met ALL toonde aan dat het de troponine T verhoging verminderde bij beide geslachten,38 en dat het de vermindering van de fractionele verkorting beperkte en de linker ventrikel dikte-dimensie ratio handhaafde na vijf jaar, maar alleen bij meisjes.39 Recentelijk zijn er drie gevallen gerapporteerd van volwassenen die chemotherapie ondergingen in combinatie met dexrazoxaan voor borstkanker en die acute myeloïde leukemie ontwikkelden. Twee studies waarin dexrazoxaan werd vergeleken met placebo bij kinderen met ALL die gedurende vijf en tien jaar werden gevolgd, toonden echter geen verschil in de incidentie van secundaire maligniteit.40,41 Niettemin hebben de FDA en het Europees Geneesmiddelenbureau, gezien de bekende bijwerkingen, het gebruik van dexrazoxaan beperkt tot volwassen patiënten met gevorderde of gemetastaseerde borstkanker die reeds een cumulatieve dosis doxorubicine van meer dan 300 mg/m2 hebben gekregen en die baat zullen hebben bij aanvullende anthracyclinetherapie.42
Bètablokkers
De cardioprotectie die wordt geboden door bètablokkers (BB’s) lijkt voort te komen uit hun antioxiderende en anti-apoptotische eigenschappen. Eén BB, carvedilol, is bijzonder veelbelovend gebleken in het verminderen van de incidentie van anthracycline-geïnduceerde cardiomyopathie en het behoud van de systolische en diastolische functie.43 Bij kinderen beperkte carvedilol de troponine I-stijging en verbeterde zowel de fractionele verkorting als de totale systolische piekspanning.44 Volgens sommige studies kunnen BB’s en angiotensine-converting enzyme (ACE)-remmers (zie hieronder) de met HF geassocieerde remodellering voorkomen door de adrenerge respons te verminderen.45,46 Er zijn echter geen cardioprotectieve effecten waargenomen met metoprolol of enalapril.47
Angiotensine-converterende-enzymremmers en angiotensine-receptorblokkers
ACE-remmers en angiotensine-receptorblokkers (ARB’s) vertonen cardioprotectieve eigenschappen, mogelijk door vermindering van oxidatieve stress, linkerventrikelremodellering en apoptose.48 Wanneer enalapril gedurende ten minste twee jaar na het staken van de chemotherapie werd toegediend aan kinderen met door anthracyclines veroorzaakte LVSD, bleek er geen voordeel te zijn wat betreft vermindering van de belasting van de linkerventrikelwand aan het eind van de systolische wand of behoud van de fractionele verkorting.49 Bij volwassenen die werden behandeld met hoge doses anthracyclines voorkwam enalapril daarentegen HF en verslechtering van parameters van de hartfunctie, zoals LVEF.50 Studies in angiotensine II type I receptor knock-out muizen toonden aan dat doxorubicine geen cardiotoxisch effect had in deze dieren en dat de toediening van ARB’s daunorobucine-geïnduceerde cardiomyopathie kan voorkomen.48 Hoewel er bij ons weten slechts twee gerandomiseerde onderzoeken naar ARB’s bij chemotherapiepatiënten zijn verricht, is aangetoond dat valsartan acute verlenging van het gecorrigeerde QT, linker ventrikel diastolische dilatatie en verhoging van het BNP gedurende één week chemotherapie voorkomt, hoewel het geen effect heeft op de LVEF,51 en dat telmisartan verlaging van de piekbelastingsfrequentie tijdens hoge-dosis anthracycline-therapie voorkomt.52 Verdere studies met een langere follow-up zijn nodig om deze effecten te bevestigen.
Statines
Statines hebben antioxiderende en ontstekingsremmende eigenschappen.53 Studies in diermodellen tonen aan dat fluvastatine de door anthracycline veroorzaakte cardiotoxiciteit vermindert door de oxidatieve stress te verminderen en de expressie van het antioxiderende enzym mitochondriaal superoxide dismutase 2 te verhogen, wat resulteert in verminderde hartontsteking.53 In één klinische studie waarin het effect werd beoordeeld van continue behandeling met statines bij patiënten met borstkanker die chemotherapie op basis van anthracycline kregen, hadden de patiënten die statines kregen een lagere incidentie van HF.54 In een andere studie bij patiënten met een voorheen normale LVEF die anthracycline-chemotherapie ondergingen, was de LVEF na zes maanden onveranderd bij degenen die met atorvastatine werden behandeld, vergeleken met een daling van 8% in de controlegroep.55
Ten slotte moet worden benadrukt dat er nog geen solide bewijs is voor de effectiviteit van farmacologische preventie van anthracycline-geïnduceerde cardiomyopathie, en dus blijft de belangrijkste preventieve strategie een grondige voorafgaande cardiovasculaire beoordeling van patiënten en een adequate monitoring, selectie en aanpassing van de chemotherapiedoseringen.
Behandeling van hartfalen
Na de ontwikkeling van tekenen of symptomen van HF of een afname van de LVEF als gevolg van chemotherapie-gerelateerde cardiotoxiciteit, moet de behandeling worden gebaseerd op de huidige richtlijnen.56 Hoewel de selectie van de beste therapie uiteraard belangrijk is, heeft één studie aangetoond dat de belangrijkste factor die bepalend is voor een succesvolle behandeling de tijd is tussen het einde van de chemotherapie en het begin van de HF-therapie, aangezien het onwaarschijnlijk is dat de LVEF zich volledig herstelt als deze langer is dan zes maanden.57
Vooruitzichten voor de toekomst
Er lopen momenteel verschillende klinische trials ter beoordeling van verschillende therapeutische strategieën, farmacologische en niet-farmacologische, voor de preventie van anthracycline-geïnduceerde cardiomyopathie (tabel 8). Het zal nog enige jaren duren voordat de resultaten bekend zijn, en er is nog steeds dringend behoefte aan op bewijsmateriaal gebaseerde richtsnoeren voor de beoordeling en klinische monitoring van deze patiënten.
Klinische onderzoeken naar de preventie van anthracycline-geïnduceerde cardiomyopathie.
| Hoofdauteur en ClinicalTrials.gov nr. | Type proef | Conditie | Chemotherapiemiddel(en) | Interventie | Nr. patiënten | Follow-up | Primaire uitkomstmaat | Geplande conclusie trial |
|---|---|---|---|---|---|---|---|---|
| Mavrudis D NCT01120171 |
Gerandomiseerd, fase 2 | borstkanker | Anthracyclines | Cyclophosphamide vs. liposoom-ingekapseld doxorubicine | 48 | 4 jaar | Overall response rate by CT or MRI | mei 2015 |
| Campbell K NCT02006979 |
Single blind, fase 2 | borstkanker | Anthracyclines | Een acute oefening 24 uur voorafgaand aan elke anthracycline-infusie | 24 | 1 jaar | GLS | December 2015 |
| Cipolla C NCT01968200 |
Gerandomiseerd, fase 3 | Kanker | Anthracyclines | Enalapril na optreden van hartschade vs. enalapril gelijktijdig met chemotherapie | 268 | Tot een jaar na voltooiing van chemotherapie | Cardiale troponinespiegels | juli 2016 |
| Virani S NCT01708798 |
Dubbelblind, fase 2, 3 | borstkanker | Anthracyclines | Eplerenon vs. placebo | 78 | 6 maanden | Verandering in LVDF | mei 2015 |
| Bocchi E NCT01724450 |
Double blind, fase 3 | Borstkanker | Anthracyclines | Carvedilol vs. placebo | 200 | 2 jaar | LVSD (10% reductie in LVEF) | oktober 2016 |
| Livi L NCT02236806 |
Single blind, fase 3 | borstkanker | Anthracyclines en trastuzumab | Bisoprolol vs. ramipril, bisoprolol vs. placebo, ramipril vs. placebo | 480 | 1 jaar | LVEF | November 2017 |
| Smith K NCT02096588 |
Gerandomiseerd, fase 2 | borstkanker | Anthracyclines | Simvastatine | 90 | 5 jaar | GLS | april 2021 |
CT: computertomografie; GLS: globale longitudinale rek; LVDF: linkerventrikel diastolische functie; LVEF: linkerventrikel ejectiefractie; LVSD: linkerventrikel systolische disfunctie; MRI: magnetische resonantie beeldvorming.
Conclusie
De langere overleving van patiënten die antikankertherapie ondergaan en de daaruit voortvloeiende toename van de incidentie van door anthracycline veroorzaakte cardiomyopathie maken het noodzakelijk de precieze mechanismen die tot nadelige cardiale effecten leiden, te onderzoeken en vast te stellen, teneinde deze te voorkomen. Verder onderzoek zal het mogelijk maken specifieke en gevalideerde preventieplannen op te stellen.
Belangenconflicten
De auteurs hebben geen belangenconflicten aan te geven.