CH3OH lub Metanol jest łatwopalną, bezbarwną i lotną cieczą, która ma charakterystyczny alkoholowy zapach. Badając jego metanol, można poznać kształt cząsteczki, kąt wiązania i polarność cząsteczki. Polarność CH3OH jest jedną z istotnych cech, ponieważ pomaga poznać inne właściwości związku, takie jak jego rozpuszczalność, ładunki elektryczne i wiele innych. Aby zrozumieć polarność metanolu, spójrzmy najpierw na kąty wiązań i układ atomów w cząsteczce CH3OH.

Kąty wiązań CH3OH
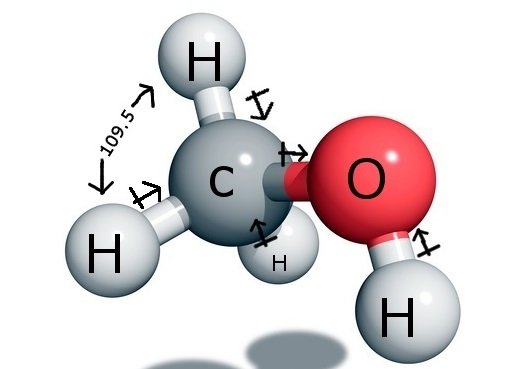
Środkowy atom węgla tworzy w związku cztery wiązania, trzy z atomem wodoru i jedno z grupą hydroksylową ( OH). A ponieważ ten atom węgla ma hybrydyzację sp3 i tworzy kształt czworościanu foremnego, ma kąty wiązania 109.5 stopni z jego atomów wiążących.
W przeciwieństwie do tego, tlen tworzy jedno wiązanie sigma, ale ma dwie samotne pary, więc jest pochylony w jego kąt wiązania z powodu sił odpychania pary wiązanej-jednej pary. To zmniejsza kąt wiązania do 104,5 stopnia.
Więc węgiel ma kąt wiązania 109,5 stopnia ze wszystkimi trzema atomami wodoru i kąt wiązania 104,5 stopnia z grupą hydroksylową.
Is CH3OH Polar?
Polaryzacja dowolnego związku zależy od momentu dipolowego netto na związek. Ten moment dipolowy netto może być znany poprzez zauważenie ładunków elektrycznych na atomach w cząsteczce. Tutaj oba atomy węgla i tlenu (które są uważane za centra geometryczne dla tego związku) w metanolu są elektronegatywnymi atomami. Ale tlen jest bardziej elektronegatywny niż węgiel lub wodór w związku.
CH3OH nie może być niepolarny, ponieważ istnieje różnica w ładunkach elektrycznych między atomami w cząsteczce metanolu. Tlen ma większą gęstość elektronową ze względu na jego dwie samotne pary elektronów. To powoduje dipol netto skierowany w stronę atomu tlenu, dzięki czemu CH3OH jest polarny.
Oprócz ładunków elektrycznych, cząsteczka CH3OH jest asymetryczna, co przekreśla możliwość niepolarności. Cząsteczka niepolarna ma budowę symetryczną, ponieważ moment dipolowy-dipolowy jest zniesiony. Ponieważ jednak metanol ma wygięty kształt, prowadzi to do powstania struktury asymetrycznej, w wyniku czego elektryczny moment dipolowy netto jest ujemnie skierowany w stronę atomu tlenu. Tak więc CH3OH jest cząsteczką polarną.
Teraz, gdy znamy polarność cząsteczki CH3OH, przejrzyjmy niektóre z jej właściwości fizycznych:
- Punkt wrzenia metanolu ( CH3OH) wynosi 64.7 °C.
- Punkt topnienia metanolu wynosi -97.6 °C.
- Ciężar cząsteczkowy Metanolu wynosi 32,04 g/mol.
- Jest to rozpuszczalnik polarny i jest również znany jako alkohol drzewny, ponieważ był kiedyś produkowany przez destylację drewna.
- Zapach tego związku jest po słodszej stronie w porównaniu do etanolu.
Użycia CH3OH
- Metanol jest również używany do produkcji węglowodorów i do syntezy innych związków chemicznych, takich jak formaldehyd.
- Jest używany jako środek przeciw zamarzaniu w rurach.
- CH3OH jest również używany jako dodatek do benzyny w kilku krajach ze względu na jego niską temperaturę topnienia.
- Związek ten jest również używany jako paliwo w spalaniu w silnikach wewnętrznych.
- Wiele firm farmaceutycznych używa czystego Metanolu do syntezy innych związków.
Mam nadzieję, że ten artykuł pomoże Ci zrozumieć polarność cząsteczki i jej właściwości fizyczne oraz zastosowania. CH3OH jest polarną cząsteczką, ponieważ moment dipolowy-dipolowy nie jest anulowany z powodu jego asymetrycznego kształtu.