INTRODUÇÃO
Apesar de progredir nas técnicas diagnósticas e cirúrgicas e nos cuidados pós-operatórios, a dissecção aguda da aorta tipo A continua associada a alta morbidade e mortalidade a curto e longo prazo. A mortalidade hospitalar atual tem sido estimada entre 15% e 35%, com sobrevida de 5 anos de 65%-75%.1-7
A alta incidência de AVC pós-operatório nestes pacientes (10%-20%)3,5,7,8 tem sido associada à proteção cerebral inadequada durante parada circulatória, eventos embólicos ou má perfusão devido ao fluxo preferencial através da falsa luz durante a perfusão utilizando a artéria femoral.9,10 Nos últimos anos, a introdução de novas técnicas de proteção cerebral, como a perfusão cerebral anterógrada seletiva e a canulação da artéria axilar, reduziu consideravelmente a incidência desta complicação.10-17
O objetivo deste estudo retrospectivo é descrever nossa experiência com a cirurgia de dissecção aguda da aorta tipo A – em relação à mortalidade hospitalar, à incidência de reintervenção e à sobrevida em longo prazo – e analisar a influência da proteção cerebral em nossos resultados.
METHODS
Entre março de 1990 e outubro de 2007, 98 pacientes consecutivos (79 homens e 19 mulheres) foram operados em nosso hospital para dissecção aguda da aorta tipo A. Dos pacientes diagnosticados e encaminhados para cirurgia (103) durante esse período, 5 foram excluídos; 2 pacientes por terem mais de 85 anos e os outros por apresentarem lesões cerebrais ou viscerais irreversíveis.
A mediana de idade foi de 59 anos. O sintoma mais freqüente na apresentação foi a dor torácica aguda. O diagnóstico foi confirmado através da aortografia no período inicial (18%), ecocardiografia transtorácica (76%), ecocardiografia transesofágica (66%) e tomografia computadorizada toracoabdominal (TC) (65%). Com exceção de 11 pacientes, onde foi realizado um único exame diagnóstico, todos os pacientes foram diagnosticados com 2 ou 3 destas técnicas de imagem em combinação (atualmente, o sistema diagnóstico empregado é a TC toracoabdominal com ou sem ecocardiografia transtorácica e a ecocardiografia transesofágica intra-operatória).
Um total de 91 (93%) pacientes foram submetidos a cirurgia de emergência (em 24 h) e os demais foram submetidos a cirurgia de urgência (nas 72 h seguintes ao diagnóstico).
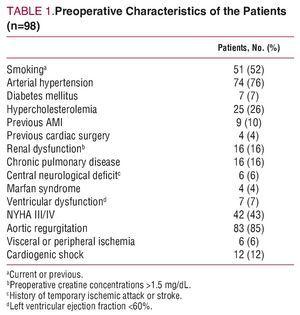
Os exames de imagem demonstraram regurgitação aórtica em 83 pacientes (55% com regurgitação severa). As características clínicas e demográficas pré-operatórias são apresentadas na Tabela 1.
>
Técnica Cirúrgica
>
Os conceitos básicos do procedimento cirúrgico envolvem a substituição da aorta ascendente ou arco aórtico, ressecção da laceração primária e preparação da anastomose distal durante a parada circulatória. Durante este período de 18 anos, tem havido evolução progressiva na estratégia cirúrgica empregada para esta patologia. Inicialmente, apenas a aorta ascendente foi ressecada com pinçamento da aorta sem parada circulatória. Em 1994, foi introduzida a anastomose distal com parada circulatória, que é a técnica atualmente utilizada em todos os pacientes, aplicando-se diferentes métodos de proteção cerebral. A perfusão cerebral anterógrada seletiva via artéria axilar foi recentemente introduzida como método de proteção cerebral durante a parada circulatória (Figura 1).
>
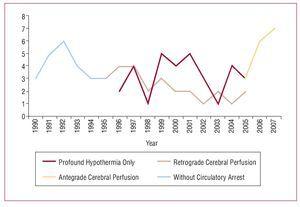 >
>Figure 1. Evolução da estratégia cirúrgica.
Foi realizada via esternotomia mediana, canulação da artéria femoral (82%), canulação da artéria axilar (16%), ou canulação do arco aórtico (2%), com retorno venoso através do átrio direito (85%) ou veia femoral (15%) e circulação extracorpórea. A temperatura corporal foi monitorizada através do esôfago e bexiga, e hipotermia profunda foi alcançada quando a temperatura da bexiga atingiu 18oC.
Após pinçamento aórtico, a aorta ascendente foi aberta longitudinalmente e transecção supracoronária realizada para localizar a laceração intimal, se houver, e para examinar a morfologia e o funcionamento da valva aórtica. Em seguida, em hipotermia profunda e parada circulatória, a aorta ascendente foi desobstruída e todo o arco aórtico examinado. Em 27% dos pacientes, a perfusão cerebral retrógrada foi adicionada através da veia cava superior (200-300 mL/min). Nos 16 pacientes em que foi realizada proteção cerebral anterógrada, foi utilizada a artéria axilar direita (10-15 mL/kg/min) e perfusão seletiva via artéria carótida esquerda em todos os pacientes.
A laceração primária foi identificada em 83 pacientes; localizou-se na raiz da aorta em 14%, a aorta ascendente em 67% e o arco aórtico em 19% dos pacientes. O segmento aórtico afetado pela laceração primária foi ressecado e substituído por um enxerto de dacron Hemashield (Boston Scientific, Massachusetts, EUA) anastomizado com sutura contínua de monofilamento 4/0 suportada por uma tira de pericárdio heterólogo e reforçando a aorta nativa proximal e distal com gelatino-resorcina-formaldeído (GRF, cola biológica; Laboratórios Cardial, Saint-Etienne, França). Durante nossa experiência inicial, a substituição do segmento aórtico foi realizada utilizando a técnica de inclusão (cobertura do tubo protético com a aorta nativa ressecada) em 21 pacientes. Atualmente, a técnica de interposição do enxerto é utilizada (substituição por prótese tubular com ressecção completa da aorta nativa).
A substituição da aorta ascendente foi realizada apenas em 61 (63%) pacientes, estendida à hemiarca em 24 (24%), e ao arco aórtico total em 13 (13%). Por hemiarca, referem-se os casos de ressecção parcial do arco, com anastomose apenas distal, sem necessidade de reimplante do tronco supra-aórtico. A tromba de elefante foi utilizada em 6 pacientes (durante a substituição total do arco aórtico, um segmento livre do tubo protético permanece na anastomose distal pendurado na aorta torácica descendente, o que facilita potenciais intervenções nesta área). A valva aórtica foi poupada pela ressuspensão das comissuras com suturas monofilamentares 4/0 suportadas por um retalho de teflon em 46 pacientes (47%), substituídas em 34 (35%) e reimplantadas em 1 (1%). Quando a valva aórtica precisou ser substituída, em 73% dos pacientes isto foi feito com enxerto valvar com reimplante das artérias coronárias utilizando a técnica de Bentall. O estado pré-operatório da valva aórtica está descrito na Tabela 2. Após a cirurgia, em casos de ressuspensão, a competência valvar foi objetivada através do ecocardiograma transesofágico intra-operatório em 84% dos pacientes, regurgitação leve em 13% e regurgitação moderada (II/IV) nos demais pacientes.

O tempo de circulação extracorpórea foi de 183 (58) min, tempo de isquemia, 113 (39) min e tempo de parada circulatória, 3 (23) min.
Um total de 24% dos pacientes, compreendendo a experiência inicial, não sofreu parada circulatória. Nos demais pacientes, o método de proteção cerebral utilizado foi hipotermia profunda em apenas 32 (33%) pacientes, perfusão cerebral retrógrada em 26 (27%) pacientes e perfusão anterógrada nos demais 16 (16%).
Seguimento
Todos os pacientes sobreviventes foram submetidos a exames clínicos e ecocardiográficos anuais, bem como exames de TC seriados para avaliação da aorta distal. Os dados clínicos foram obtidos através de entrevistas pessoais e telefônicas com os pacientes, familiares e médicos da atenção primária. Uma taxa de seguimento de 95% foi alcançada (79 pacientes).
Análise estatística
O programa estatístico SPSS (versão 14.0 para Windows) foi utilizado em todas as análises. Uma análise univariada foi realizada nas variáveis perioperatórias para determinar os fatores de risco estatisticamente significativos (P
RESULTADOS
Mortalidade hospitalar
A mortalidade hospitalar foi de 15% (15/98): 6 pacientes morreram devido a sangramento intra-operatório; 3, baixo débito cardíaco; 2, dano neurológico; 2, sepse; e 2, devido a falência multiorgânica pós-operatória. A Tabela 3 mostra as complicações pós-operatórias.
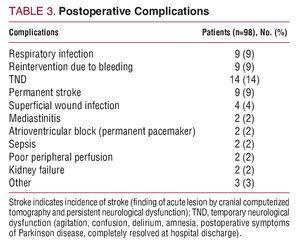
A análise univariada mostrou que a velhice, disfunção ventricular esquerda, choque cardiogênico, tempo de circulação extracorpórea >200 min, tempo de pinçamento aórtico >130 min e acidente vascular cerebral pós-operatório foram fatores de risco para mortalidade hospitalar (Tabela 4). Estas variáveis foram submetidas a análise multivariada que mostrou que a idade avançada (≥70 anos) (RR=2,85; P=,04) e o choque cardiogênico pré-operatório (RR=2,6; P=,025) foram identificados como preditores independentes de mortalidade hospitalar.

Disfunção neurológica pré-operatória e os primeiros anos de experiência (1990-1994) foram as únicas variáveis associadas às complicações neurológicas pós-operatórias (Tabela 4) na análise univariada, mas estas não alcançaram significância estatística na análise multivariada.
Mortalidade e complicações neurológicas específicas pós-operatórias (acidente vascular cerebral permanente e disfunção neurológica temporária) foram medidas entre os pacientes que sofreram parada circulatória e aqueles que não o fizeram e foram estratificados de acordo com o método de proteção cerebral utilizado (hipotermia profunda isolada ou em combinação com perfusão retrógrada ou anterógrada) (Tabela 5). Não foram encontradas diferenças estatisticamente significativas entre nenhum deles.

Follow-up
Uma taxa de seguimento de 95% (79 pacientes) foi alcançada, com mediana de 61 (variação, 1-204) meses. Após a alta hospitalar, todos os pacientes foram submetidos a exame ecocardiográfico aos 2 meses e anualmente, em seguida. Um total de 67% (56/83) dos pacientes foram submetidos a pelo menos 1 exame de TC. Dos 27 pacientes sobreviventes que não foram submetidos à TC, 17 recusaram o exame ou não compareceram, 4 foram perdidos para o estudo e 6 morreram durante o acompanhamento, 1 devido a uma causa aórtica conhecida (ruptura do aneurisma da aorta abdominal).
A tomografia computadorizada mostrou falsa luz persistente e patente na aorta distal em 71% dos pacientes, dos quais 17% apresentaram dilatação progressiva da aorta torácica e aorta abdominal.
Reintervenção
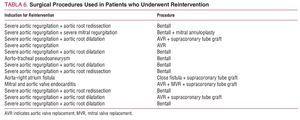
No total, 13 (16%) pacientes foram reintervenções durante o seguimento. As causas foram as seguintes: regurgitação aórtica grave e dilatação da raiz aórtica em 5 pacientes, regurgitação aórtica grave e redissecção da raiz aórtica em 3, regurgitação aórtica grave isolada em 1, regurgitação aórtica grave e mitral em 1, endocardite mitral e valvar aórtica em 1, pseudoaneurisma aorto-traqueal em 1 e fístula entre a raiz aórtica e o átrio direito em 1. Nenhum paciente foi submetido a reintervenção por doença da aorta descendente. Os procedimentos cirúrgicos aplicados são mostrados na Tabela 6. A mortalidade hospitalar foi de 23% (3/13), 2 pacientes morreram devido a sangramento intra-operatório e 1 devido a baixo débito cardíaco.
>
>
 >
>>
>
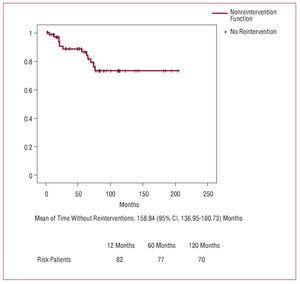
Figure 2. Curva de não intervenção
>
 >
>>
Sobrevivência a longo prazo
>
>
>
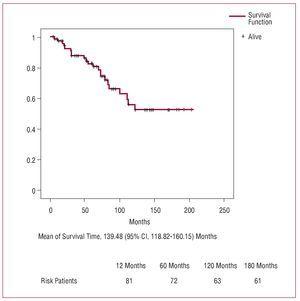
Figure 3. Curva de sobrevivência durante o seguimento (Kaplan-Meier).
>

A análise univariada mostrou a idade avançada (≥70 anos), a técnica de inclusão, o TND pós-operatório e a aplicação de métodos de proteção cerebral não anterógrados (Tabela 9) como preditores de mortalidade durante o seguimento. Na análise multivariada, o único preditor independente estatisticamente significativo de mortalidade durante o seguimento foi o não uso de proteção cerebral anterógrada (RR=3,1; P=,02).

DISCUSSÃO
A dissecção aguda da aorta tipo A é uma situação crítica que requer resposta clínica imediata e intervenção cirúrgica de emergência na maioria dos casos.
Siegal et al18 estimaram que, em pacientes não tratados, o risco de mortalidade aumenta em 1% a cada hora durante as primeiras 48 h e atinge 70% após 1 semana. Segundo dados do International Registry of Acute Aortic Syndrome (IRAD)1, a mortalidade entre os pacientes tratados de forma conservadora é de 58% contra 24% da mortalidade cirúrgica total.
Embora nos últimos anos tenham sido feitos grandes progressos nas técnicas diagnósticas e cirúrgicas e nos cuidados pós-operatórios, há uma variabilidade considerável na mortalidade hospitalar, variando entre 15 e 30%.2,3,19-21 Em nossa experiência, a mortalidade hospitalar foi de 15%, semelhante aos melhores resultados das séries atuais.4,22
Os preditores de mortalidade hospitalar coincidem com os da maioria das séries publicadas.2-4,21 Segundo dados do IRAD1, as variáveis independentes de mortalidade são idade avançada, hipotensão/choque, cardiopatia prévia e isquemia renal, mesentérica ou miocárdica pré-operatória. Estes resultados mostram que a mortalidade hospitalar está geralmente associada às características clínicas pré-operatórias dos pacientes e que são difíceis de serem modificadas. 1 demonstraram que pacientes instáveis têm uma mortalidade cirúrgica que é pelo menos o dobro dos pacientes estáveis (31,4% vs 16,7%). Esses achados revelam a importância da estabilidade hemodinâmica pré-operatória e enfatizam a necessidade de cirurgia de emergência antes do início da deterioração hemodinâmica.
Em nossa série, os únicos preditores independentes de mortalidade hospitalar foram idade avançada (≥70 anos) e choque cardiogênico pré-operatório.
A extensão da ressecção cirúrgica não foi identificada como fator de risco independente de mortalidade hospitalar; ressecções mais extensas com substituição do arco aórtico não afetaram os resultados precoces ou tardios. Outros autores, por outro lado, propuseram a ressecção exclusiva da aorta ascendente, argumentando que o risco envolvido em ressecções mais extensas supera o benefício potencial e que o objetivo principal da cirurgia é a sobrevida do paciente.5
A causa da lesão neurológica durante a cirurgia de dissecção da aorta é multifatorial, podendo levar a parada circulatória prolongada, eventos embólicos e má perfusão cerebral devido ao fluxo preferencial através da falsa luz.
As complicações neurológicas pós-operatórias são uma causa freqüente de morbidade e mortalidade na cirurgia de dissecção da aorta, com incidência estimada de 10%-20%.3,5,7,8
Ergin et al9 e Hagl et al10 apontam que o AVE pós-operatório causa principalmente eventos embólicos em uma possível associação com perfusão retrógrada da artéria femoral, mas não diretamente com o método de proteção cerebral utilizado, enquanto que o TND estaria associado com proteção cerebral inadequada. A perfusão cerebral anterógrada tem sido associada a uma redução significativa da TND em séries recentes,10,11,23,24 embora seu papel seja menos claro em relação à redução do AVE.
A perfusão cerebral anterógrada modificou o conceito de parada circulatória nesses pacientes porque, a rigor, a parada circulatória total não é realizada, visto que a perfusão cerebral contínua é mantida entre 500 mL/min e 1000 mL/min. Além disso, vários autores propuseram que hipotermia moderada (25oC) seria suficiente para proteger o cérebro e evitar os efeitos prejudiciais da hipotermia profunda.17,25,26 Entretanto, nosso grupo aplicou hipotermia profunda, pois esses reparos são complexos, espera-se que sejam de longa duração e porque esse método de resfriamento se mostrou muito eficaz na proteção do cérebro, assim como dos outros órgãos.17,27,28
A canulação da artéria axilar, em vez de femoral, reduz o risco de má perfusão visceral e cerebral, remobilização de trombos da aorta abdominal e torácica em direção ao cérebro e, além disso, redireciona o fluxo para o lúmen verdadeiro, diminui a chance de acúmulo de pressão excessiva ao pinçar a aorta e facilita a restauração da perfusão distal anterógrada.12-16 Todas estas vantagens parecem indicar que a perfusão cerebral anterógrada via artéria axilar, exceto quando esta é afetada por aterosclerose grave, é o método de escolha para a proteção cerebral.10,11,17
Em nossa série, a perfusão cerebral anterógrada utilizando a artéria axilar reduziu a incidência de TND para 6% e a mortalidade hospitalar para 6% nos últimos 16 pacientes operados, sugerindo, mas não demonstrando, seu papel na proteção contra as complicações neurológicas e sua concomitante morbidade e mortalidade. Possivelmente, esta falta de significância estatística deve-se ao baixo número de intervenções com perfusão anterógrada através da artéria axilar. Dada a raridade desta intervenção (
Em 10 anos, 73,3% dos pacientes não tinham sido submetidos a reintervenção e este resultado é semelhante aos publicados.3,4,6,29,30 A valva aórtica foi poupada sempre que possível e somente em casos de degeneração valvar, ectasia anularoaórtica ou cardiopatia valvular prévia foi decidido realizar a troca valvar sozinha ou com troca da raiz aórtica (técnica de Bentall), procedimento que não modificou a mortalidade hospitalar.
Em nossa série, 77% dos pacientes submetidos à reintervenção (13/78) necessitaram disso devido à regurgitação aórtica grave que anteriormente se apresentava e foi tratada conservadoramente por ressuspensão da valva durante a intervenção inicial. Regurgitação aórtica aguda pré-operatória e poupando a valva aórtica foram precisamente os fatores determinantes da reintervenção tardia da aorta, o que justificaria o manejo agressivo da valva aórtica durante o procedimento inicial.6,29 Hagl et al31 recomendaram a substituição sistemática da raiz e da valva aórtica (técnica de Bentall). 32 relataram um nível aceitável de durabilidade após poupar a valva aórtica; apontaram que uma possível reintervenção não deveria ditar o procedimento inicial e recomendaram poupar a valva aórtica para evitar a terapia anticoagulante crônica e seu possível papel na ausência de trombose da falsa luz.33
Consideramos que a apresentação inicial de regurgitação aórtica grave determina maior gravidade da dissecção, cuja origem ou extensão inclui a raiz aórtica e, portanto, o manejo agressivo com ressecção da raiz aórtica, ressecção valvar e implante de enxerto valvar (técnica de Bentall) deve ser o procedimento de escolha.4,6,29,31 Nesses casos, a ressuspensão valvar, ao poupar a raiz aórtica, deixa para trás um segmento intrinsecamente doente da aorta que apresenta maior risco de redissecção e complicações subseqüentes. Os resultados publicados sobre a técnica de substituição da raiz aórtica com reimplante da valva aórtica (técnica de David) são promissores e, embora seja necessária uma avaliação em longo prazo, ela pode se tornar uma opção interessante.33,34
Dos 56 pacientes que sobreviveram à alta hospitalar e foram submetidos à TC durante o acompanhamento, apenas em 6 (11%) foi evidente a dilatação progressiva em outras regiões da aorta com indicação cirúrgica: 2 pacientes com aneurisma de aorta abdominal, 2 com aneurisma toracoabdominal e 2 com aneurisma de aorta torácica descendente. Destes pacientes, 2 recusaram reintervenção e os outros tiveram alguma comorbidade (idade avançada, déficit neurológico grave, etc.) que impossibilitou o procedimento.
Tal baixa taxa de reintervenção da aorta distal deve-se provavelmente ao alto percentual de lacerações intimais primárias localizadas durante a intervenção e nossa decisão de ressecá-la em todos os casos. De facto, dos 15 pacientes em que a laceração intimal não foi encontrada, 60% (9 pacientes) eram membros do grupo que não sofreram paragem circulatória (o que impede o exame do arco aórtico e exclui as lacerações intimais a esse nível) e que apresentavam um risco acrescido de reintervenção próximo dos limites de significância estatística (P=,06). Assim, vários autores descrevem a ausência de ressecção da ruptura intimal durante a cirurgia inicial como o principal fator envolvido na reintervenção tardia para dilatação da aorta torácica ou abdominal.6,30
Embora nosso grupo não tenha experiência a esse respeito, alguns autores apontam que, em determinados casos, o implante de um stent na aorta torácica descendente durante o procedimento inicial ou um segundo poderia melhorar os resultados, diminuindo a incidência de reintervenção e o início das complicações decorrentes da progressão da doença para a a aorta distal.35,36
A curva atuarial de sobrevida após a alta hospitalar indica algumas porcentagens comparáveis às descritas por outros autores.2,3,5,6 A velhice é um dos fatores independentes de risco de mortalidade durante o acompanhamento na maioria das séries, em parte devido à baixa expectativa de vida neste grupo de pacientes.2 Em geral, há uma grande variabilidade na determinação dos preditores independentes de sobrevida a longo prazo. 2 descreveram uma série de 487 pacientes que foram submetidos a intervenção para dissecção da aorta tipo A e constataram que o único fator de risco era o diabetes pré-operatório. 3, em um grupo de 315 pacientes, identificaram a idade avançada e a diálise pós-operatória como preditores de mortalidade durante o seguimento.
Em nossa série, encontramos que o não uso de proteção cerebral anterógrada foi um preditor de mortalidade tardia, indicando que, embora a perfusão anterógrada não tenha modificado significativamente os resultados pós-operatórios iniciais, tem grande importância em relação à sobrevida tardia.
Ergin et al9 associaram a TND pós-operatória com comprometimento da função cerebral em longo prazo. 37 avaliaram a influência dos eventos neurológicos perioperatórios na mortalidade tardia, ou seja, os pacientes que sobreviveram à internação hospitalar devido a lesão neurológica tiveram piores taxas de sobrevida em longo prazo. Este fato pode ser explicado pelo alto risco de broncopneumonia, novos eventos neurológicos e outras complicações relacionadas à capacidade funcional reduzida destes pacientes.4
Limitações
Este artigo compartilha todas as limitações associadas aos estudos retrospectivos não-randomizados. A baixa incidência desta doença significa que poucos pacientes foram submetidos à intervenção, limitando assim o poder estatístico dos achados.
Como esta revisão abrange um longo período de experiência, os primeiros pacientes, que foram tratados sem parada circulatória, e os últimos pacientes, que foram tratados com perfusão cerebral anterógrada, não foram contemporâneos com os outros métodos de proteção cerebral mencionados. O último método (perfusão cerebral anterógrada) foi aplicado a uma amostra pequena (16 pacientes), limitando a significância estatística dos resultados.
CONCLUSÕES
A cirurgia de dissecção aguda da aorta produz resultados aceitáveis a curto e longo prazo e a intervenção de emergência deve ser indicada na maioria dos pacientes.
Regurgitação aguda da aorta está associada a um alto risco de reintervenção precoce e isto justificaria o manejo agressivo da valva aórtica durante a cirurgia inicial.
Perfusão cerebral anterógrada modificou o conceito de parada circulatória e melhorou o prognóstico a longo prazo entre estes pacientes. Consideramos que, embora seja necessária experiência com séries mais extensas, a aplicação da perfusão cerebral anterógrada na cirurgia de dissecção aguda da aorta poderia melhorar o prognóstico entre esses pacientes.
ABREVIATIONS
CT: tomografia computadorizada
TND: disfunção neurológica temporária