NervsystemetRedigera
Prenatal exponering av BaP hos råttor är känd för att påverka inlärning och minne i gnagermodeller. Dräktiga råttor som äter BaP har visat sig ha en negativ inverkan på hjärnfunktionen i det sena livet hos sin avkomma. Vid en tidpunkt då synapser först bildas och justeras i styrka av aktivitet, minskade BaP NMDA-receptorberoende nervcellsaktivitet mätt som mRNA-uttryck av NMDA NR2B-receptorunderenheten.
ImmunförsvarRedigera
BaP har en effekt på antalet vita blodkroppar, vilket hämmar en del av dem från att differentiera till makrofager, kroppens första försvarslinje för att bekämpa infektioner. År 2016 avslöjades den molekylära mekanismen som en skada på makrofagmembranets lipidflottintegritet genom att minska membrankolesterolet med 25 %. Detta innebär att färre immunreceptorer CD32 (en medlem av Fc-familjen av immunreceptorer) kunde binda till IgG och förvandla den vita blodcellen till en makrofag. Därför blir makrofagmembranen mottagliga för bakterieinfektioner.
ReproduktionssystemEdit
I experiment med hanråttor har subkronisk exponering för inhalerat BaP visat sig generellt minska funktionen hos testiklar och epididymis med lägre produktion av könssteroider/testosteron och spermieproduktion.
CarcinogenicitetEdit
BaP:s metaboliter är mutagena och mycket cancerframkallande, och det är listat som cancerframkallande ämne i grupp 1 av IARC. Chemical agents and related occupations, Volume 10, A review of Human Carcinogens, IARC Monographs, Lyon France 2009
I juni 2016 lades BaP som bensokrysen till i Reach Candidate List of Substances of very high concern for Authorisation.
Antaliga studier sedan 1970-talet har dokumenterat samband mellan BaP och cancer. Det har varit svårare att koppla cancer till specifika BaP-källor, särskilt hos människor, och svårare att kvantifiera riskerna med olika exponeringsmetoder (inandning eller intag). En koppling mellan A-vitaminbrist och emfysem hos rökare beskrevs 2005 som orsakad av BaP, som framkallar A-vitaminbrist hos råttor.
En studie från 1996 gav molekylära bevis för att komponenter i tobaksrök är kopplade till lungcancer. BaP visade sig orsaka genetiska skador i lungceller som var identiska med de skador som observerats i DNA i de flesta maligna lungtumörer.
Reguljär konsumtion av tillagat kött har epidemiologiskt sett förknippats med ökade nivåer av tjocktarmscancer (även om detta i sig självt inte bevisar cancerogenicitet).I en NCI-studie från 2005 konstaterades att en ökad risk för kolorektala adenom var förknippad med intag av BaP och i högre grad med intag av BaP från alla livsmedel. Livsmedlen i sig är dock inte nödvändigtvis cancerframkallande, även om de innehåller spår av cancerframkallande ämnen, eftersom mag-tarmkanalen skyddar sig mot cancer genom att kontinuerligt avlägsna sitt yttre skikt. Dessutom har avgiftningsenzymer, t.ex. cytokromer P450, ökad aktivitet i tarmen för att skydda mot livsmedelsburna toxiner. I de flesta fall metaboliseras därför små mängder BaP innan de överförs till blodet. Lungorna skyddas inte på något av dessa sätt.
Detoxifieringsenzymerna cytokrom P450 1A1 (CYP1A1) och cytokrom P450 1B1 (CYP1B1) är både skyddande och nödvändiga för bensopyrentoxicitet. Försök med musstammar som konstruerats för att avlägsna (knockout) CYP1A1 och CYP1B1 visar att CYP1A1 i första hand skyddar däggdjur från låga doser BaP och att avlägsnande av detta skydd leder till att stora koncentrationer av BaP ackumuleras. Om inte CYP1B1 också slås ut uppstår toxicitet genom bioaktivering av BaP till bensopyren-7,8-dihydrodiol-9,10-epoxid, den ytterst toxiska föreningen.
Interaktion med DNAEdit

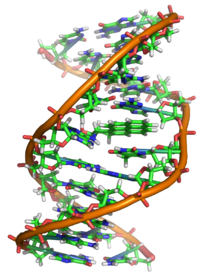
Enligt uppgift är BaP en prokarcinogen, vilket innebär att dess mekanism för karcinogenes beror på dess enzymatiska metabolism till BaP-diolepoxid. Den interkalerar i DNA, och den elektrofila epoxiden attackeras av nukleofila guaninbaser och bildar ett skrymmande guaninaddukt.

Studier av röntgenkristallografiska och kärnmagnetiska resonansstrukturer har visat hur denna bindning förvränger DNA:t genom att förvirra den dubbelhelikala DNA-strukturen. Detta stör den normala processen att kopiera DNA och orsakar mutationer, vilket förklarar förekomsten av cancer efter exponering. Denna verkningsmekanism liknar den för aflatoxin som binder till N7-positionen av guanin.
Det finns indikationer på att bensopyrendiollepoxid specifikt riktar sig mot den skyddande p53-genen. Denna gen är en transkriptionsfaktor som reglerar cellcykeln och därmed fungerar som en tumörsuppressor. Genom att inducera G (guanin) till T (tymidin) transversioner i transversionshotspots inom p53 finns det en sannolikhet för att bensopyrendiollepoxid inaktiverar den tumörundertryckande förmågan i vissa celler, vilket leder till cancer.
Benzopyren-7,8-dihydrodiol-9,10-epoxid är den cancerframkallande produkten av tre enzymatiska reaktioner:
- Benzopyren oxideras först av cytokrom P450 1A1 för att bilda en mängd olika produkter, inklusive (+)bensopyren-7,8-epoxid.
- Denna produkt metaboliseras av epoxidhydrolas, vilket öppnar epoxidringen för att ge (-)bensopyren-7,8-dihydrodiol.
- Den ultimata carcinogenen bildas efter ytterligare en reaktion med cytokrom P450 1A1 för att ge (+)bensopyren-7,8-dihydrodiol-9,10-epoxid. Det är denna diolepoxid som binder kovalent till DNA.
BaP inducerar cytokrom P4501A1 (CYP1A1) genom att binda till AHR (arylhydrokarbonreceptorn) i cytosolen. Vid bindning translokeras den transformerade receptorn till kärnan där den dimeriseras med ARNT (aryl hydrocarbon receptor nuclear translocator) och sedan binder xenobiotic response elements (XREs) i DNA som ligger uppströms vissa gener. Denna process ökar transkriptionen av vissa gener, särskilt CYP1A1, följt av en ökad produktion av CYP1A1-protein. Denna process liknar induktionen av CYP1A1 av vissa polyklorerade bifenyler och dioxiner. Det verkar som om CYP1A1-aktiviteten i tarmslemhinnan förhindrar att större mängder av intagen bensopyren kommer in i portalblodet och den systemiska cirkulationen. Intestinal, men inte hepatisk, expression av CYP1A1 är beroende av TOLL-liknande receptor 2 (TLR2), som är en eukaryotisk receptor för bakteriella ytstrukturer såsom lipoteikosyra.
För övrigt har BaP visat sig aktivera ett transposon, LINE1, hos människor.