CH3OH eller metanol är en brännbar, färglös och flyktig vätska som har en distinkt alkoholisk lukt. Genom att studera sin metanol kan man få reda på molekylens molekylform, bindningsvinkel och polaritet. Polariteten hos CH3OH är en av de viktigaste egenskaperna eftersom den hjälper till att känna till andra egenskaper hos föreningen, såsom dess löslighet, elektriska laddningar och mycket mer. För att förstå metanolens polaritet ska vi först titta på bindningsvinklarna och atomernas placering i CH3OH-molekylen.

CH3OH Bindningsvinklar
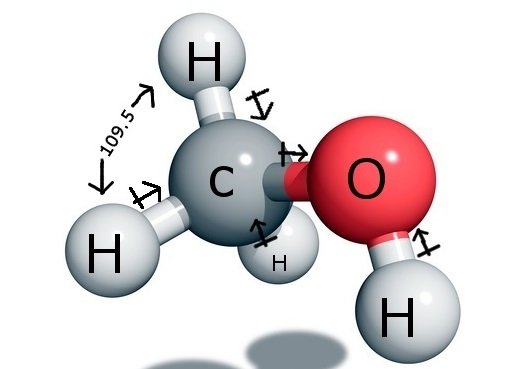
Den centrala kolatomen bildar fyra bindningar i föreningen, tre med väteatomen och en med hydroxyl ( OH) gruppen. Och eftersom denna kolatom har en sp3-hybridisering och bildar en tetraederform har den bindningsvinklar på 109,5 grader med sina bindningsatomer.
I kontrast till detta bildar syre en sigma-bindning men har två ensamma par, så det finns en böjning i dess bindningsvinkel på grund av bindningspar-lönepars repulsionskrafter. Detta minskar bindningsvinkeln till 104,5 grader.
Därmed har kolet en bindningsvinkel på 109,5 grader med alla de tre väteatomerna och en bindningsvinkel på 104,5 grader med hydroxylgruppen.
Är CH3OH polärt?
Polarisationen av en viss förening beror på nettodipolmomentet på föreningen. Detta nettodipolmoment kan man känna till genom att lägga märke till de elektriska laddningarna på atomerna i molekylen. Här är både kol- och syreatomerna (som betraktas som geometriska centra för denna förening) i metanol elektronegativa atomer. Men syre är mer elektronegativt än kol eller väte i föreningen.
CH3OH kan inte vara opolär eftersom det finns en skillnad i elektriska laddningar mellan atomerna i metanolmolekylen. Syre har mer elektrontäthet på grund av sina två ensamma elektronpar. Detta orsakar en nettodipol som pekar mot syreatomen, vilket gör CH3OH polärt.
Bortsett från de elektriska laddningarna är CH3OH-molekylen asymmetrisk, vilket upphäver möjligheten till opolaritet. En opolär molekyl har en symmetrisk struktur, eftersom dipol-dipolmomentet upphävs. Men eftersom det finns en böjning i metanolens form leder det till att det bildas en asymmetrisk struktur som resulterar i att det elektriska nettodipolmomentets negativa ände riktas mot syreatomen. CH3OH är alltså en polär molekyl.
När vi nu känner till CH3OH-molekylens polaritet, låt oss gå igenom några av dess fysikaliska egenskaper:
- Metanol ( CH3OH) har en kokpunkt på 64,7 °C.
- Metanolens smältpunkt är -97,6 °C.
- Metanolens molekylvikt är 32,04 g/mol.
- Det är ett polärt lösningsmedel och är även känt som träalkohol eftersom det en gång i tiden framställdes genom destillation av trä.
- Den här föreningens lukt är på den sötare sidan jämfört med etanol.
Användningar av CH3OH
- Metanol används också för framställning av kolväten och för syntes av andra kemikalier som formaldehyd.
- Det används som frysskydd i rör.
- CH3OH används också som tillsats i bensin i flera länder på grund av dess låga smältpunkt.
- Förbindelsen används också som bränsle vid förbränning i interna motorer.
- Många läkemedelsföretag använder ren metanol för syntes av andra föreningar.
Jag hoppas att den här artikeln hjälper dig att förstå molekylens polaritet och dess fysikaliska egenskaper och användningsområden. CH3OH är en polär molekyl eftersom dipol-dipolmomentet inte upphävs på grund av dess asymmetriska form.