Valvulär aortastenos (AS) är den vanligaste klaffsjukdomen i utvecklade länder. Diagnosen AS bekräftas klassiskt av ekokardiografi, som är standardverktyget för att upptäcka och bedöma sjukdomens svårighetsgrad (1). Bedömningen av svårighetsgraden av AS är dock fortfarande en utmaning. Svår AS definieras vanligen som medelgradient >40 mmHg, aortaklaffarea (AVA) <1 cm2 och topphastighet för aortastrålen >4,0 m/s (2). Ofta observeras dock diskrepanser mellan medelgradienten och klaffytan hos en enskild patient (3). Dessa diskrepanser är lätta att förstå hos patienter med låg hjärtminutvolym sekundärt till minskad LV-ejektionsfraktion, men kan också förekomma hos patienter med till synes bevarad LV-funktion (4). I den dagliga praktiken kan de potentiellt leda till en underskattning av stenos och symtomens svårighetsgrad och därmed till en olämplig fördröjning av aortaklaffbyte (AVR), vilket i sin tur kan ha en negativ inverkan på patientens resultat (5-7). I detta nummer av Cardiovascular Diagnosis and Therapy har OZKAN på ett elegant sätt gått igenom begreppet AS med låg gradient hos patienter med bevarad LV-funktion (8).
Ny klassificering av aortastenos
Nyligen har flera författare rapporterat att under samma benämning av allvarlig AS (AVA <1 cm2) kan flera entiteter identifieras som skiljer sig åt när det gäller transvalvulära flödeshastigheter och tryckgradienter som utvecklas (9-11). Pibarot et al. (5) var först med att understryka vikten av att integrera förhållandet mellan klaffgradient och flödesmönster, medan Miners et al. (3) var först med att tydligt visa på inkonsekvenserna när det gäller att gradera svårighetsgraden av AS och att tillsammans med Dumesnil et al. (6) föreslå den nya klassificeringen av AS. Hos patienter med en AVA <1 cm2 kan fyra kategorier av AS med flödesgradient identifieras: normalt flöde/låg gradient (NF/LG), normalt flöde/hög gradient (NF/HG), lågt flöde/hög gradient (LF/HG) och lågt flöde/låg gradient (LF/LG). LF definieras som en indexerad LV-slagvolym <35 mL/m2 och LG som en genomsnittlig trans-aortisk tryckgradient <40 mmHg (12).
Normalt flöde-låg gradient
Detta mönster observeras hos 31-38 % av patienterna och tycks identifiera en patientgrupp med en mindre allvarlig grad av AS – en inbyggd inkonsekvens som ingår i riktlinjerna – eller som har utsatts för sjukdomen under en kortare tidsperiod. Denna enhet kännetecknas av en bevarad longitudinell LV-myokardfunktion, vilket resulterar i lägre BNP-nivå och Monins riskpoäng (12,13). Prognosen för dessa patienter verkar vara relativt bevarad jämfört med de andra kategorierna.
Normalt flöde-hög gradient
Detta mönster representerar den mest förekommande entiteten (39-72 %) och överensstämmer helt med de kriterier som föreslås i riktlinjerna (4,5,12). Jämfört med NF/LG-gruppen är BNP högre än i NF/LG-gruppen, även om den longitudinella LV-funktionen är bevarad, och överlevnaden utan hjärthändelser är lägre i NF/HG-gruppen. Dessutom verkar patienter med NF/HG ha allvarligare AS, vilket tyder på en längre exponering för denna progressiva sjukdom. När de är symtomatiska hänvisas dessa patienter klassiskt till AVR, medan behandlingen av dessa patienter när de är asymtomatiska understryker behovet av optimerad riskstratifiering.
Lågt flöde-hög gradient
Detta mönster står för 8 % av patienterna med svår AS (4,12). Det kännetecknas av en indexerad LV-slagvolym <35 ml/m2 trots bevarad LV-ejektionsfraktion, en hög BNP-nivå och Monins riskpoäng samt en signifikant minskning av LV:s longitudinella funktion (14). Noterbart är att LV-ejektionsfraktion är en grov uppskattning av den systoliska LV-funktionen. LV-ejektionsfraktion påverkas både av intrinsikala myokardiella funktioner och av LV-hålans geometri. För en liknande omfattning av intrinsik myokardisk förkortning tenderar därför LV-utstötningsfraktionen att öka i förhållande till omfattningen av LV:s koncentriska remodellering. LV-utstötningsfraktionen kan därför markant underskatta omfattningen av den myokardiella funktionsnedsättningen vid förekomst av koncentrisk remodellering av LV, vilket i allmänhet är fallet hos AS-patienter. Det som är normalt för ett LV med normal geometri kan alltså vara onormalt för ett LV med koncentrisk remodellering. Dessutom kan minskningen av LV-produktionen (relaterad till inneboende myokardisk dysfunktion och betydande LV-remodellering) i sin tur resultera i lägre transvalvulära gradienter än förväntat. Utfallet för dessa patienter är nästan identiskt med patienter med NF/HG. När de är symtomatiska tenderar dessa patienter att ha en bättre överlevnad om de behandlas kirurgiskt.
Lågt flöde-låg gradient
Prevalensen av LF/LG-mönstret verkar vara lägre än vad som ursprungligen rapporterades. Denna enhet står för 7 % hos asymtomatiska patienter och upp till 15-35 % hos symtomatiska patienter (4-6,12,14). Detta mönster, nämligen paradoxalt lågflödes-AS, utgör en utmanande klinisk enhet som nyligen har betonats. Det är förknippat med mer uttalad LV-koncentrisk remodellering, mindre LV-hålighet, ökad global LV-efterbelastning, inneboende myokardiell dysfunktion, myokardfibros och en dyster prognos (12,15). Hos asymtomatiska patienter har vi visat att sannolikheten att förbli vid liv utan AVR efter tre år var fem gånger lägre än för NF/LG-mönstret och 4,3 gånger högre än i NF/HG-gruppen (12). Denna kliniska enhet är ofta feldiagnostiserad, vilket kan leda till en underskattning av AS svårighetsgrad och därmed till underutnyttjande eller olämplig fördröjning av kirurgi. Det är viktigt att känna igen denna entitet för att inte neka operation till en symtomatisk patient med liten AVA och LG.
Diskrepans mellan gradient och klaffarea
Potentiella orsaker till diskrepans mellan AVA och gradient hos patienter med bevarad LV-utkastningsfraktion är bland annat (I) mätfel, (II) liten kroppsstorlek, (III) paradoxalt AS med lågt flöde och (IV) inkonsekvent gradering som är relaterad till inneboende skillnader i kriterierna för riktlinjer (4,6,7,10,11). För det första kan patienter med liten kroppsstorlek och små LV-dimensioner uppvisa en lägre transvalvulär tryckgradient på grund av en lägre om än normal slagvolym. För det andra kan slagvolymen och därmed AVA underskattas på grund av att LV:s utflödeskanal underskattas och/eller att provvolymen för Doppler med pulsade vågor placeras fel. Flera metoder kan användas för att bekräfta de dopplerekokardiografiska mätningarna av slagvolym och AVA. I avsaknad av signifikant mitralregurgitation kan t.ex. slagvolymen lätt uppskattas med Simpsons metod (volymetrisk metod för att mäta LV:s ejektionsfraktion och volymer). Om den slagvolym som mäts med dessa oberoende metoder stämmer överens med den slagvolym som mäts i LV:s utflödeskanal kan man vara säker på att mätningen av slagvolymen är korrekt. För det tredje utgör paradoxal LF/LG en ny enhet där LF-tillståndet är resultatet av både LV:s koncentriska remodellering och minskad subendokardiell longitudinell funktion. Detta visar att det inte finns någon felaktig uppskattning av svårighetsgraden av AS. För det fjärde kan diskrepansen i förhållandet mellan gradient och ventilarea i vissa fall vara relaterad till inkonsekvenser i nuvarande riktlinjer. En harmonisering av definitionen av svår AS kan omklassificera vissa av dessa patienter med ”svår” AS till ”måttlig” AS. När man kombinerar de nuvarande prospektiva kliniska uppgifterna med tidigare hemodynamiska eko- och invasiva uppgifter verkar det som om en gradient på 40 mmHg stämmer bättre överens med en klaffyta på 0,8 cm2 medan en klaffyta på 1 cm2 relaterar till en genomsnittlig gradient på 26 mmHg (3,6,16). När det dessutom finns en diskrepans mellan klaffytan (i det allvarliga området) och gradienten (i det måttliga området) hos patienter med bevarad LV-ejektionsfraktion kan det krävas en mer omfattande ekokardiografisk dopplerutvärdering och eventuellt andra diagnostiska tester (BNP, kalciumpoäng med multislice datortomografi, ansträngnings-/dobutaminstressekokardiografi) för att bekräfta sjukdomens allvarlighetsgrad och vägleda den terapeutiska hanteringen.
Kliniska implikationer och hantering
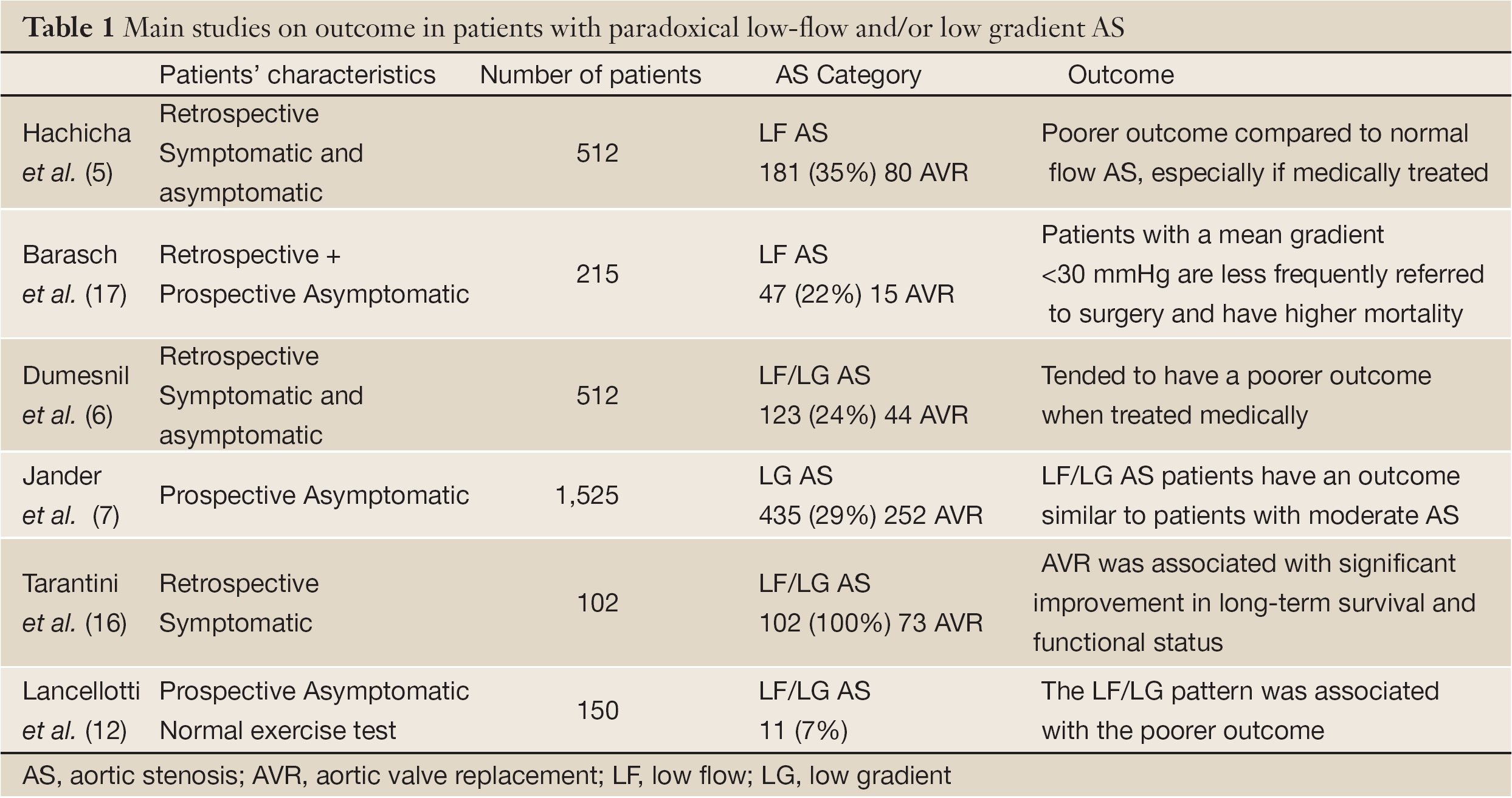
I den dagliga praktiken bör bedömningen av AS svårighetsgrad integrera flödesgradientmönstret till den klassiska mätningen av AVA. Som allmän regel utesluter en låg transvalvulär gradient (<40 mmHg) eller hastighet (<4 m/s) inte förekomsten av en allvarlig AS hos patienter med liten AVA och bevarad LV-ejektionsfraktion. Dessutom utesluter en bevarad LV-ejektionsfraktion (>50 %) inte förekomsten av myokardiell systolisk dysfunktion och lågt transvalvulärt flöde vid AS. Patienter med NF/LG AS har klassiskt sett ingen eller minimal subendokardiell dysfunktion och ett relativt välbevarat resultat. I denna NF/LG-kategori bör indikationen för AVR begränsas till patienter där symtomen tydligt kan hänföras till AS. I NF/HG-kategorin är AVR (kirurgiskt eller perkutant) den enda behandling som avsevärt förbättrar både överlevnad och symtom. När de är asymtomatiska kan individuell riskstratifiering hjälpa till att identifiera patienter som kan dra nytta av tidig kirurgi. I de andra kategorierna representerar LF-tillståndet ett vittne till inneboende myokardisk dysfunktion och en mer avancerad sjukdomsprocess. Symtomatiska patienter med LF/HG bör också gynnas av snabb AVR. När de är asymtomatiska bör individuell riskstratifiering också uppmuntras. Ekokardiografi vid ansträngning kan vara av intresse genom att avslöja patienter med begränsad ventilföljsamhet och/eller uttömd LV-kontraktilreserv (17,18). Paradoxal LF/LG ger ett dåligt resultat även hos asymtomatiska patienter. Även om nyttan av kirurgi inte är bevisad i denna kategori kan AVR troligen vara fördelaktigt hos utvalda symtomatiska patienter (7,19,20) (tabell 1). I klinisk praxis är det en utmaning att fastställa denna enhet. Innan man överväger kirurgi bör symtomen matchas med svårighetsgraden av AS. Hos patienter med låg risk kan AVR förespråkas. Hos högriskpatienter behövs ytterligare resultatstudier för att fastställa den lämpligaste modaliteten och tidpunkten för behandling.
Full Table
Acknowledgements
Upplysning: Författarna uppger att de inte har några intressekonflikter.
- Lancellotti P, Donal E, Magne J, et al. Riskstratifiering vid asymtomatisk måttlig till svår aortastenos: betydelsen av det valvulära, arteriella och ventrikulära samspelet. Heart 2010;96:1364-71.
- Bonow RO, Carabello BA, Kanu C, et al. ACC/AHA 2006 guidelines for the management of patients with valvular heart disease: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (skrivande kommitté för att revidera 1998 års riktlinjer för behandling av patienter med valvulär hjärtsjukdom): utvecklad i samarbete med Society of Cardiovascular Anesthesiologists: godkänd av Society for Cardiovascular Angiography and Interventions och Society of Thoracic Surgeons. Circulation 2006;114:e84-231.
- Minners J, Allgeier M, Gohlke-Baerwolf C, et al. Inkonsekvent klassificering av stenos i aortaklaffen enligt nuvarande riktlinjer: hemodynamiska studier hos patienter med till synes normal vänsterkammarfunktion. Heart 2010;96:1463-8.
- Adda J, Mielot C, Giorgi R, et al. Low-Flow, Low-Gradient Severe Aortic Stenosis Despite Normal Ejection Fraction Is Associated With Severe Left Ventricular Dysfunction as Assessed by Speckle-Tracking Echocardiography: En multicenterstudie. Circ Cardiovasc Imaging 2012;5:27-35.
- Hachicha Z, Dumesnil JG, Bogaty P, et al. Paradoxal low-flow, low-gradient severe aortic stenosis despite preserved ejection fraction is associated with higher afterload and reduced survival. Circulation 2007;115:2856-64.
- Dumesnil JG, Pibarot P, Carabello B. Paradoxal low flow och/eller low gradient severe aortic stenosis despite preserved left ventricular ejection fraction: implications for diagnosis and treatment. Eur Heart J 2010;31:281-9.
- Jander N, Minners J, Holme I, et al. Utfallet för patienter med ”svår” aortastenos med låg gradient och bevarad ejektionsfraktion. Circulation 2011;123:887-95.
- Ozkan A. Low gradient ”severe” aortic stenosis with preserved left ventricular ejection fraction. Cardiovasc Diagn Ther 2012;2:19-27.
- Dumesnil JG, Pibarot P, Akins C. New approaches to quantifying aortic stenosis severity. Curr Cardiol Rep 2008;10:91-7.
- Pibarot P, Dumesnil JG. Bedömning av aortastenosens svårighetsgrad: när gradienten inte stämmer överens med klaffområdet. Heart 2010;96:1431-3.
- Lancellotti P, Magne J. Valvuloarteriell impedans vid aortastenos: titta på belastningen, men glöm inte flödet. Eur J Echocardiogr 2011;12:354-7.
- Lancellotti P, Magne J, Donal E, et al. Clinical outcome in asymptomatic severe aortic stenosis insights from the new proposed aortic stenosis grading classification. J Am Coll Cardiol 2012;59:235-43.
- Monin JL, Lancellotti P, Monchi M, et al. Risk score for predicting outcome in patients with asymptomatic aortic stenosis. Circulation 2009;120:69-75.
- Lancellotti P, Donal E, Magne J, et al. Effekten av den globala vänsterkammarens efterbelastning på vänsterkammarens funktion vid asymtomatisk allvarlig aortastenos: en tvådimensionell speckle-tracking-studie. Eur J Echocardiogr 2010;11:537-43.
- Herrmann S, Störk S, Niemann M, et al. Low-gradient aortic valve stenosis myocardial fibrosis and its influence on function and outcome. J Am Coll Cardiol 2011;58:402-12.
- Zoghbi WA. Låggradig ”svår” aortastenos med normal systolisk funktion: dags att förfina riktlinjerna? Circulation 2011;123:838-40.
- Lancellotti P, Lebois F, Simon M, et al. Prognostic importance of quantitative exercise doppler echocardiography in asymptomatic valvular aortic stenosis. Circulation 2005;112:I377-82.
- Maréchaux S, Hachicha Z, Bellouin A, et al. Användbarheten av ansträngande ekokardiografi för riskstratifiering av asymtomatiska patienter med stenos i aortaklaffen. Eur Heart J 2010;31:1390-7.
- Tarantini G, Covolo E, Razzolini R, et al. Ventilbyte för svår aortastenos med låg transvalvulär gradient och vänsterkammarens ejektionsfraktion över 0,50. Ann Thorac Surg 2011;91:1808-15.
- Barasch E, Fan D, Chukwu EO, et al. Svår isolerad aortastenos med normal systolisk funktion i vänster kammare och låga transvalvulära gradienter: patofysiologiska och prognostiska insikter. J Heart Valve Dis 2008;17:81-8.