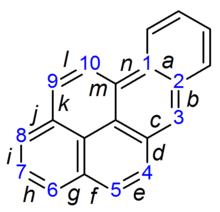
Sistema nervosoModifica
L’esposizione prenatale di BaP nei ratti è nota per influenzare l’apprendimento e la memoria nei modelli di roditori. È stato dimostrato che le ratte incinte che mangiano BaP influenzano negativamente la funzione del cervello nella tarda vita della loro prole. In un momento in cui le sinapsi sono formate per la prima volta e regolate in forza dall’attività, il BaP ha diminuito l’attività delle cellule nervose dipendenti dal recettore NMDA misurata come espressione dell’mRNA della subunità del recettore NMDA NR2B.
Sistema immunitarioModifica
Il BaP ha un effetto sul numero di globuli bianchi, inibendo alcuni di loro dal differenziarsi in macrofagi, la prima linea di difesa del corpo per combattere le infezioni. Nel 2016, il meccanismo molecolare è stato scoperto come danno all’integrità della zattera lipidica della membrana dei macrofagi diminuendo il colesterolo di membrana al 25%. Questo significa che meno immunorecettori CD32 (un membro della famiglia di immunorecettori Fc) potrebbero legarsi alle IgG e trasformare il globulo bianco in un macrofago. Pertanto, le membrane dei macrofagi diventano suscettibili alle infezioni batteriche.
Sistema riproduttivoModifica
In esperimenti con ratti maschi, è stato dimostrato che l’esposizione subcronica al BaP inalato riduce generalmente la funzione dei testicoli e dell’epididimo con una minore produzione di steroidi sessuali/testosterone e di sperma.
CarcinogenicitàModifica
I metaboliti del BaP sono mutageni e altamente cancerogeni, ed è elencato come cancerogeno del gruppo 1 dallo IARC. Chemical agents and related occupations, Volume 10, A review of Human Carcinogens, IARC Monographs, Lyon France 2009
Nel giugno 2016, il BaP è stato aggiunto come benzochrysene alla REACH Candidate List of Substances of very high concern for Authorisation.
Numerosi studi a partire dagli anni ’70 hanno documentato collegamenti tra BaP e tumori. È stato più difficile collegare i tumori a fonti specifiche di BaP, soprattutto negli esseri umani, e difficile quantificare i rischi posti dai vari metodi di esposizione (inalazione o ingestione). Un collegamento tra la carenza di vitamina A e l’enfisema nei fumatori è stato descritto nel 2005 per essere dovuto al BaP, che induce la carenza di vitamina A nei ratti.
Uno studio del 1996 ha fornito prove molecolari che collegano i componenti del fumo di tabacco al cancro ai polmoni. Il BaP ha dimostrato di causare danni genetici nelle cellule polmonari che erano identici ai danni osservati nel DNA della maggior parte dei tumori polmonari maligni.
Il consumo regolare di carni cotte è stato epidemiologicamente associato a un aumento dei livelli di cancro al colon (anche se questo di per sé non prova la cancerogenicità),Uno studio del 2005 del NCI ha trovato un aumento del rischio di adenomi colorettali è stato associato all’assunzione di BaP, e più fortemente con l’assunzione di BaP da tutti gli alimenti. Tuttavia, gli alimenti stessi non sono necessariamente cancerogeni, anche se contengono tracce di cancerogeni, perché il tratto gastrointestinale si protegge dai carcinomi spargendo continuamente il suo strato esterno. Inoltre, gli enzimi di disintossicazione, come i citocromi P450, hanno una maggiore attività nell’intestino per proteggersi dalle tossine di origine alimentare. Così, nella maggior parte dei casi, piccole quantità di BaP vengono metabolizzate prima di essere passate nel sangue. I polmoni non sono protetti in nessuno di questi modi.
Gli enzimi di detossificazione citocromo P450 1A1 (CYP1A1) e citocromo P450 1B1 (CYP1B1) sono entrambi protettivi e necessari per la tossicità del benzopirene. Esperimenti con ceppi di topi ingegnerizzati per rimuovere (knockout) CYP1A1 e CYP1B1 rivelano che CYP1A1 agisce principalmente per proteggere i mammiferi da basse dosi di BaP, e che la rimozione di questa protezione accumula grandi concentrazioni di BaP. A meno che anche il CYP1B1 sia eliminato, la tossicità deriva dalla bioattivazione del BaP a benzopirene -7,8-diidrodiolo-9,10-epoxide, il composto tossico per eccellenza.
Interazione con DNAEdit

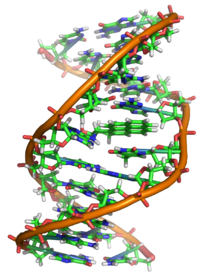
Propriamente parlando, il BaP è un procarcinogeno, il che significa che il suo meccanismo di carcinogenesi dipende dal suo metabolismo enzimatico a BaP diolo epossido. Si intercala nel DNA, e l’epossido elettrofilo viene attaccato dalle basi nucleofile della guanina, formando un voluminoso addotto di guanina.

Studi di struttura cristallografica a raggi X e risonanza magnetica nucleare hanno mostrato come questo legame distorca il DNA confondendo la struttura a doppia elica del DNA. Questo interrompe il normale processo di copiatura del DNA e causa mutazioni, il che spiega l’insorgenza del cancro dopo l’esposizione. Questo meccanismo d’azione è simile a quello dell’aflatossina che si lega alla posizione N7 della guanina.
Ci sono indicazioni che il benzopirene diolo epossido mira specificamente al gene protettivo p53. Questo gene è un fattore di trascrizione che regola il ciclo cellulare e quindi funziona come soppressore tumorale. Inducendo le trasversioni da G (guanina) a T (timidina) negli hotspot di trasversione all’interno di p53, è probabile che il benzopirene diolo epossido inattivi la capacità di soppressione del tumore in alcune cellule, portando al cancro.
Il benzopirene-7,8-diidrodiolo-9,10-epossido è il prodotto cancerogeno di tre reazioni enzimatiche:
- Il benzopirene viene prima ossidato dal citocromo P450 1A1 per formare una varietà di prodotti, compreso il (+)benzopirene-7,8-epossido.
- Questo prodotto viene metabolizzato dall’epossido idrolasi, aprendo l’anello epossidico per produrre (-)benzopirene-7,8-diidrodiolo.
- Il cancerogeno definitivo si forma dopo un’altra reazione con il citocromo P450 1A1 per produrre il (+)benzopirene-7,8-diidrodiolo-9,10-epoxide. È questo diolo epossido che si lega covalentemente al DNA.
BaP induce il citocromo P4501A1 (CYP1A1) legandosi all’AHR (aryl hydrocarbon receptor) nel citosol. Dopo il legame, il recettore trasformato si trasloca nel nucleo dove si dimerizza con ARNT (traslocatore nucleare del recettore degli idrocarburi arilici) e poi lega gli elementi di risposta xenobiotica (XRE) nel DNA situati a monte di alcuni geni. Questo processo aumenta la trascrizione di alcuni geni, in particolare CYP1A1, seguita da un aumento della produzione della proteina CYP1A1. Questo processo è simile all’induzione del CYP1A1 da parte di alcuni bifenili policlorurati e diossine. Apparentemente, l’attività del CYP1A1 nella mucosa intestinale impedisce a grandi quantità di benzopirene ingerito di entrare nel sangue portale e nella circolazione sistemica. L’espressione intestinale, ma non epatica, del CYP1A1 dipende dal recettore TOLL-like 2 (TLR2), che è un recettore eucariotico per le strutture di superficie dei batteri come l’acido lipoteico.
Inoltre, si è scoperto che il BaP attiva un trasposone, LINE1, negli esseri umani.