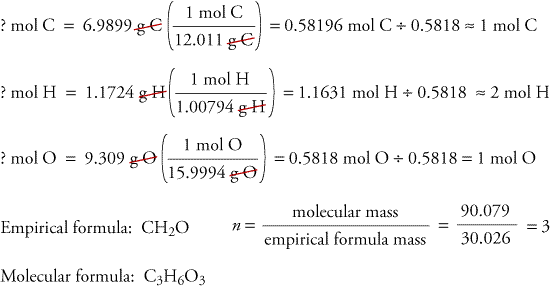Získání empirických a molekulových vzorců z údajů o spalování
Empirické a molekulové vzorce sloučenin, které obsahují pouze uhlík a vodík (CaHb) nebo uhlík, vodík a kyslík (CaHbOc), lze určit postupem zvaným analýza spalování. Kroky tohoto postupu jsou následující
Zvážíme vzorek analyzované sloučeniny a vložíme jej do přístroje znázorněného na obrázku níže.
Sloučeninu zcela spálíme. Jedinými produkty spalování sloučeniny, která obsahuje pouze uhlík a vodík (CaHb) nebo uhlík, vodík a kyslík (CaHbOc), jsou oxid uhličitý a voda.
H2O a CO2 se nasávají dvěma trubicemi. Jedna trubice obsahuje látku, která pohlcuje vodu, a druhá obsahuje látku, která pohlcuje oxid uhličitý. Zvažte každou z těchto trubic před a po spalování. Přírůstek hmotnosti v první trubici je hmotnost H2O, která vznikla při hoření, a přírůstek hmotnosti u druhé trubice je hmotnost vzniklého CO2.
Předpokládejte, že veškerý uhlík ve sloučenině byl přeměněn na CO2 a zachycen v druhé trubici. Vypočítejte hmotnost uhlíku ve sloučenině z hmotnosti uhlíku v naměřené hmotnosti vzniklého CO2.
Předpokládejte, že veškerý vodík ve sloučenině byl přeměněn na H2O a zachycen v první trubici. Vypočítejte hmotnost vodíku ve sloučenině z hmotnosti vodíku v naměřené hmotnosti vody.
Pokud sloučenina obsahuje kromě uhlíku a vodíku také kyslík, vypočítejte hmotnost kyslíku odečtením hmotnosti uhlíku a vodíku od celkové hmotnosti původního vzorku sloučeniny.
Použijte tyto údaje k určení empirického a molekulového vzorce obvyklým způsobem.
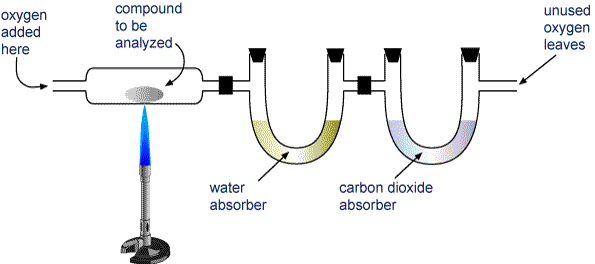
Přístroj pro analýzu spalování Sloučenina obsahující uhlík a vodík (CaHb) nebo uhlík, vodík a kyslík (CaHbOc) se zcela spálí za vzniku H2O a CO2. Produkty se nasávají přes dvě trubice. První trubice absorbuje vodu a druhá trubice absorbuje oxid uhličitý.
Pro ilustraci, jak lze z údajů získaných analýzou spalování určit empirické a molekulární vzorce, uvažujme látku zvanou trioxan. Formaldehyd, CH2O, je jako čistý plyn nestabilní a snadno vytváří směs látky zvané trioxan a polymeru zvaného paraformaldehyd. Proto se formaldehyd před prodejem a použitím rozpouští v rozpouštědle, například ve vodě. Molekulový vzorec trioxanu, kterýobsahuje uhlík, vodík a kyslík, lze určit pomocí údajů ze dvou různých experimentů. Při prvním pokusu se ve výše uvedeném přístroji spálí 17,471 g trioxanu a vznikne 10,477 g H2O a 25,612 gCO2. Při druhém experimentu byla zjištěna molekulová hmotnost trioxanu 90,079.
Molekulový vzorec sloučeniny můžeme získat z jejího empirického vzorce a molekulové hmotnosti. (Viz text, kde je připomenuto, jak se to dělá.) Abychom získali empirický vzorec, musíme určit hmotnost uhlíku, vodíku a kyslíku v gramech v 17,471 g trioxanu. Musíme tedy provést tyto obecné kroky:
První, přepočítejte z uvedených údajů na gramy uhlíku, vodíku a kyslíku.
Druhý, určete empirický vzorec z gramů uhlíku, vodíku a kyslíku.
Třetí, určete molekulový vzorec z empirického vzorce a dané molekulové hmotnosti.
Protože předpokládáme, že všechen uhlík v trioxanu zreagovalna vznik CO2, můžeme hmotnost uhlíku v 17,471 g trioxanu zjistit výpočtem hmotnosti uhlíku v 25,612 g CO2.

Protože předpokládáme, že veškerý vodík v trioxanu zreagoval za vzniku H2O,můžeme hmotnost vodíku v 17,471 g trioxanu zjistit výpočtem hmotnosti vodíku v 10. gramu trioxanu.477 g H2O.

Protože trioxan obsahuje pouze uhlík,vodík a kyslík, můžeme hmotnost kyslíku vypočítat tak, že od celkové hmotnosti trioxanu odečteme hmotnosti uhlíku a vodíku.
? g O = 17,471 g trioxanu – 6,9899 g C – 1,1724 g H = 9.
?309 g O
Nyní vypočítáme empirický vzorec, hmotnost empirického vzorce a molekulový vzorec.
Vzorový studijní list: Výpočet molekulových vzorců z údajů o spalování
Tip-off- Chcete vypočítat molekulový vzorec sloučeniny obsahující pouze uhlík a vodík (CaHb) nebo uhlík,vodík a kyslík (CaHbOc) a máte k dispozici její molekulovou hmotnost a hmotnosti CO2 a H2Ovzniklé při spalování dané hmotnosti sloučeniny.
Obecný postup
Vypočítejte počet gramů uhlíku ve sloučenině tak, že vypočtete počet gramů uhlíku v daném množství CO2.
Vypočítejte počet gramů vodíku ve sloučenině výpočtem počtu gramů vodíku v daném množství H2O.
Pokud sloučenina obsahuje kyslík, vypočtěte počet gramů kyslíku v ní odečtením hmotností uhlíku a vodíku od dané celkové hmotnosti sloučeniny.
? g O = (dané) g celkem – (vypočtené) g C – (vypočtené) g H
Vypočítejte empirický vzorec sloučeniny z gramů uhlíku, vodíku a kyslíku.
Vypočítejte hmotnost vzorce pro empirický vzorec a vydělte danou molekulovou hmotnost hmotností empirického vzorce, abyste získali n.
Vynásobte každý z dílčích indexů v empirickém vzorci n, abyste získali molekulový vzorec.
PŘÍKLAD – Získání molekulového vzorce z údajů o spalování:
Dianabol je jedním z anabolických steroidů, který někteří sportovci používají ke zvětšení velikosti a síly svých svalů. Je podobný mužskému hormonu testosteronu. Některé studie naznačují, že žádoucí účinky tohoto léku jsou minimální a vedlejší účinky, mezi které patří sterilita a zvýšené riziko rakoviny jater a srdečních onemocnění, brání většině lidí v jeho užívání. Molekulární vzorec Dianabol, který se skládá z uhlíku, vodíku a kyslíku, lze určit pomocí údajů ze dvou různých experimentů. Při prvním pokusu se spálí 14,765 g Dianabol a vznikne 43,257 g CO2 a 12,395 g H2O.Při druhém pokusu se zjistí, že molekulová hmotnost Dianabol je 300,44. Při druhém pokusu se zjistí, že molekulový vzorec je 300,44. Jaký je molekulový vzorec pro Dianabol?
Roztok:
.