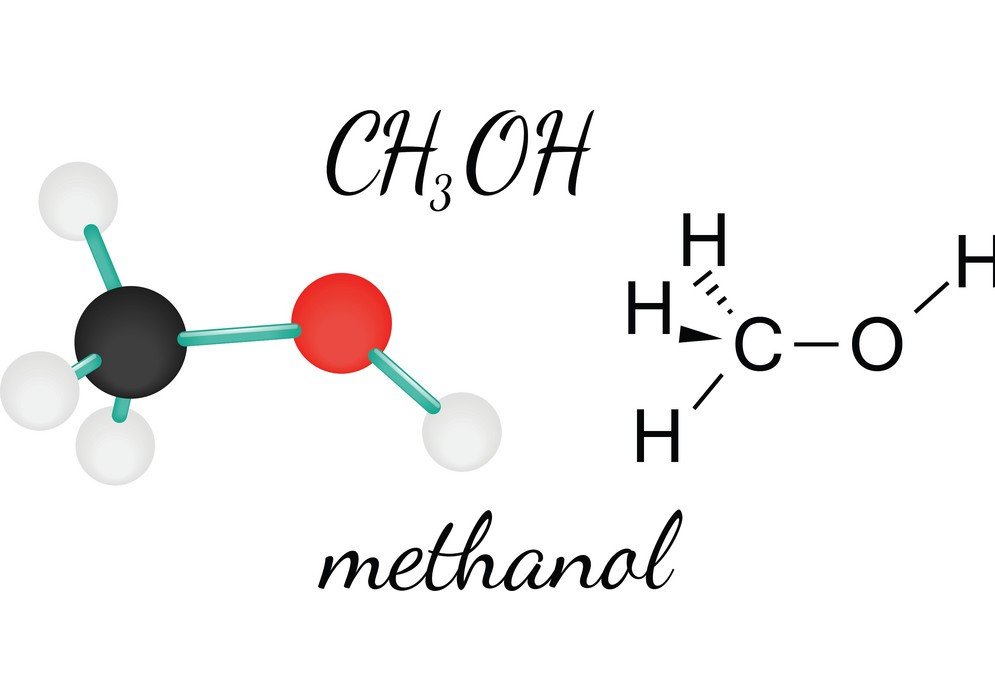
CH3OH neboli methanol je hořlavá, bezbarvá a těkavá kapalina, která má charakteristický alkoholový zápach. Zkoumáním jeho Methanolu lze poznat tvar molekuly, vazebný úhel a polaritu molekuly. Polarita CH3OH je jednou ze zásadních charakteristik, protože pomáhá při poznávání dalších vlastností sloučeniny, jako je její rozpustnost, elektrické náboje a mnoho dalších. Abychom pochopili polaritu methanolu, podívejme se nejprve na vazebné úhly a uspořádání atomů v molekule CH3OH.

Vazbové úhly CH3OH
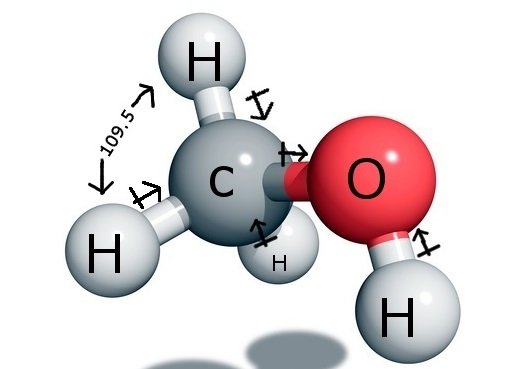
Střední atom uhlíku tvoří ve sloučenině čtyři vazby, tři s atomem vodíku a jednu s hydroxylovou ( OH) skupinou. A protože tento atom uhlíku má hybridizaci sp3 a tvoří tvar čtyřstěnu, má se svými vazebnými atomy vazebné úhly 109,5 stupně.
Naproti tomu kyslík tvoří jednu vazbu sigma, ale má dva osamělé páry, takže v jeho vazebném úhlu dochází k ohybu v důsledku sil odpuzování vazebných párů-osamělých párů. Tím se vazebný úhel sníží na 104,5 stupně.
Uhlík má tedy vazebný úhel 109,5 stupně se všemi třemi atomy vodíku a vazebný úhel 104,5 stupně s hydroxylovou skupinou.
Je CH3OH polární?
Polarita každé dané sloučeniny závisí na čistém dipólovém momentu na sloučenině. Tento čistý dipólový moment lze poznat tak, že si všimneme elektrických nábojů na atomech v molekule. Zde jsou oba atomy uhlíku a kyslíku ( které jsou považovány za geometrická centra této sloučeniny) v methanolu elektronegativní atomy. Kyslík je však ve sloučenině elektronegativnější než uhlík nebo vodík.
CH3OH nemůže být nepolární, protože mezi atomy v molekule metanolu je rozdíl elektrických nábojů. Kyslík má větší elektronovou hustotu díky svým dvěma osamělým párům elektronů. To způsobuje čistý dipól směřující k atomu kyslíku, takže CH3OH je polární.
Kromě elektrických nábojů je molekula CH3OH asymetrická, což ruší možnost nepolarity. Nepolární molekula má symetrickou strukturu, protože se ruší dipólový moment. Protože je však tvar methanolu ohnutý, vede to ke vzniku asymetrické struktury, což má za následek záporný konec čistého elektrického dipólového momentu směrem k atomu kyslíku. CH3OH je tedy polární molekula.
Teď, když známe polaritu molekuly CH3OH, projděme si některé její fyzikální vlastnosti:
- Teplota varu methanolu ( CH3OH) je 64,7 °C.
- Teplota tání methanolu je -97,6 °C.
- Molekulová hmotnost methanolu je 32,04 g/mol.
- Je to polární rozpouštědlo a je také známý jako dřevný alkohol, protože se kdysi vyráběl destilací dřeva.
- Vůně této sloučeniny je ve srovnání s ethanolem na sladší straně.
Použití CH3OH
- Methanol se také používá k výrobě uhlovodíků a k syntéze dalších chemických látek, například formaldehydu.
- Používá se jako nemrznoucí směs do potrubí.
- CH3OH se v několika zemích používá také jako přísada do benzinu díky nízkému bodu tání.
- Sloučenina se také používá jako palivo ve spalovacích motorech.
- Mnoho farmaceutických firem používá čistý metanol k syntéze dalších sloučenin.
Doufám, že vám tento článek pomůže pochopit polaritu molekuly a její fyzikální vlastnosti a použití. CH3OH je polární molekula, protože dipólový moment se díky jejímu asymetrickému tvaru neruší.