 Alle Materie, ob lebendig oder nicht, besteht aus chemischen Elementen; diese sind grundlegende Chemikalien in dem Sinne, dass sie sind, was sie sind – sie können nicht in ein anderes Element umgewandelt werden. Jedes Element zeichnet sich durch die Anzahl der Protonen
Alle Materie, ob lebendig oder nicht, besteht aus chemischen Elementen; diese sind grundlegende Chemikalien in dem Sinne, dass sie sind, was sie sind – sie können nicht in ein anderes Element umgewandelt werden. Jedes Element zeichnet sich durch die Anzahl der Protonen , Neutronen
, Neutronen und Elektronen
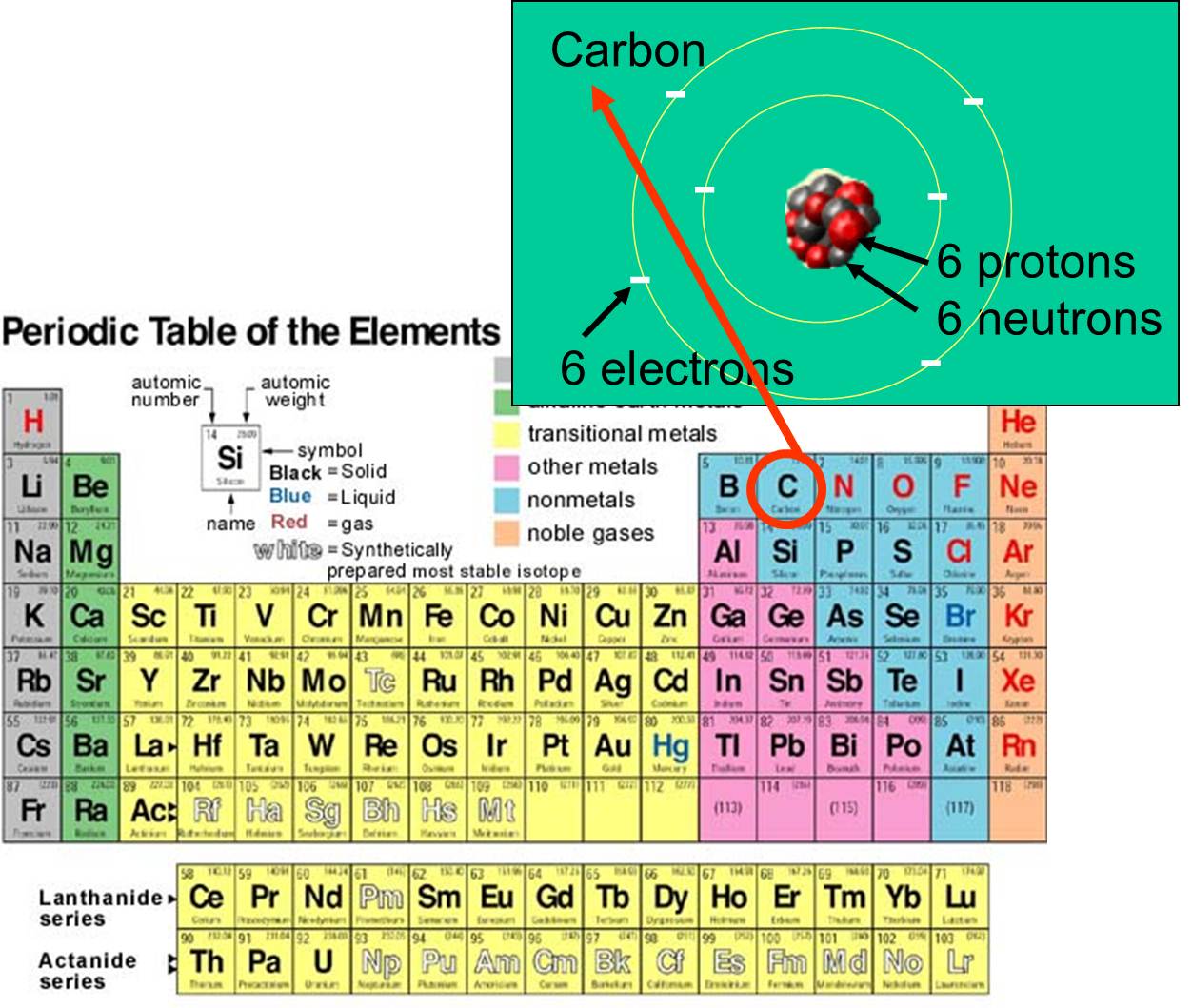
und Elektronen aus, über die es verfügt. Kohlenstoff zum Beispiel hat die Ordnungszahl 6 und eine Atommasse von etwa 12, weil er 6 positiv geladene Protonen und 6 ungeladene Neutronen hat. Die 6 geladenen Elektronen tragen nur wenig zur Atommasse bei. Es gibt 92 natürlich vorkommende Elemente auf der Erde. Die Anordnung der Elemente und ihre subatomare Struktur sind im rechts abgebildeten Periodensystem der Elemente zusammengefasst.
aus, über die es verfügt. Kohlenstoff zum Beispiel hat die Ordnungszahl 6 und eine Atommasse von etwa 12, weil er 6 positiv geladene Protonen und 6 ungeladene Neutronen hat. Die 6 geladenen Elektronen tragen nur wenig zur Atommasse bei. Es gibt 92 natürlich vorkommende Elemente auf der Erde. Die Anordnung der Elemente und ihre subatomare Struktur sind im rechts abgebildeten Periodensystem der Elemente zusammengefasst.
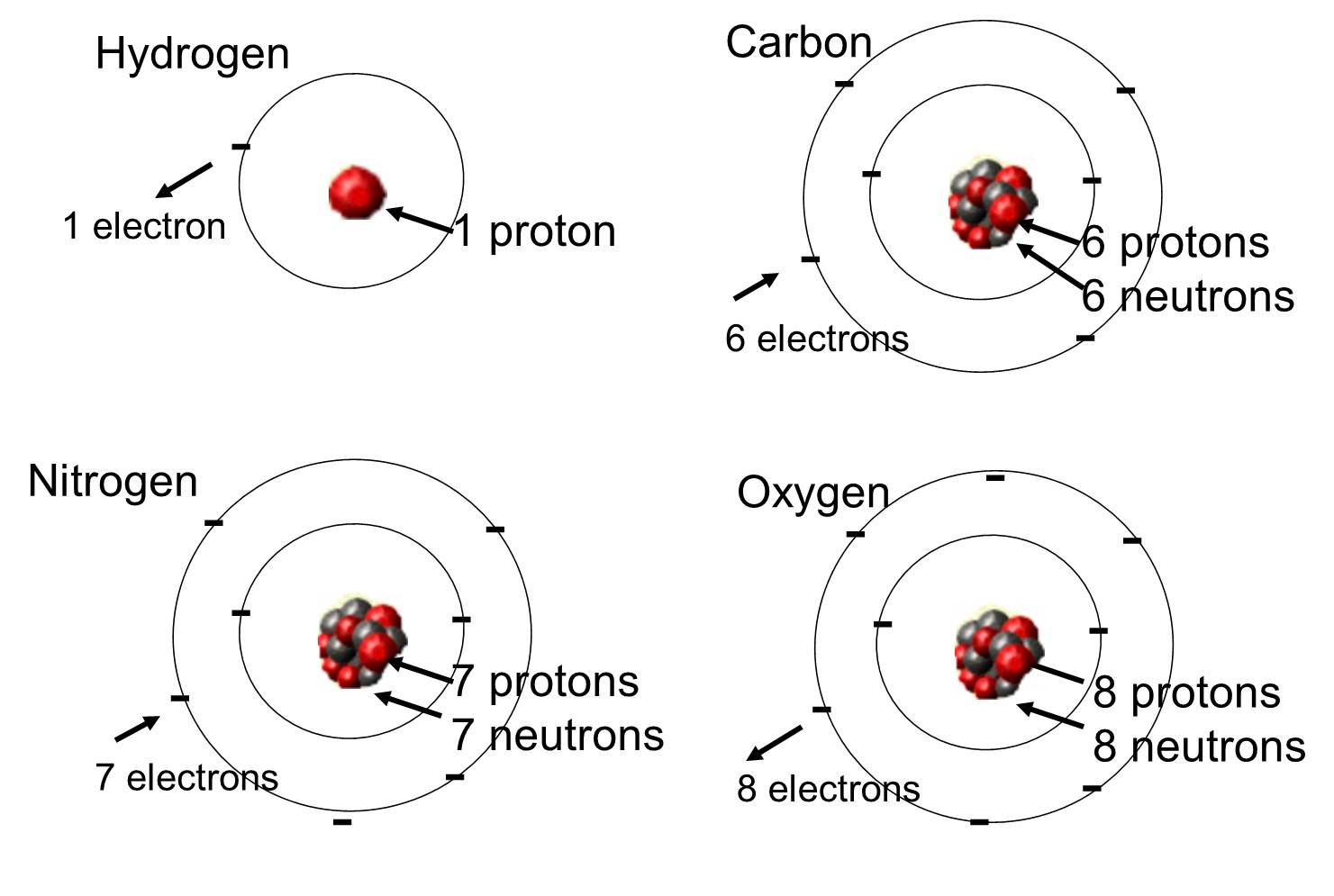
In lebenden Organismen sind die am häufigsten vorkommenden Elemente Kohlenstoff, Wasserstoff und Sauerstoff. Diese drei Elemente machen zusammen mit Stickstoff, Phosphor und einer Handvoll anderer Elemente den größten Teil der lebenden Materie aus. Ein Atom ist eine einzelne Einheit eines chemischen Elements. Einige dieser Elemente, die häufig in organischen Molekülen vorkommen, sind unten abgebildet.
 Atome können sich mit anderen Atomen verbinden, indem sie chemische Bindungen eingehen.
Atome können sich mit anderen Atomen verbinden, indem sie chemische Bindungen eingehen.
Kovalente Bindungen
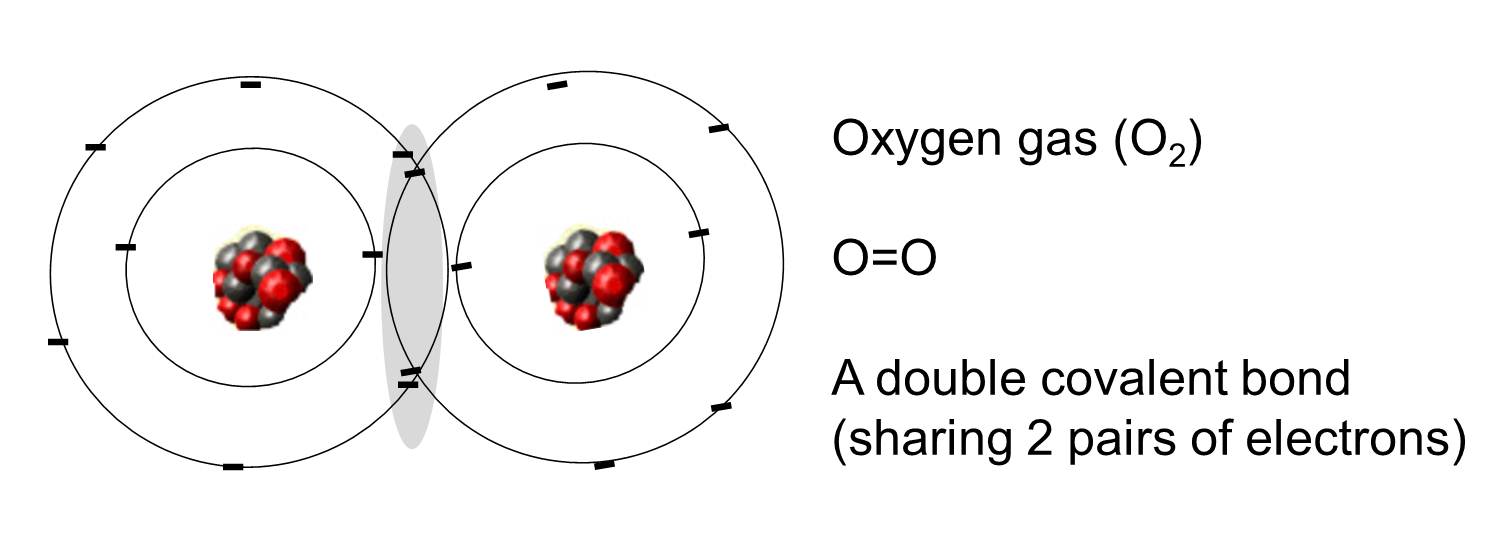
Eine kovalente Bindung ist eine Bindung, bei der ein oder mehrere Elektronenpaare von zwei Atomen gemeinsam genutzt werden. Die Abbildung rechts zeigt zwei Sauerstoffatome, die kovalent gebunden sind, indem sie sich zwei Elektronenpaare teilen, wie im schattierten Bereich dargestellt.
Die folgende Abbildung zeigt eine Reihe von Molekülen, die durch kovalente Bindung entstanden sind. Bewege die Maus über jedes Molekül, um eine kurze Beschreibung zu erhalten.
, 
Wasser ist ein polares Molekül
Beachte auch, dass die Elektronen nicht immer gleichmäßig verteilt sind. In einem Wassermolekül zum Beispiel halten sich die negativ geladenen Elektronen mehr in der Nähe des schwereren Sauerstoffatoms auf.
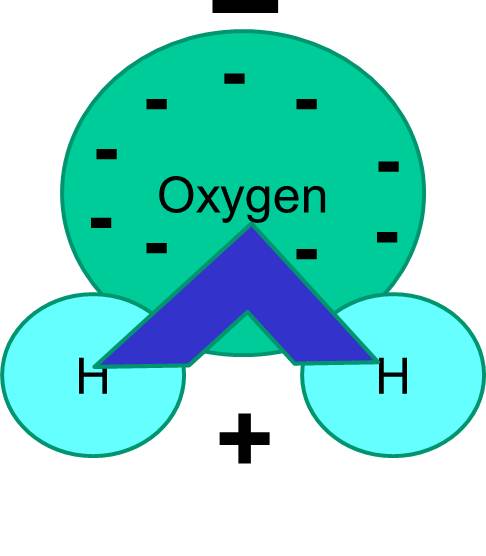
Das Ergebnis ist, dass ein Ende des Wassermoleküls im Vergleich zum anderen Ende negativer ist. Wasser ist also ein „polares“ Molekül. Wir werden sehen, dass diese Polarität wichtige Auswirkungen auf viele biologische Phänomene, einschließlich der Zellstruktur, hat. Vielleicht haben Sie schon einmal den Ausdruck „Gleiches löst sich gleich“ gehört. Damit ist gemeint, dass sich polare Moleküle gut in polaren Flüssigkeiten wie Wasser auflösen. Zucker (z. B. Glukose) und Salze sind polare Moleküle, und sie lösen sich in Wasser auf, weil sich die positiven und negativen Teile der beiden Molekülarten gut untereinander verteilen können.
Ionische Bindungen
Natrium hat ein einziges Elektron in seiner äußersten Orbitalschale und ist thermodynamisch stabiler, wenn es dieses Elektron abgibt. Dieser Verlust eines negativen Elektrons führt zu einem positiv geladenen Natriumion, abgekürzt Na+. Chlor hingegen hat sieben Elektronen in seiner äußersten Orbitalschale, und es ist thermodynamisch stabiler, wenn es ein zusätzliches Elektron erhält, um die äußere Orbitalschale zu vervollständigen. Das Ergebnis ist ein negativ geladenes Chlorid-Ion, abgekürzt Na+. Die positiv geladenen Natriumionen und die negativ geladenen Chloridionen ziehen sich gegenseitig an und bilden eine Ionenbindung. In Abwesenheit von Wasser bilden Natrium und Chlorid aufgrund der Anziehungskraft der negativen und positiven Ionen ein Kristallgitter.
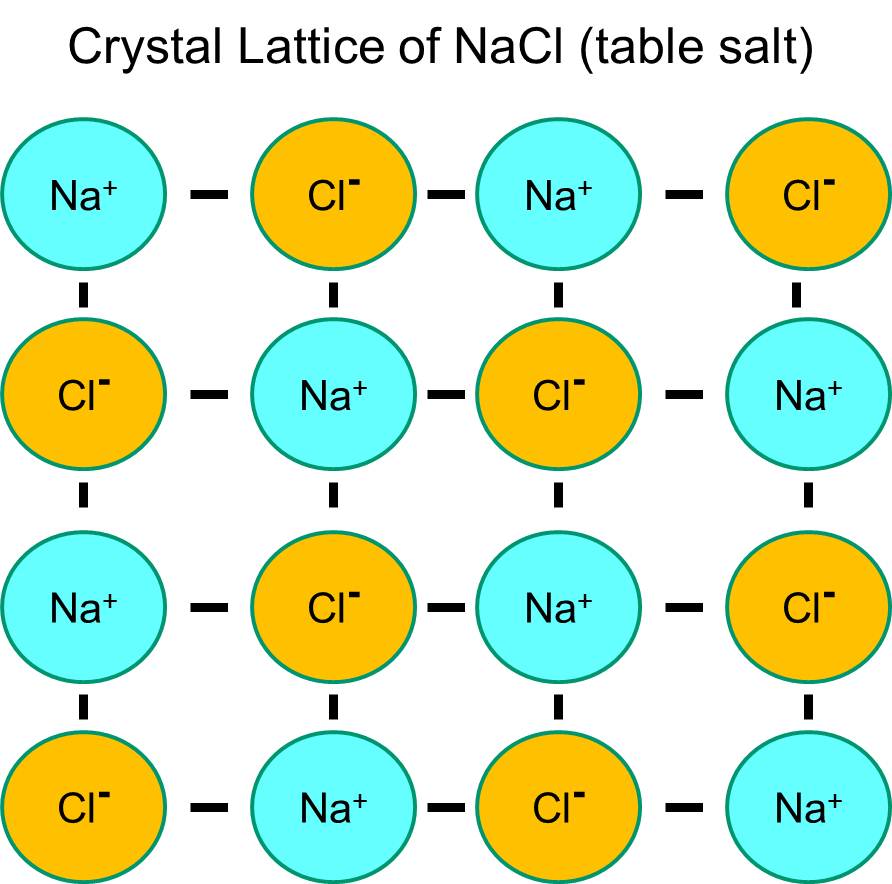
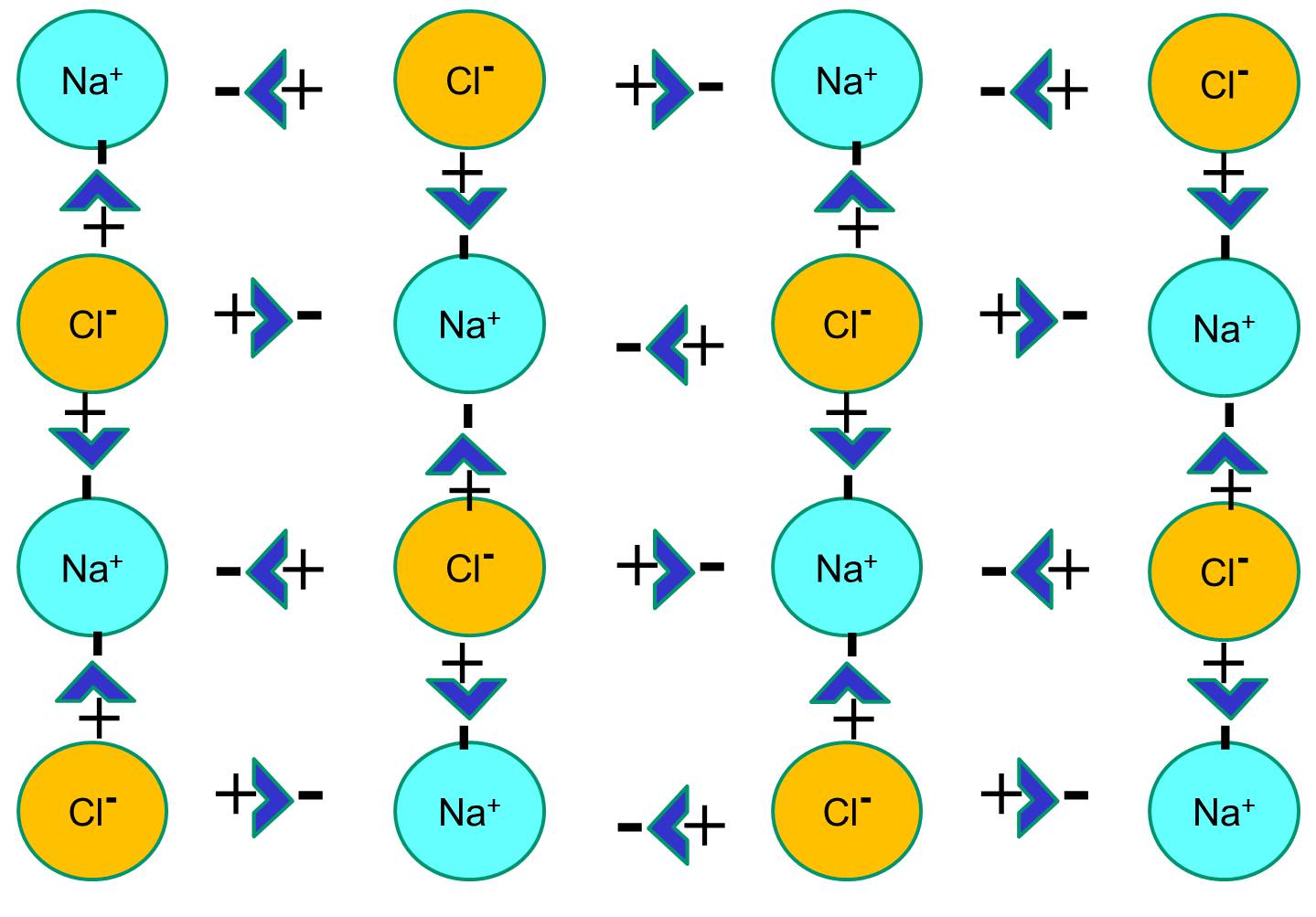
Wenn jedoch Natriumchloridkristalle in Wasser eingelegt werden, „hydratisieren“ die polaren Wassermoleküle die Natrium- und Chloridatome, da die Wassermoleküle polar sind. In der folgenden Abbildung stellen die dunkleren blauen V-förmigen Figuren polare Wassermoleküle dar. Die positiven Enden der Wassermoleküle werden von den negativ geladenen Chlorid-Ionen angezogen, während der negative Pol des Wassermoleküls von den positiven Natrium-Ionen angezogen wird. Infolgedessen werden die Ionen hydratisiert und das Kristallgitter löst sich in der wässrigen Lösung auf. Das ist genau das, was passiert, wenn man kristallines Kochsalz in ein Glas Wasser gibt.