La stenosi aortica valvolare (AS) è la malattia valvolare più frequente nei paesi sviluppati. La diagnosi di AS è classicamente confermata dall’ecocardiografia, lo strumento standard per individuare e valutare la gravità della malattia (1). Tuttavia, la valutazione della gravità dell’AS è ancora impegnativa. L’AS grave è solitamente definito come gradiente medio >40 mmHg, area della valvola aortica (AVA) <1 cm2 e velocità del getto aortico di picco >4,0 m/s (2). Tuttavia, si osservano spesso discrepanze tra il gradiente medio e l’area della valvola in un singolo paziente (3). Queste discrepanze sono facili da capire in pazienti con bassa gittata cardiaca secondaria a una ridotta frazione di eiezione del LV, ma possono verificarsi anche in pazienti con funzione LV apparentemente conservata (4). Nella pratica quotidiana, possono potenzialmente portare a una sottostima della stenosi e della gravità dei sintomi e quindi a un ritardo inappropriato della sostituzione della valvola aortica (AVR), che può, a sua volta, avere un impatto negativo sul risultato del paziente (5-7). In questo numero di Cardiovascular Diagnosis and Therapy, OZKAN ha elegantemente rivisto il concetto di AS a basso gradiente in pazienti con funzione LV conservata (8).
Nuova classificazione di classificazione della stenosi aortica
Di recente, diversi autori hanno riportato che sotto la stessa denominazione di AS grave (AVA <1 cm2), possono essere identificate diverse entità che differiscono in termini di velocità di flusso transvalvolare e gradienti di pressione sviluppati (9-11). Il primo a sottolineare l’importanza di integrare la relazione valvola-gradiente al pattern di flusso è stato il gruppo di Pibarot et al. (5), mentre Miners et al. (3) sono stati i primi a mostrare chiaramente le incongruenze per classificare la gravità della SA e a proporre con Dumesnil et al. (6) la nuova classificazione della SA. Nei pazienti con un’AVA <1 cm2, si possono identificare quattro categorie di AS con gradiente di flusso: flusso normale/basso gradiente (NF/LG), flusso normale/alto gradiente (NF/HG), basso flusso/alto gradiente (LF/HG) e basso flusso/basso gradiente (LF/LG). LF è definito come un LV stroke volume indicizzato <35 mL/m2 e LG come un gradiente medio di pressione trans-aortica <40 mmHg (12).
Flusso normale-basso gradiente
Questo modello è osservato nel 31-38% dei pazienti e sembra identificare un gruppo di pazienti con un grado meno grave di AS – incoerenza inerente contenuta nelle linee guida – o che è stato esposto alla malattia per un periodo di tempo più breve. Questa entità è caratterizzata da una conservata funzione miocardica longitudinale del LV, con conseguente minore livello di BNP e punteggio di rischio di Monin (12,13). La prognosi di questi pazienti sembra essere relativamente conservata rispetto alle altre categorie.
Flusso normale-alto gradiente
Questo modello rappresenta l’entità più prevalente (39-72%) ed è pienamente coerente con i criteri proposti dalle linee guida (4,5,12). Rispetto al gruppo NF/LG, anche se la funzione longitudinale del LV è conservata, il BNP è più alto e il tasso di sopravvivenza libera da eventi cardiaci di NF/HG è ridotto. Inoltre, i pazienti con NF/HG sembrano avere un’AS più grave, suggerendo un’esposizione più lunga a questa malattia progressiva. Quando sono sintomatici, questi pazienti vengono classicamente indirizzati all’AVR, mentre quando sono asintomatici, la gestione di questi pazienti sottolinea la necessità di ottimizzare la stratificazione del rischio.
Basso flusso-alto gradiente
Questo modello rappresenta l’8% dei pazienti con AS grave (4,12). È caratterizzato da un volume indicizzato di ictus LV <35 mL/m2 nonostante la frazione di eiezione LV conservata, un alto livello di BNP e il punteggio di rischio di Monin e una significativa riduzione della funzione longitudinale LV (14). Da notare che la frazione di eiezione di LV è una stima grezza della funzione sistolica di LV. La frazione di eiezione del LV è influenzata sia dalla funzione miocardica intrinseca che dalla geometria della cavità del LV. Quindi, per un simile grado di accorciamento miocardico intrinseco, la frazione di eiezione del LV tenderà ad aumentare in relazione all’entità del rimodellamento concentrico del LV. La frazione di eiezione del LV può quindi sottostimare notevolmente l’entità della compromissione miocardica in presenza di rimodellamento concentrico del LV, come avviene generalmente nei pazienti con AS. Quindi, ciò che è normale per un LV con geometria normale può essere anormale per un LV con rimodellamento concentrico. Inoltre, la riduzione della portata del LV (legata alla disfunzione miocardica intrinseca e al significativo rimodellamento del LV) può, a sua volta, risultare in gradienti trans-valvolari inferiori al previsto. L’esito di questi pazienti è quasi identico a quello dei pazienti con NF/HG. Quando sono sintomatici, questi pazienti tendono ad avere una migliore sopravvivenza se trattati chirurgicamente.
Basso flusso-basso gradiente
La prevalenza del modello LF/LG sembra essere inferiore a quanto riportato inizialmente. Questa entità rappresenta il 7% nei pazienti asintomatici e fino al 15-35% nei pazienti sintomatici (4-6,12,14). Questo pattern, cioè l’AS paradossale a basso flusso, rappresenta un’entità clinica impegnativa che è stata recentemente enfatizzata. È associato a un rimodellamento concentrico del LV più pronunciato, a una cavità LV più piccola, a un aumento del postcarico globale del LV, a disfunzioni miocardiche intrinseche, a fibrosi miocardica e a una prognosi infausta (12,15). Nei pazienti asintomatici, abbiamo dimostrato che la probabilità di rimanere in vita senza AVR a 3 anni era 5 volte inferiore rispetto al modello NF/LG e 4,3 volte superiore rispetto al gruppo NF/HG (12). Questa entità clinica è spesso mal diagnosticata, il che può portare a una sottostima della gravità della SA e quindi a un sottoutilizzo o a un ritardo inappropriato della chirurgia. È importante riconoscere questa entità per non negare la chirurgia a un paziente sintomatico con una piccola AVA e LG.
Discordanza tra gradiente e area valvolare
Le potenziali cause di discordanza tra AVA e gradiente in pazienti con frazione di eiezione LV conservata includono (I) errori di misurazione; (II) piccole dimensioni del corpo; (III) paradossale AS a basso flusso; e (IV) classificazione incoerente legata a discrepanze intrinseche nei criteri delle linee guida (4,6,7,10,11). Prima di tutto, i pazienti con dimensioni corporee e LV di piccole dimensioni possono presentare un gradiente di pressione trans-valvolare inferiore a causa di un volume di ictus inferiore, anche se normale. In secondo luogo, il volume di ictus e quindi l’AVA può essere sottostimato a causa della sottostima del tratto di efflusso del LV e/o errato posizionamento del volume di campione Doppler a onde pulsate. Diversi metodi possono essere utilizzati per corroborare le misure Doppler-ecocardiografiche di stroke volume e AVA. Ad esempio, in assenza di significativo rigurgito mitralico, il volume di ictus può essere facilmente stimato dal metodo di Simpson (metodo volumetrico per misurare la frazione di eiezione LV e volumi). Se il volume di ictus misurato da questi metodi indipendenti è coerente con il volume di ictus misurato nel tratto di efflusso del LV, si può essere rassicurati circa l’accuratezza della misurazione del volume di ictus. In terzo luogo, la LF/LG paradossale rappresenta una nuova entità in cui lo stato LF deriva sia dal rimodellamento concentrico del LV che dalla ridotta funzione longitudinale subendocardica. Questo delinea l’assenza di una stima errata della gravità dell’AS. In quarto luogo, in alcuni casi, la discrepanza nel rapporto gradiente-area valvolare può essere legata alle incongruenze delle attuali linee guida. Un’armonizzazione della definizione di AS grave può riclassificare alcuni di questi pazienti con AS “grave” in AS “moderata”. Quando si combinano gli attuali dati clinici prospettici con precedenti dati emodinamici eco e invasivi, sembra che un gradiente di 40 mmHg si adatti maggiormente a un’area valvolare di 0,8 cm2 , mentre un’area valvolare di 1 cm2 si riferisce a un gradiente medio di 26 mmHg (3,6,16). Inoltre, quando c’è una discordanza tra l’area valvolare (nel range grave) e il gradiente (nel range moderato) in pazienti con frazione di eiezione LV conservata, una valutazione ecocardiografica Doppler più completa e potenzialmente altri test diagnostici (BNP, punteggio di calcio da tomografia computerizzata multislice, ecocardiografia da sforzo/dobutamina) possono essere necessari per confermare la gravità della malattia e guidare la gestione terapeutica.
Implicazioni cliniche e gestione
Nella pratica quotidiana, la valutazione della gravità dell’AS dovrebbe integrare il pattern flusso-gradiente alla classica misurazione dell’AVA. Come regola generale, un basso gradiente trans-valvolare (<40 mmHg) o velocità (<4 m/s) non esclude la presenza di un grave AS in pazienti con piccola AVA e frazione di eiezione LV conservata. Inoltre, una frazione di eiezione LV conservata (>50%) non esclude la presenza di disfunzione miocardica sistolica e di un basso flusso trans-valvolare nell’AS. I pazienti con NF/LG AS hanno classicamente nessuna o minima disfunzione subendocardica e un esito relativamente conservato. In questa categoria NF/LG, l’indicazione all’AVR dovrebbe essere limitata ai pazienti in cui i sintomi possono essere chiaramente attribuiti all’AS. Nella categoria NF/HG, l’AVR (chirurgica o percutanea) è l’unica terapia che migliora significativamente sia la sopravvivenza che i sintomi. Quando sono asintomatici, la stratificazione del rischio individuale può aiutare a identificare i pazienti che possono beneficiare di un intervento chirurgico precoce. Nelle altre categorie, lo stato LF rappresenta una testimonianza di disfunzione miocardica intrinseca e un processo di malattia più avanzato. Anche i pazienti sintomatici con LF/HG dovrebbero beneficiare di una rapida AVR. Quando sono asintomatici, dovrebbe essere incoraggiata anche la stratificazione del rischio individuale. L’ecocardiografia da sforzo può essere interessante per smascherare i pazienti con compliance valvolare limitata e/o riserva contrattile di LV esaurita (17,18). La LF/LG paradossale trasmette un cattivo esito anche nei pazienti asintomatici. In questa categoria, anche se il beneficio della chirurgia non è dimostrato, l’AVR può probabilmente essere utile in pazienti sintomatici selezionati (7,19,20) (Tabella 1). Nella pratica clinica, accertare questa entità è impegnativo. Prima di considerare l’intervento chirurgico, i sintomi dovrebbero essere abbinati alla gravità della SA. Nei pazienti a basso rischio, l’AVR può essere raccomandata. Nei pazienti ad alto rischio, sono necessari ulteriori studi di outcome per determinare la modalità più appropriata e la tempistica del trattamento.
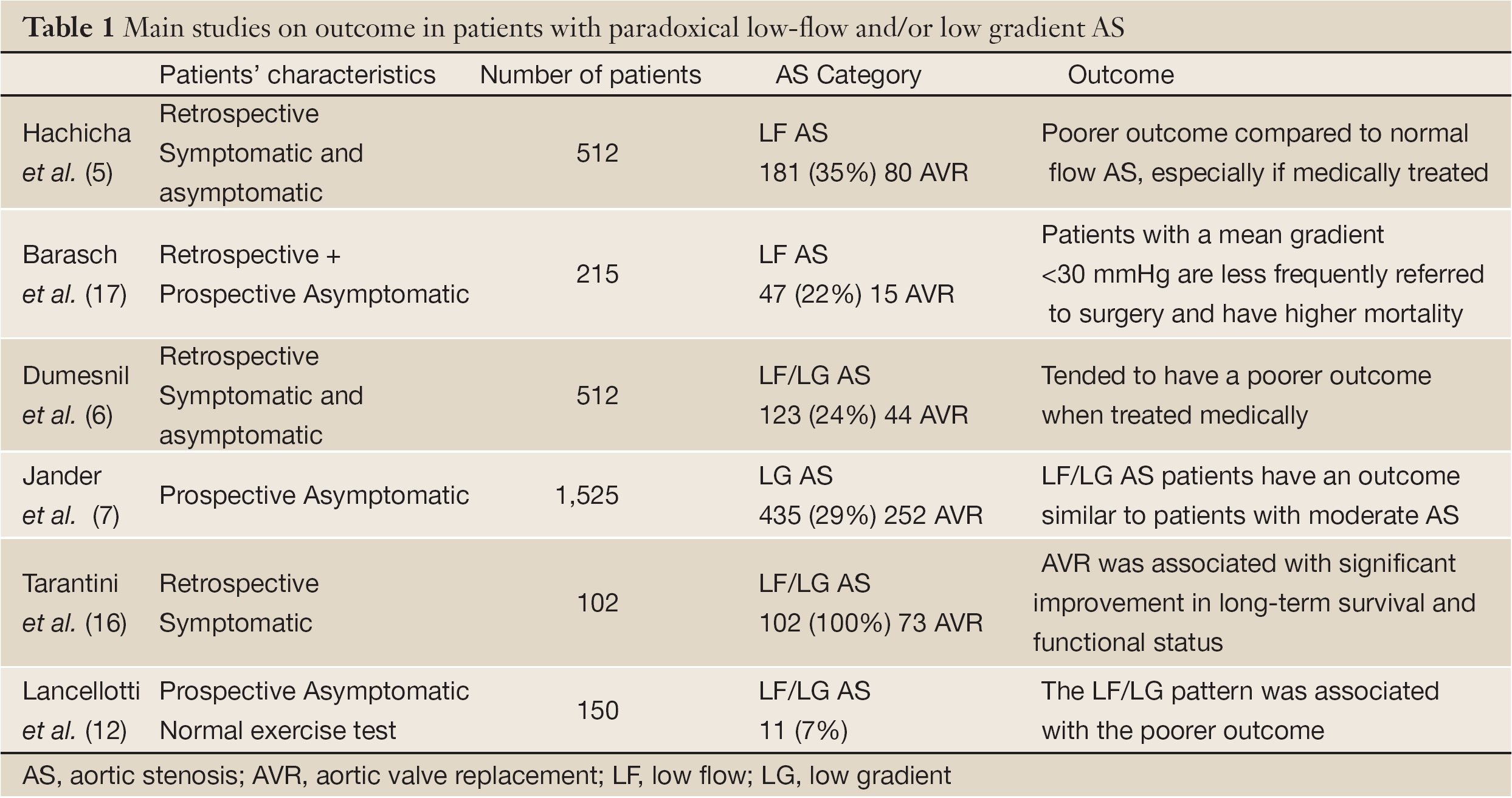
Tabella completa
Riconoscimenti
Disclosure: Gli autori non dichiarano alcun conflitto di interessi.
- Lancellotti P, Donal E, Magne J, et al. stratificazione del rischio nella stenosi aortica asintomatica moderata e grave: l’importanza dell’interazione valvolare, arteriosa e ventricolare. Cuore 2010;96:1364-71.
- Bonow RO, Carabello BA, Kanu C, et al. ACC/AHA 2006 linee guida per la gestione dei pazienti con cardiopatia valvolare: un rapporto dell’American College of Cardiology/American Heart Association Task Force on Practice Guidelines (comitato di scrittura per rivedere le linee guida del 1998 per la gestione dei pazienti con cardiopatia valvolare): sviluppato in collaborazione con la Society of Cardiovascular Anesthesiologists: approvato dalla Society for Cardiovascular Angiography and Interventions e la Society of Thoracic Surgeons. Circolazione 2006;114:e84-231.
- Minners J, Allgeier M, Gohlke-Baerwolf C, et al. Inconsistente classificazione di stenosi della valvola aortica da linee guida attuali: studi emodinamici in pazienti con funzione ventricolare sinistra apparentemente normale. Heart 2010;96:1463-8.
- Adda J, Mielot C, Giorgi R, et al. Low-Flow, Low-Gradient grave stenosi aortica nonostante frazione di eiezione normale è associato con grave disfunzione ventricolare sinistra come valutato da Speckle-Tracking ecocardiografia: Uno studio multicentrico. Circ Cardiovasc Imaging 2012;5:27-35.
- Hachicha Z, Dumesnil JG, Bogaty P, et al. Paradossale stenosi aortica grave a basso flusso e basso gradiente nonostante frazione di eiezione conservata è associata ad un postcarico più elevato e ridotta sopravvivenza. Circulation 2007;115:2856-64.
- Dumesnil JG, Pibarot P, Carabello B. Stenosi aortica grave paradossale a basso flusso e/o basso gradiente nonostante frazione di eiezione ventricolare sinistra conservata: implicazioni per la diagnosi e il trattamento. Eur Heart J 2010;31:281-9.
- Jander N, Minners J, Holme I, et al. Outcome of patients with low-gradient “severe” aortic stenosis and preserved ejection fraction. Circulation 2011;123:887-95.
- Ozkan A. Stenosi aortica “grave” a basso gradiente con frazione di eiezione ventricolare sinistra conservata. Cardiovasc Diagn Ther 2012;2:19-27.
- Dumesnil JG, Pibarot P, Akins C. Nuovi approcci per quantificare la gravità della stenosi aortica. Curr Cardiol Rep 2008;10:91-7.
- Pibarot P, Dumesnil JG. Valutazione della gravità della stenosi aortica: quando il gradiente non corrisponde all’area della valvola. Heart 2010;96:1431-3.
- Lancellotti P, Magne J. Impedenza valvuloarteriosa nella stenosi aortica: guardare il carico, ma non dimenticare il flusso. Eur J Echocardiogr 2011;12:354-7.
- Lancellotti P, Magne J, Donal E, et al. Clinical outcome in asymptomatic severe aortic stenosis insights from the new proposed aortic stenosis grading classification. J Am Coll Cardiol 2012;59:235-43.
- Monin JL, Lancellotti P, Monchi M, et al. Punteggio di rischio per prevedere l’esito in pazienti con stenosi aortica asintomatica. Circulation 2009;120:69-75.
- Lancellotti P, Donal E, Magne J, et al. Impact of global left ventricular afterload on left ventricular function in asymptomatic severe aortic stenosis: a two-dimensional speckle-tracking study. Eur J Echocardiogr 2010;11:537-43.
- Herrmann S, Störk S, Niemann M, et al. Low-gradient aortic valve stenosis myocardial fibrosis and its influence on function and outcome. J Am Coll Cardiol 2011;58:402-12.
- Zoghbi WA. Stenosi aortica “grave” a bassa gradazione con funzione sistolica normale: tempo di perfezionare le linee guida? Circulation 2011;123:838-40.
- Lancellotti P, Lebois F, Simon M, et al. Importanza prognostica dell’ecocardiografia Doppler quantitativa da sforzo nella stenosi aortica valvolare asintomatica. Circulation 2005;112:I377-82.
- Maréchaux S, Hachicha Z, Bellouin A, et al. Usefulness of exercise-stress echocardiography for risk stratification of true asymptomatic patients with aortic valve stenosis. Eur Heart J 2010;31:1390-7.
- Tarantini G, Covolo E, Razzolini R, et al. Sostituzione valvolare per stenosi aortica grave con basso gradiente transvalvolare e frazione di eiezione ventricolare sinistra superiore a 0,50. Ann Thorac Surg 2011;91:1808-15.
- Barasch E, Fan D, Chukwu EO, et al. Stenosi aortica isolata grave con funzione sistolica ventricolare sinistra normale e bassi gradienti transvalvolari: approfondimenti fisiopatologici e prognostici. J Heart Valve Dis 2008;17:81-8.