以下は私がルイス構造を描くときの手順です。 構造の中心原子を決める。 通常、最も電気陰性度の低い原子 (#”C” #) になります。
2. 他の原子が中心原子に単結合しているスケルトン構造を描きます:
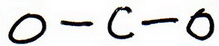
3. 各原子の周りに電子対を置き、それぞれが八重になるまで試行構造を描きます。
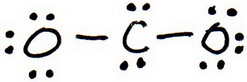
4. 試行構造中の価電子を数える(20)
5.試行構造中の価電子を数えなさい。 ここで、実際に利用できる価電子を数えてみましょう。 #C1+O2=1×4+2×6=16#です。
試行構造では電子が4つ多すぎます。
三重結合か二重結合を2つ入れる必要があります。
⑥新しい試行構造を描き、今度は結合を余分に挿入してください。
3つの可能性があります:
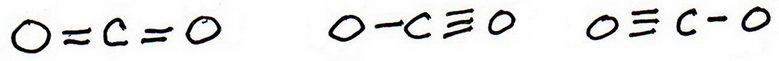
7. 先ほどと同じように、各原子に八重項を与えるために価電子を追加します:
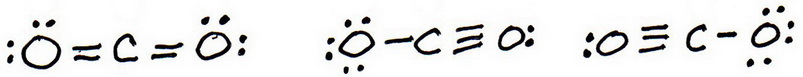
8. 各原子の形式電荷を計算します。
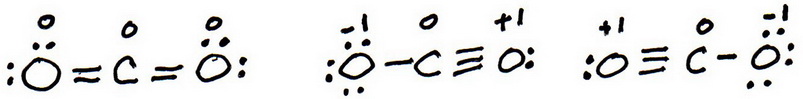
9.
最初の構造は形式電荷がないので、#”CO”_2# の最適なルイス構造は

となる。