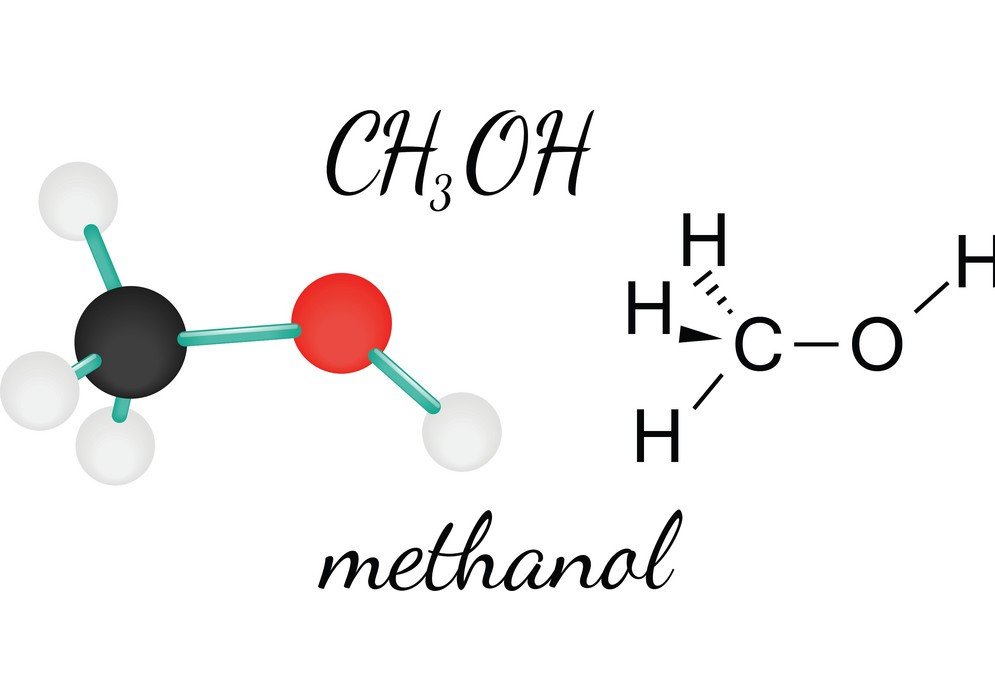
CH3OH sau metanolul este un lichid inflamabil, incolor și volatil, care are un miros distinctiv de alcool. Studiind metanolul, se poate ajunge să se cunoască forma moleculară, unghiul de legătură și polaritatea moleculei. Polaritatea CH3OH este una dintre caracteristicile vitale, deoarece ajută la cunoașterea celorlalte proprietăți ale compusului, cum ar fi solubilitatea sa, sarcinile electrice și multe altele. Pentru a înțelege polaritatea metanolului, să ne uităm mai întâi la unghiurile de legătură și la aranjamentul atomilor din molecula de CH3OH.

CH3OH Unghiuri de legătură
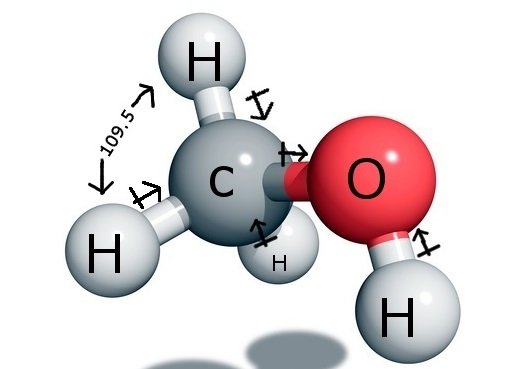
Astomul central de carbon formează patru legături în compus, trei cu atomul de hidrogen și una cu gruparea hidroxil ( OH). Și cum acest atom de carbon are o hibridizare sp3 și formează o formă de tetraedru, are unghiurile de legătură de 109,5 grade cu atomii săi de legătură.
În schimb, Oxigenul formează o legătură sigma, dar are două perechi singuratice, astfel că există o încovoiere a unghiului său de legătură din cauza forțelor de respingere a perechilor de legătură-pereche singuratică. Acest lucru scade unghiul de legătură la 104,5 grade.
Acum, Carbonul are un unghi de legătură de 109,5 grade cu toți cei trei atomi de Hidrogen și un unghi de legătură de 104,5 grade cu grupul hidroxil.
Este CH3OH polar?
Polaritatea oricărui compus dat depinde de momentul dipolar net al compusului. Acest moment dipolar net poate fi cunoscut prin observarea sarcinilor electrice de pe atomii din moleculă. Aici, atât atomii de carbon, cât și cei de oxigen ( care sunt considerați centre geometrice pentru acest compus) din metanol sunt atomi electronegativi. Dar Oxigenul este mai electronegativ decât Carbonul sau hidrogenul din compus.
CH3OH nu poate fi nepolar deoarece există o diferență de sarcini electrice între atomii din molecula de metanol. Oxigenul are o densitate mai mare de electroni datorită celor două perechi de electroni solitari. Acest lucru determină un dipol net îndreptat spre atomul de oxigen, ceea ce face ca CH3OH să fie polar.
Pe lângă sarcinile electrice, molecula de CH3OH este asimetrică, ceea ce anulează posibilitatea de nepolaritate. O moleculă nepolară are o structură simetrică, deoarece momentul dipol-dipolar este anulat. Dar cum există o curbură în forma metanolului, aceasta duce la formarea unei structuri asimetrice, ceea ce duce la formarea unei structuri asimetrice, rezultând că momentul dipolului electric net se termină negativ spre atomul de oxigen. Astfel, CH3OH este o moleculă polară.
Acum că știm polaritatea moleculei de CH3OH, să trecem în revistă câteva dintre proprietățile sale fizice:
- Punctul de fierbere al Metanolului ( CH3OH) este de 64,7 °C.
- Punctul de topire al Metanolului este de -97,6 °C.
- Greutatea moleculară a metanolului este de 32,04 g/mol.
- Este un solvent polar și este cunoscut și sub numele de alcool de lemn, deoarece a fost odinioară produs prin distilarea lemnului.
- Mirosul acestui compus este mai dulce în comparație cu cel al etanolului.
Utilizări ale CH3OH
- Metanolul este, de asemenea, utilizat pentru producerea de hidrocarburi și pentru sinteza altor substanțe chimice, cum ar fi formaldehida.
- Este utilizat ca antigel în conducte.
- CH3OH este, de asemenea, utilizat ca aditiv pentru benzină în mai multe țări datorită punctului său scăzut de topire.
- Compusul este, de asemenea, folosit ca și combustibil în combustia motoarelor interne.
- Multe companii farmaceutice folosesc metanolul pur pentru sinteza altor compuși.
Sper că acest articol vă ajută să înțelegeți polaritatea moleculei și proprietățile fizice și utilizările sale. CH3OH este o moleculă polară deoarece momentul dipol-dipolar nu se anulează din cauza formei sale asimetrice.