Stenoza aortică valvulară (SA) este cea mai frecventă boală valvulară în țările dezvoltate. Diagnosticul de SA este confirmat în mod clasic prin ecocardiografie, instrument standard pentru detectarea și evaluarea severității bolii (1). Cu toate acestea, evaluarea severității AS este încă dificilă. AS severă este de obicei definită ca fiind gradientul mediu >40 mmHg, aria valvei aortice (AVA) <1 cm2 și viteza maximă a jetului aortic >4,0 m/s (2). Cu toate acestea, se observă frecvent discrepanțe între gradientul mediu și aria valvei la un singur pacient (3). Aceste discrepanțe sunt ușor de înțeles la pacienții cu debit cardiac scăzut secundar fracției de ejecție redusă a LV, dar pot apărea și la pacienții cu funcție LV aparent conservată (4). În practica de zi cu zi, ele pot duce, potențial, la o subestimare a stenozei și a severității simptomelor și, astfel, la întârzierea necorespunzătoare a înlocuirii valvei aortice (AVR), ceea ce poate avea, la rândul său, un impact negativ asupra rezultatelor pacienților (5-7). În acest număr al revistei Cardiovascular Diagnosis and Therapy, OZKAN a trecut în revistă în mod elegant conceptul de SA cu gradient scăzut la pacienții cu funcție LV conservată (8).
Noua clasificare a gradului de clasificare a stenozei aortice
Recent, mai mulți autori au raportat că, sub aceeași denumire de SA severă (AVA <1 cm2), pot fi identificate mai multe entități care diferă în ceea ce privește debitele transvalvulare și gradienții de presiune dezvoltați (9-11). Primul care a subliniat importanța integrării relației valvă-gradient la modelul de flux a fost grupul lui Pibarot et al. (5), în timp ce Miners et al. (3) au fost primii care au arătat clar inconsecvențele pentru clasificarea severității SA și au propus împreună cu Dumesnil et al. (6) noua clasificare a SA. La pacienții cu un AVA <1 cm2, pot fi identificate patru categorii de SA cu gradient de flux: flux normal/gradient scăzut (NF/LG), flux normal/gradient ridicat (NF/HG), flux scăzut/gradient ridicat (LF/HG) și flux scăzut/gradient scăzut (LF/LG). LF este definit ca un volum cerebral indexat al LV <35 ml/m2 și LG ca un gradient mediu de presiune trans-aortică <40 mmHg (12).
Flux normal/gradient scăzut
Acest model este observat la 31-38% dintre pacienți și pare să identifice un grup de pacienți cu un grad mai puțin sever de SA – incoerență inerentă conținută în ghiduri – sau care a fost expus la boală pentru o perioadă mai scurtă de timp. Această entitate se caracterizează printr-o funcție miocardică longitudinală a LV conservată, rezultând un nivel mai scăzut al BNP și un scor de risc Monin’s (12,13). Prognosticul acestor pacienți pare a fi relativ conservat în comparație cu celelalte categorii.
Flux normal – gradient înalt
Acest model reprezintă entitatea cea mai răspândită (39-72%) și este în deplină concordanță cu criteriile propuse de ghiduri (4,5,12). În comparație cu grupul NF/LG, deși funcția longitudinală a LV este păstrată, BNP este mai mare și rata de supraviețuire fără evenimente cardiace a NF/HG este redusă. Mai mult, pacienții cu NF/HG par să aibă o SA mai severă, sugerând o expunere mai îndelungată la această boală progresivă. Atunci când sunt simptomatici, acești pacienți sunt îndrumați în mod clasic pentru AVR, în timp ce atunci când sunt asimptomatici, managementul acestor pacienți subliniază necesitatea unei stratificări optimizate a riscului.
Flux scăzut – gradient ridicat
Acest model reprezintă 8% dintre pacienții cu SA severă (4,12). Este caracterizat de un volum de accident vascular cerebral indexat al LV <35 ml/m2 în ciuda unei fracții de ejecție a LV conservate, a unui nivel ridicat al BNP și a scorului de risc Monin și a unei reduceri semnificative a funcției longitudinale a LV (14). De remarcat, fracția de ejecție a LV este o estimare brută a funcției sistolice a LV. Fracția de ejecție a LV este influențată atât de funcția miocardică intrinsecă, cât și de geometria cavității LV. Prin urmare, pentru un grad similar de scurtare miocardică intrinsecă, fracția de ejecție a LV va avea tendința de a crește în raport cu gradul de remodelare concentrică a LV. Prin urmare, fracția de ejecție a LV poate subestima în mod semnificativ gradul de afectare miocardică în prezența remodelării concentrice a LV, așa cum este în general cazul pacienților cu SA. Prin urmare, ceea ce este normal pentru un LV cu o geometrie normală poate fi anormal pentru un LV cu remodelare concentrică. Mai mult, reducerea debitului LV (legată de disfuncția miocardică intrinsecă și remodelarea semnificativă a LV) poate, la rândul său, să aibă ca rezultat gradienți trans-valvulari mai mici decât se așteaptă. Rezultatul acestor pacienți este aproape identic cu cel al pacienților cu NF/HG. Atunci când sunt simptomatici, acești pacienți tind să aibă o supraviețuire mai bună dacă sunt tratați chirurgical.
Flux scăzut – gradient scăzut
Prevalența modelului LF/LG pare a fi mai mică decât cea raportată inițial. Această entitate reprezintă 7% la pacienții asimptomatici și până la 15-35% la pacienții simptomatici (4-6,12,14). Acest pattern, și anume SA paradoxal cu debit scăzut, reprezintă o entitate clinică dificilă care a fost recent evidențiată. Este asociat cu o remodelare concentrică mai pronunțată a LV, o cavitate LV mai mică, o postîncărcare globală crescută a LV, disfuncție miocardică intrinsecă, fibroză miocardică și un prognostic sumbru (12,15). La pacienții asimptomatici, am arătat că probabilitatea de a rămâne în viață fără AVR la 3 ani a fost de 5 ori mai mică decât pentru modelul NF/LG și de 4,3 ori mai mare decât în grupul NF/HG (12). Această entitate clinică este adesea diagnosticată greșit, ceea ce poate duce la o subestimare a severității SA și, prin urmare, la subutilizarea sau la întârzierea necorespunzătoare a intervenției chirurgicale. Este important să se recunoască această entitate pentru a nu refuza intervenția chirurgicală unui pacient simptomatic cu AVA și LG mici.
Discordanță între gradient și suprafața valvulară
Cauzele potențiale ale discordanței dintre AVA și gradient la pacienții cu fracție de ejecție LV conservată includ (I) erori de măsurare; (II) dimensiuni mici ale corpului; (III) AS paradoxal cu flux scăzut; și (IV) clasificare inconsecventă legată de discrepanțele intrinseci în criteriile ghidurilor (4,6,7,10,11). În primul rând, pacienții cu dimensiuni corporale și LV mici pot prezenta un gradient de presiune trans-valvulară mai mic din cauza unui volum cerebral mai mic, deși normal. În al doilea rând, volumul de accident vascular cerebral și, prin urmare, AVA poate fi subestimat din cauza subestimării tractului de ieșire al LV și/sau a poziționării greșite a volumului eșantionului Doppler cu unde pulsate. Mai multe metode pot fi utilizate pentru a corobora măsurătorile Doppler-ecocardiografice ale volumului de accident vascular cerebral și AVA. De exemplu, în absența unei regurgitări mitrale semnificative, volumul vascular cerebral poate fi estimat cu ușurință prin metoda Simpson (metodă volumetrică de măsurare a fracției de ejecție și a volumelor LV). Dacă volumul de accident vascular cerebral măsurat prin aceste metode independente este în concordanță cu volumul de accident vascular cerebral măsurat în tractul de ieșire al LV, se poate fi liniștit în ceea ce privește acuratețea măsurării volumului de accident vascular cerebral. În al treilea rând, LF/LG paradoxal reprezintă o nouă entitate în care starea LF rezultă atât din remodelarea concentrică a LV, cât și din reducerea funcției longitudinale subendocardice. Acest lucru conturează absența unei estimări eronate a severității AS. În al patrulea rând, în unele cazuri, discrepanța în relația gradient-arie valvulară poate fi legată de inconsecvențele din orientările actuale. O armonizare a definiției AS severă poate reclasifica unii dintre acești pacienți cu AS „severă” în AS „moderată”. Atunci când se combină datele clinice prospective actuale cu datele hemodinamice eco și invazive anterioare, se pare că un gradient de 40 mmHg se potrivește mai mult cu o suprafață valvulară de 0,8 cm2, în timp ce o suprafață valvulară de 1 cm2 se referă la un gradient mediu de 26 mmHg (3,6,16). Mai mult, atunci când există o discordanță între aria valvulară (în intervalul sever) și gradientul (în intervalul moderat) la pacienții cu fracția de ejecție LV conservată, poate fi necesară o evaluare ecocardiografică Doppler mai cuprinzătoare și, eventual, alte teste de diagnostic (BNP, scorul de calciu prin tomografie computerizată multislice, ecocardiografie de efort/dobutamină de efort) pentru a confirma severitatea bolii și a ghida managementul terapeutic.
Implicații clinice și management
În practica de zi cu zi, evaluarea severității AS ar trebui să integreze modelul flux-gradient la măsurarea clasică a AVA. Ca regulă generală, un gradient trans-valvular scăzut (<40 mmHg) sau o viteză (<4 m/s) nu exclude prezența unei SA severe la pacienții cu AVA mică și fracție de ejecție LV păstrată. În plus, o fracție de ejecție a LV conservată (>50%) nu exclude prezența disfuncției sistolice miocardice și a unui flux trans-valvular scăzut în SA. Pacienții cu SA NF/LG au în mod clasic o disfuncție subendocardică inexistentă sau minimă și un rezultat relativ conservat. În această categorie NF/LG, indicația pentru AVR ar trebui să se limiteze la pacienții la care simptomele pot fi atribuite în mod clar AS. În categoria NF/HG, AVR (chirurgicală sau percutanată) este singura terapie care îmbunătățește semnificativ atât supraviețuirea, cât și simptomele. Atunci când sunt asimptomatici, stratificarea riscului individual poate ajuta la identificarea pacienților care pot beneficia de o intervenție chirurgicală precoce. În celelalte categorii, starea LF reprezintă un martor al disfuncției miocardice intrinseci și un proces de boală mai avansat. Pacienții simptomatici cu LF/HG ar trebui să beneficieze, de asemenea, de o AVR promptă. Atunci când sunt asimptomatici, ar trebui, de asemenea, încurajată stratificarea individuală a riscului. Ecocardiografia de efort poate fi de interes prin demascarea pacienților cu complianță valvulară limitată și/sau rezervă contractilă LV epuizată (17,18). LF/LG paradoxală transmite un rezultat prost chiar și la pacienții asimptomatici. În această categorie, deși beneficiul intervenției chirurgicale nu este dovedit, AVR poate fi probabil benefică la pacienții simptomatici selectați (7,19,20) (tabelul 1) (tabelul 1). În practica clinică, constatarea acestei entități este dificilă. Înainte de a lua în considerare intervenția chirurgicală, simptomele trebuie să fie potrivite cu severitatea SA. La pacienții cu risc scăzut, poate fi recomandată AVR. La pacienții cu risc ridicat, sunt necesare studii suplimentare privind rezultatele pentru a determina modalitatea cea mai adecvată și momentul tratamentului.
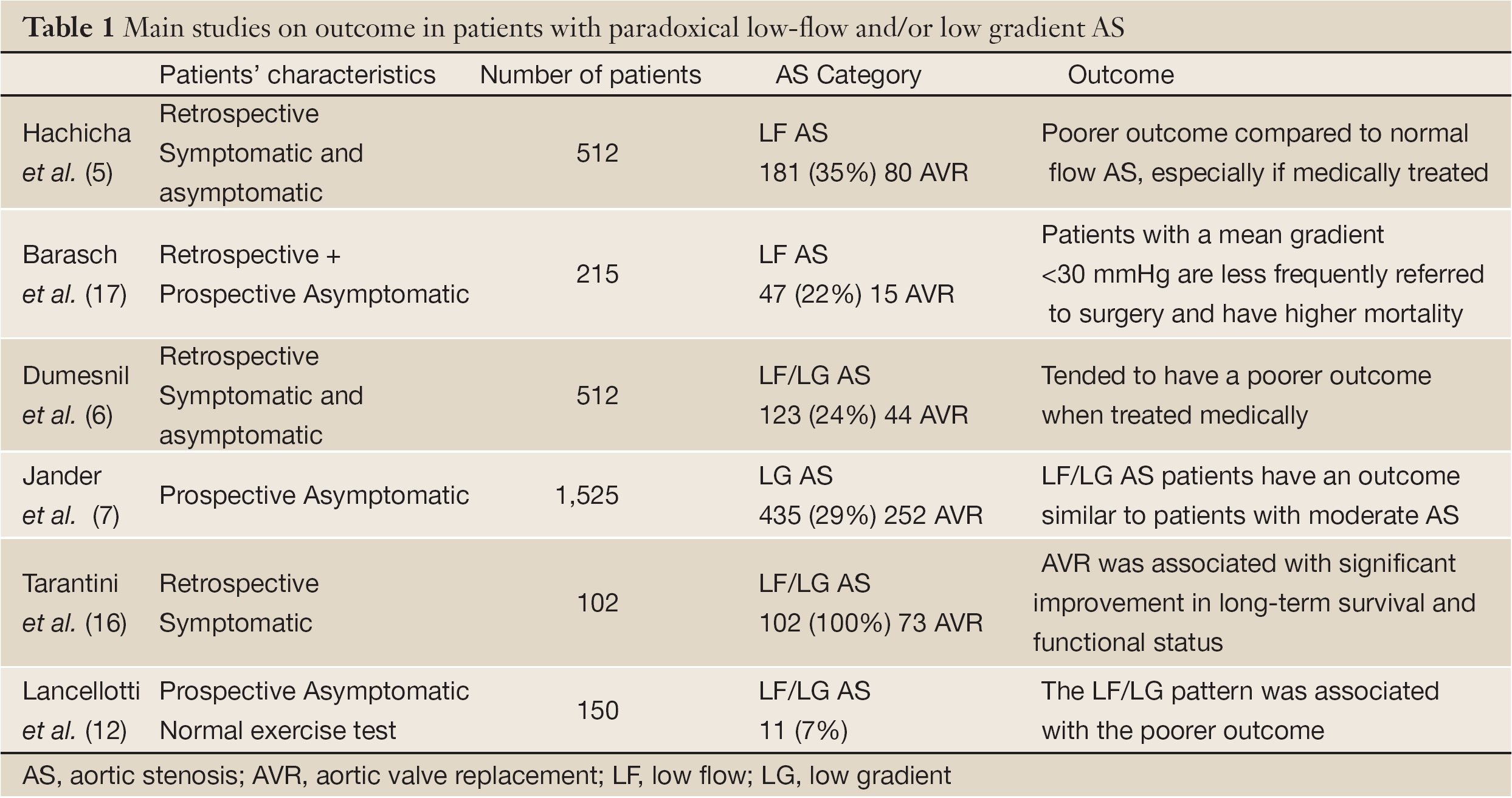
Tabel complet
Recunoștințe
Dezvăluiri: Autorii nu declară niciun conflict de interese.
- Lancellotti P, Donal E, Magne J, et al. Stratificarea riscului în stenoza aortică asimptomatică moderată până la severă: importanța interacțiunii valvulare, arteriale și ventriculare. Heart 2010;96:1364-71.
- Bonow RO, Carabello BA, Kanu C, et al. Liniile directoare ACC/AHA 2006 pentru managementul pacienților cu boli cardiace valvulare: un raport al Grupului de lucru pentru ghiduri de practică al Colegiului American de Cardiologie/Asociației Americane de Cardiologie/American Heart Association (comitet de redactare pentru revizuirea Liniilor directoare din 1998 pentru managementul pacienților cu boli cardiace valvulare): elaborat în colaborare cu Societatea Anesteziștilor Cardiovasculari: aprobat de Societatea pentru Angiografie și Intervenții Cardiovasculare și Societatea Chirurgilor Toracici. Circulation 2006;114:e84-231.
- Minners J, Allgeier M, Gohlke-Baerwolf C, et al. Gradarea inconsecventă a stenozei valvei aortice de către ghidurile actuale: studii hemodinamice la pacienții cu funcție ventriculară stângă aparent normală. Heart 2010;96:1463-8.
- Adda J, Mielot C, Giorgi R, et al. Low-Flow, Low-Gradient Severe Aortic Stenosis Severe Despite Normal Ejection Fraction Is Associated With Severe Left Ventricular Dysfunction as Assessed by Speckle-Tracking Echocardiography: A Multicenter Study. Circ Cardiovasc Imaging 2012;5:27-35.
- Hachicha Z, Dumesnil JG, Bogaty P, et al. Paradoxal low-flow, low-gradient severe aortic stenosis despite preserved ejection fraction is associated with higher afterload and reduced survival. Circulation 2007;115:2856-64.
- Dumesnil JG, Pibarot P, Carabello B. Stenoza aortică severă paradoxală cu flux scăzut și/sau gradient scăzut în ciuda fracției de ejecție ventriculară stângă conservate: implicații pentru diagnostic și tratament. Eur Heart J 2010;31:281-9.
- Jander N, Minners J, Holme I, et al. Outcome of patients with low-gradient „severe” aortic stenosis and preserved ejection fraction. Circulation 2011;123:887-95.
- Ozkan A. Low gradient „severe” aortic stenosis with preserved left ventricular ejection fraction. Cardiovasc Diagn Ther 2012;2:19-27.
- Dumesnil JG, Pibarot P, Akins C. New approaches to quantifying aortic stenosis severity. Curr Cardiol Rep 2008;10:91-7.
- Pibarot P, Dumesnil JG. Evaluarea severității stenozei aortice: când gradientul nu se potrivește cu aria valvei. Heart 2010;96:1431-3.
- Lancellotti P, Magne J. Impedanța valvuloarterială în stenoza aortică: uitați-vă la sarcină, dar nu uitați de flux. Eur J Echocardiogr 2011;12:354-7.
- Lancellotti P, Magne J, Donal E, et al. Clinical outcome in asymptomatic severe aortic stenosis insights from the new proposed aortic stenosis grading classification. J Am Coll Cardiol 2012;59:235-43.
- Monin JL, Lancellotti P, Monchi M, et al. Risk score for predicting outcome in patients with asymptomatic aortic stenosis. Circulation 2009;120:69-75.
- Lancellotti P, Donal E, Magne J, et al. Impactul postîncărcării globale a ventriculului stâng asupra funcției ventriculare stângi în stenoza aortică severă asimptomatică: un studiu de urmărire speckle bidimensională. Eur J Echocardiogr 2010;11:537-43.
- Herrmann S, Störk S, Niemann M, et al. Low-gradient aortic valve stenosis myocardial fibrosis and its influence on function and outcome. J Am Coll Cardiol 2011;58:402-12.
- Zoghbi WA. Stenoza aortică „severă” cu grad scăzut de gradient cu funcție sistolică normală: este timpul să rafinăm liniile directoare? Circulation 2011;123:838-40.
- Lancellotti P, Lebois F, Simon M, et al. Prognostic importance of quantitative exercise Doppler echocardiography in asymptomatic valvular aortic stenosis. Circulation 2005;112:I377-82.
- Maréchaux S, Hachicha Z, Bellouin A, et al. Utilitatea ecocardiografiei de efort pentru stratificarea riscului la pacienții cu stenoză valvulară aortică cu adevărat asimptomatică. Eur Heart J 2010;31:1390-7.
- Tarantini G, Covolo E, Razzolini R, et al. Înlocuirea valvei pentru stenoza aortică severă cu gradient transvalvular scăzut și fracție de ejecție ventriculară stângă mai mare de 0,50. Ann Thorac Surg 2011;91:1808-15.
- Barasch E, Fan D, Chukwu EO, et al. Stenoză aortică severă izolată cu funcție sistolică ventriculară stângă normală și gradiente transvalvulare scăzute: perspective fiziopatologice și prognostice. J Heart Valve Dis 2008;17:81-8.
.