
In precedenza, la scienza dietro la vita basata sul silicio è stata determinata essere fantascienza. I composti del silicio sono limitati a disposizioni cristalline invariabili, mentre i composti del carbonio, cioè gli organici, possono formare una grande varietà di molecole tali che qualsiasi disposizione molecolare stabile potrebbe formarsi spontaneamente e che la selezione naturale favorirebbe quelle molecole che sostengono la vita. Nella competizione prebiotica tra le basi di silicio e carbonio per la vita, il carbonio molto probabilmente dominerebbe. Ma consideriamo l’alternativa in cui l’acqua fosse sostituita da una sostanza chimica molto familiare, ma improbabile. Potrebbe esistere la vita in un mondo dominato da oceani, laghi e fiumi di ammoniaca?
La rottura
L’ammoniaca è una sostanza tossica per gli esseri umani, gli insetti e persino i batteri. È l’ingrediente principale di alcuni solventi industriali e soluzioni di pulizia ed è pericolosa per l’ambiente. L’ammoniaca è persino una parte essenziale di una ricetta usata per fare esplosivi ad alto rendimento. Come potrebbe qualcosa di così letale come l’ammoniaca permettere la nascita e l’evoluzione degli organismi viventi? Che ci crediate o no, l’ammoniaca ha molte delle stesse proprietà molecolari di un altro composto familiare che è essenziale per la vita: l’acqua. Alcuni astrobiologi propongono che la vita possa evolversi in un mezzo ammoniacale nello stesso modo in cui la vita sulla Terra è cresciuta in un mezzo idratato. Immaginate: la stessa sostanza che è nota per sciogliere i metalli, bruciare la pelle, inquinare l’ambiente ed esplodere se mescolata impropriamente potrebbe benissimo essere l'”acqua della vita” su alcuni mondi extraterrestri (e non sto parlando di Dune).
Per prima cosa consideriamo perché l’ammoniaca è un potenziale candidato. L’ammoniaca e l’acqua sono entrambe molecole polari. Le elettronegatività degli atomi di ossigeno e di azoto sono maggiori dell’elettronegatività delle loro controparti di idrogeno. La differenza di elettronegatività tra l’atomo centrale (azoto o ossigeno) e gli atomi di idrogeno fa sì che le molecole diventino polari. L’atomo centrale adotta una carica leggermente negativa e gli idrogeni diventano leggermente positivi. Questo rende l’ammoniaca e l’acqua potenti solventi, in quanto possono dissolvere sali e piccole molecole polari.
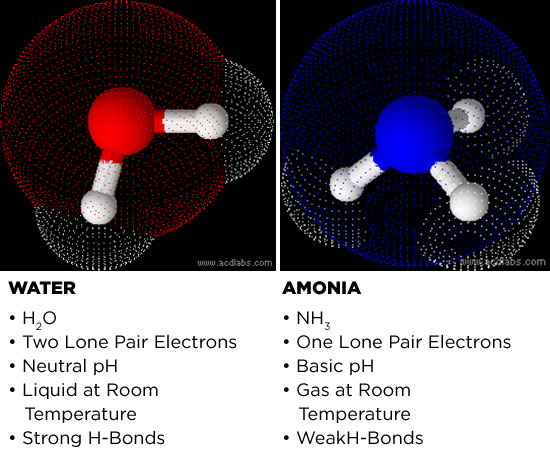
Diverse proprietà fisiche dell’acqua sono condivise anche dall’ammoniaca. Entrambi i mezzi possono condurre l’elettricità, anche se debolmente, e la coordinazione degli idrogeni caricati positivamente con parti caricate negativamente su molecole vicine forma una delle più forti forze intermolecolari conosciute in chimica: il legame idrogeno. Questo è analogo a prendere un oggetto con una carica positiva ad una estremità e legarlo elettrostaticamente ad una carica negativa su un altro oggetto. In termini profani, i legami a idrogeno permettono alle molecole polari di attaccarsi molto bene l’una all’altra, da qui la ragione per cui l’acqua ha una tensione superficiale e un punto di ebollizione così alti.
In questa misura, l’acqua è un solvente versatile: può sciogliere quasi “tutto”, e la solubilità è essenziale in condizioni prebiotiche. Può sciogliere molti sali e piccole molecole organiche polari come zuccheri e aminoacidi. La solubilità dei composti organici e dei sali è molto importante per la vita perché tampona le miscele di reazione per resistere ai cambiamenti del pH, della salinità e persino degli stati di ossidazione. Un ambiente che supporta al meglio la vita è quello con concentrazioni stabili di biomolecole essenziali.
Un’altra caratteristica molto importante delle proprietà fisiche dell’acqua è l’effetto idrofobico dei grandi composti non polari. Le sostanze polari e non polari non si mescolano molto bene in soluzione, ed è per questo che le molecole non polari tendono a conglomerarsi in una soluzione di molecole polari. In altre parole: le molecole non polari si attaccano l’una all’altra molto più strettamente quando sono circondate da molecole polari.
L’effetto idrofobico è cruciale nel processo di abiogenesi perché guida la formazione di micelle e proteine. Senza l’effetto idrofobico, i lipidi non potrebbero ricucire per formare le membrane cellulari, e i polimeri di aminoacidi non potrebbero piegarsi per formare proteine ed enzimi funzionali.
Mentre l’ammoniaca può avere la capacità di formare legami idrogeno, la sua polarità impallidisce in confronto a quella dell’acqua. L’ammoniaca è meno capace di formare legami idrogeno e di conseguenza anche l’effetto idrofobico e la solubilità delle molecole organiche sono più deboli.
Questo presenta problemi per l’abiogenesi. Le piccole molecole bioorganiche non si dissolvono molto bene nell’ammoniaca. Le proteine e le membrane possono essere instabili in una soluzione di ammoniaca perché potrebbero non piegarsi correttamente. Le membrane e i lipidi diventano un problema ancora più grande; se le membrane cellulari non sono sufficientemente compatte, allora le cellule potrebbero rompersi anche con lievi cambiamenti ambientali. La vita sarebbe meno adattabile in un ambiente di ammoniaca che in un ambiente di acqua.
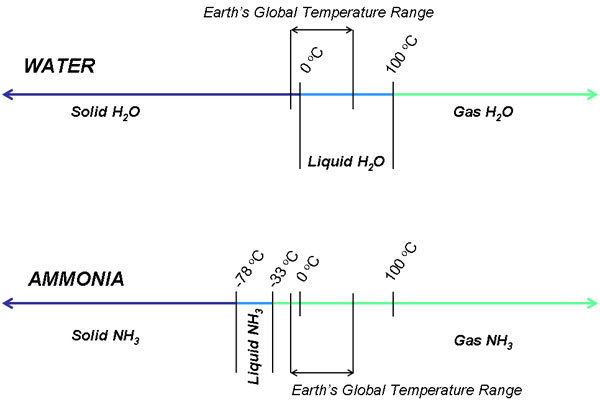
La stessa stabilità dell’ammoniaca liquida desta preoccupazione. Teoricamente, la vita può essere sostenuta solo in un liquido, non in un gas o in un solido. Se viene fatta bollire troppo velocemente o troppo facilmente, gli organismi potrebbero avere più difficoltà ad adattarsi all’ambiente. L’ammoniaca esiste come gas a temperatura ambiente, mentre l’acqua è stabile come liquido da un intervallo di temperatura da 0 a 100 gradi Celsius. Ciò è dovuto alla forza del legame a idrogeno: più forti sono i legami a idrogeno, più è probabile che le molecole rimangano insieme abbastanza a lungo da condensarsi in un liquido. L’ammoniaca ha un debole legame a idrogeno, ed è per questo che la temperatura deve essere abbassata drasticamente sotto la normale pressione atmosferica per stabilizzare l’ammoniaca allo stato liquido; stiamo parlando di un mondo che deve subire un’era glaciale di 4 miliardi di anni. Un pianeta freddo e morto è difficilmente un candidato ideale per sostenere la vita.

Superficie di Andoria.
Il punto di ebollizione dell’ammoniaca è di -33 gradi Celsius sotto 14,7 psi di pressione, il che significa che l’ammoniaca liquida è stabile sotto questa temperatura solo alla pressione atmosferica della Terra. Supponendo per un momento che il ripiegamento, la congerie e la solubilità delle molecole organiche siano termodinamicamente probabili, una temperatura globale dovrebbe essere mantenuta da -78 gradi Celsius e -33 gradi a 14,7 psi. Questa è una fascia troppo stretta perché gli organismi possano prosperare; qualsiasi lieve fluttuazione del clima potrebbe effettivamente minacciare la sopravvivenza della vita basata sull’ammoniaca. Il metabolismo dei nutrienti e la replicazione degli organismi sarebbero interrotti da periodi di bassi e alti estremi.
L’unica soluzione alternativa per questo problema è la condensazione di un gas usando una pressione atmosferica più alta piuttosto che una temperatura più bassa. Il gas può essere condensato in un liquido sotto pressioni estreme, e la temperatura può essere mantenuta ben al di sopra del suo normale punto di ebollizione (che è una buona notizia per un clima ammoniacale in cui la vita richiede calore per prosperare). L’ammoniaca si condensa in un liquido sotto una pressione equivalente a 12,1 mila atmosfere terrestri a circa 37 gradi Celsius. Purtroppo, dobbiamo ancora scoprire o ipotizzare un modo in cui un pianeta potrebbe ospitare un’atmosfera così densa. Venere, un pianeta terrestre con l’atmosfera più densa oggi conosciuta, ha un valore di pressione di 93 bar in superficie; questo difficilmente soddisfa la richiesta atmosferica di 12.000 bar. Giove, la prossima scelta migliore, ha solo una pressione massima di circa 1000 bar al centro del pianeta; di nuovo, difficilmente ideale per i nostri scopi. È improbabile che pianeti simili abbiano pressioni atmosferiche abbastanza alte da condensare l’ammoniaca in un liquido, anche se questo non significa che la vita basata sull’ammoniaca non possa emergere con qualche altro mezzo.
Il Verdetto Finale
La vita basata sull’ammoniaca non è un tema importante di Star Trek, e mi sono sempre chiesto perché non sia mai stata inclusa negli show. Sfortunatamente, è improbabile che sia un fatto scientifico. È importante notare che molte cose inizialmente considerate impossibili nella scienza sono state alla fine dimostrate dalla scienza, o almeno in una certa misura. Come sottolineo sempre nei miei articoli: solo perché qualcosa sembra altamente improbabile, non significa che non possa accadere. Dobbiamo ancora scoprire la vita basata sull’ammoniaca, o qualsiasi vita altrove per quella materia, prima che qualcuno, anche io, possa dire che gli alieni ammoniacati possono o non possono esistere. In assenza di prove assolute, la speculazione è il meglio in cui possiamo sperare.
Su questa nota, vorrei concludere con questo impressionante estratto modificato da Cosmos di Carl Sagan, in cui ipotizza un probabile scenario in cui la vita potrebbe evolversi su un mondo come Giove.
Solo perché qualcosa sembra improbabile che si verifichi, siamo sempre stupiti nella scienza di scoprire che a volte, non importa quanto improbabile, è vero il contrario. Anche se gli organismi a base di ammoniaca non possono esistere secondo i nostri standard terrestri, ciò non implica in alcun modo che non possa accadere in nessun altro modo.
Tom Caldwell ha conseguito una laurea in biochimica alla UCLA. Attualmente sta lavorando per conseguire un dottorato di ricerca in biologia molecolare.
Si